Sra. Editora:
El seudotumor inflamatorio es una lesión expansiva caracterizada por un infiltrado de células inflamatorias y miofibroblastos, de etiología desconocida, que afecta al tejido pulmonar en niños y jóvenes y rara vez a los adultos. Su pronóstico suele ser favorable, ya que la invasión a distancia suele ser rara. Se han descrito algunos casos de seudotumor inflamatorio cardiaco en niños y jóvenes, y sólo 15 casos en adultos1, 2, 3, 4, 5, confinado al endocardio o las válvulas1. En los adultos, se ha descrito en cualquier cavidad, con aspecto de mixoma o fibroelastoma bien definido, que puede generar numerosos síntomas4. Aunque el tratamiento es la excisión del tumor siempre que sea posible1, se ha descrito algún caso de regresión con corticoides6. Las recurrencias no son infrecuentes (13-37%), aunque el pronóstico suele ser favorable. Existe un subtipo de seudotumor inflamatorio, el calcificado, que podría corresponder al estadio evolucionado del seudotumor inflamatorio, con abundantes fibras de colágeno, calcificaciones distróficas2 y patrón inmunohistoquímico característico (positividad para actina específica de músculo, FXIIIa, CD68 y vimentina y negatividad para CD34). Aunque ocasionalmente el seudotumor inflamatorio puede presentar mitosis, la ausencia de atipia lo distingue del sarcoma verdadero3. No hemos encontrado en la literatura ningún caso descrito de seudotumor inflamatorio primario cardiaco calcificado en adultos y sólo 2 casos en niños2, 7, como tampoco de afección transmural.
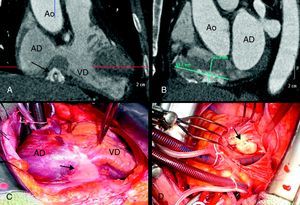
Varón de 57 años, no fumador, fue remitido por angina progresiva, con exploración y electrocardiograma normales. La coronariografía mostró estenosis del 95% en la arteria circunfleja, tratada mediante implantación de stent metálico, y oclusión de la coronaria derecha proximal. Se identificó una masa calcificada adyacente al diafragma, con compresión extrínseca de la coronaria derecha. Se realizaron ecocardiogramas transtorácico y transesofágico, que mostraron dilatación de la aurícula derecha y gran masa calcificada en la región posterior del surco auriculoventricular, con protrusión en el anillo derecho y gradiente transtricuspídeo. En la resonancia magnética cardiaca, se evidenció captación heterogénea de contraste que indicaba vascularización y signos de elevado contenido fibroso. En la tomografía computarizada multicorte, se identificó una gran masa calcificada (63,7×22,9 mm), mal definida e infiltrante en el surco (Figura 1A y B). No se evidenciaron signos de hipermetabolismo o metástasis en la tomografía por emisión de positrones. Previo consentimiento informado, se realizó cirugía con intención diagnóstica y terapéutica. Tras esternotomía, se identificó una gran calcificación en el pericardio anterior (Figura 1C), las paredes lateral e inferior de la aurícula derecha y el surco auriculoventricular, con inclusión de la coronaria derecha e infiltración transmural de la base de ambos ventrículos, protruyendo 4 cm hacia el interior del anillo tricuspídeo (Figura 1D). El análisis histológico perioperatorio evidenció infiltrado inflamatorio sin evidencia de maliginidad. La masa se resecó parcialmente y se precisó reconstrucción del surco con pericardio bovino e implantación de prótesis biológica tricuspídea. Como consecuencia de la cirugía, se implantó marcapasos definitivo por bloqueo auriculoventricular completo. El análisis histopatológico posterior identificó un infiltrado inflamatorio de linfocitos, células plasmáticas y ocasionales células mesenquimales, sin mitosis (Figura 2A-C), y áreas de colágeno con calcificaciones secundarias (cuerpos de psammoma) (Figura 2A). La inmunohistoquímica mostró positividad para actina específica de músculo, CD68, CD4 (Figura 2D y E), CD8, y negatividad para desmina, proteína S100 y CD34, todo ello compatible con el diagnóstico de seudotumor inflamatorio calcificado. A los 2 años de seguimiento, el paciente está asintomático y sin evidencia de recurrencia o progresión del tumor.
Figura 1. A y B: imágenes de tomografía de la masa calcificada en el surco auriculoventricular. C: aspecto de la calcificación del seudotumor durante la cirugía (flecha). D: protrusión de la lesión en el anillo tricuspídeo (flecha) AD: aurícula derecha; Ao: aorta; VD: ventrículo derecho.
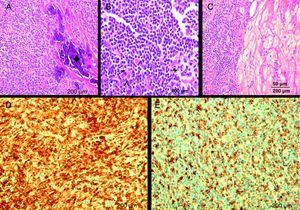
Figura 2. Imágenes histológicas. A-C: tinción de hematoxilina-eosina con infiltración por linfocitos maduros (*), histiocitos (punta de flecha), células plasmáticas (+) y calcificación (♦) en miocardio. D: células CD4+ (linfocitos T). E: células CD68+ (histiocitos). Barra=50 μm.
Autor para correspondencia: e.zamora@telefonica.net