El tratamiento de la cardiopatía isquémica aguda ha evolucionado notablemente en las últimas décadas, lo que ha contribuido a mejorar el pronóstico de los pacientes. Un rápido diagnóstico y un tratamiento precoz en la fase aguda del evento isquémico cardiaco suponen una mayor supervivencia y menor riesgo de desarrollar insuficiencia cardiaca, así como otras complicaciones concomitantes. Así pues, se ha demostrado que la administración de ciertos fármacos anticoagulantes y antiagregantes, así como bloqueadores beta, inhibidores de la enzima de conversión de angiotensina y estatinas, en la fase aguda del infarto, puede ayudar a mejorar la supervivencia y reducir el riesgo de complicaciones. En este artículo se revisa brevemente el tratamiento farmacológico inicial a administrar en las primeras 48 h de un infarto agudo de miocardio con elevación del segmento ST.
Palabras clave
El infarto agudo de miocardio con elevación del segmento ST (IAMCEST) continúa siendo hoy en día uno de los problemas de salud más relevante de los países desarrollados. En las últimas décadas ha habido un avance importante en cuanto a su diagnóstico y manejo terapéutico gracias al conocimiento de las bases fisiopatológicas de la enfermedad. Así pues, se han añadido a los estudios clásicos con aspirina y heparina, en la fase aguda del infarto, nuevos estudios con heparina de bajo peso molecular, inhibidores directos de la trombina e inhibidores del factor Xa, así como otros fármacos antiagregantes, como clopidogrel y los inhibidores de la glucoproteína IIb/IIIa. También un tema bien estudiado es el papel de los fármacos bloqueadores beta en la fase aguda del IAMCEST, así como el de los fármacos inhibidores de la enzima de conversión de angiotensina (IECA) y las estatinas.
En este artículo se describe el manejo en las primeras 48h del paciente que se presenta con un IAMCEST, y se comentan las medidas generales adecuadas y el tratamiento farmacológico a administrar como terapia añadida a la reperfusión coronaria y que significará mejora en la supervivencia y disminución del riesgo de complicaciones.
MEDIDAS INMEDIATASEn las primeras horas del ingreso del paciente con IAMCEST debemos mantener un control estricto de las constantes vitales, asegurar una vía venosa permeable y monitorización cardiaca (tabla 1). El paciente debe permanecer en reposo absoluto durante las primeras 12–24 h1,2.
Recomendaciones generales en la fase aguda según las guías de la Sociedad Europea de Cardiología1 sobre el infarto agudo de miocardio con elevación del segmento ST
| Fármaco | Dosis | Recomendación | Nivel de evidencia |
| Cloruro mórfico i.v. | 4-8mg, dosis adicionales de 2mg cada 5–15min | I | C |
| Oxígeno (2–4l/min) si hay disnea o signos de IC | I | C | |
| Ansiolíticos | IIa | C |
i.v.: intravenoso.
El paciente debe recibir una dieta baja en grasas saturadas y colesterol. Se debe restringir el aporte sódico de la dieta a los pacientes hipertensos o afectos de insuficiencia cardiaca. Los pacientes diabéticos deben recibir una dieta apropiada para diabético1,2. En diversos estudios se ha relacionado la hiperglucemia al ingreso con un incremento de la mortalidad en pacientes diabéticos que presentan IAMCEST, por lo que parece razonable mantener concentraciones de glucemia en valores normales3,4. Aunque se había apuntado a que un tratamiento estricto inicial con perfusión de insulina, seguido de dosis múltiples de insulina, reducía la mortalidad, en el estudio DIGAMI-2 se observó que, mientras se mantuviera un correcto control de las glucemias, la mortalidad no difería entre los distintos grupos de tratamiento5. Se ha indicado mantener una concentración de glucemia de 90–140mg/dl y evitar valores < 80–90mg/dl, ya que la hipoglucemia también conlleva un peor pronóstico6,7.
OxigenoterapiaEn los pacientes que presenten dificultad respiratoria, signos de insuficiencia cardiaca (IC) o saturación de oxígeno < 90%, se debe aportar oxígeno a 2–4l/min. Se ha indicado la oxigenoterapia a todo paciente con SCACEST durante las primeras 6 h1,2.
NitratosNo está justificado el uso sistemático de nitratos en pacientes con IAMCEST8,9. Se administrará nitroglicerina sublingual o intravenosa como tratamiento del dolor de origen isquémico, y está claramente indicada la administración de nitroglicerina intravenosa como vasodilatador en pacientes con hipertensión arterial o IC. No se deberá administrar si la presión arterial sistólica es < 90mmHg, o si el paciente se presenta con bradicardia (frecuencia cardiaca < 50 lat/min) o taquicardia (> 100 lat/min)1,2.
AnalgesiaEl tratamiento del dolor es de gran importancia, tanto para el confort del paciente como para paliar el efecto de la activación simpática secundaria al dolor, que causa vasoconstricción e incrementa el trabajo cardiaco1,10. El analgésico de elección es el cloruro mórfico intravenoso; se empieza con 4–8mg, con dosis adicionales de 2mg a intervalos de 5–15min hasta la desaparición del dolor1. La morfina puede producir náuseas y vómitos que, normalmente, ceden tras administrar antieméticos (metoclopramida 5–10mg intravenosa), hipotensión arterial con bradicardia, que suele responder a atropina 0,5-1mg intravenosa, hasta un total de 2mg, y depresión respiratoria. Si a pesar de la morfina el paciente continúa ansioso, considerar la administración de tratamiento ansiolítico.
Antiinflamatorios no esteroideosNo se debe administrar antiinflamatorios no esteroideos (AINE) para el tratamiento del dolor, y se debe suspender aquellos que el paciente esté tomando previamente, ya que en algunos estudios se ha observado aumento de la mortalidad, incremento del riesgo de reinfarto, hipertensión arterial, IC y rotura cardiaca, en relación con el uso de dichos fármacos1,10–14.
Tratamiento de la insuficiencia cardiacaDependerá de la gravedad del cuadro, según la clasificación Killip de IC. Los pacientes que pre sentan Killip II se benefician de oxigenoterapia, diuréticos de asa y nitratos, IECA o antagonistas de los receptores de la angiotensina II (ARA-II) en caso de contraindicación para los primeros, siempre que no presenten hipotensión arterial. Los pacientes que presentan SCACEST Killip III precisarán oxigenoterapia y, ocasionalmente, soporte ventilatorio, furosemida y nitratos si no hay hipotensión, pueden precisar agentes inotrópicos como la dopamina y la dobutamina y, en ocasiones, requieren de la colocación de catéter de Swan-Ganz. Estos pacientes precisan revascularización coronaria tan pronto como sea posible. Los pacientes que evolucionan con shock cardiogénico necesitarán oxigenoterapia y soporte ventilatorio, fármacos inotrópicos, catéter de Swan-Ganz, balón de contrapulsación intraaórtico e incluso dispositivos de asistencia mecánica y, por supuesto, revascularización coronaria urgente. Todos los pacientes deberán permanecer en todo momento monitorizados para descartar causa arrítmica de la IC.
ANTIAGREGANTES PLAQUETARIOSAspirinaSu mecanismo de acción se basa en la inhibición irreversible de la ciclooxigenasa 1 por acetilación de la enzima que, así, bloquea la síntesis de tromboxano A2. Está indicado administrarla a todo paciente con IAMCEST lo más pronto posible, salvo contraindicaciones. Se administrará dosis de carga inicial de 150–325mg vía oral de aspirina masticable y, en caso de no ser posible la ingesta oral, se optará por 250–500mg intravenosos. Posteriormente, se administrará una dosis de 75–160mg diaria de forma indefinida1,2,15,16. Sus contraindicaciones son: historia de reacción alérgica al ácido acetilsalicílico, úlcera péptica y hemorragia activa (tabla 2).
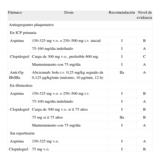
Recomendaciones terapéuticas sobre antiagregantes en la fase aguda según las guías de la Sociedad Europea de Cardiología sobre el infarto agudo de miocardio con elevación del segmento ST
| Fármaco | Dosis | Recomendación | Nivel de evidencia |
| Antiagregantes plaquetarios | |||
| En ICP primaria | |||
| Aspirina | 150-325mg v.o. o 250–500mg i.v. inicial | I | B |
| 75-160mg/día indefinido | I | A | |
| Clopidogrel | Carga de 300mg v.o., preferible 600mg. | I | C |
| Mantenimiento con 75mg/día | I | A | |
| Anti-Gp IIb/IIIa | Abciximab: bolo i.v. 0,25mg/kg seguido de 0,125μg/kg/min (máximo, 10μg/min, 12h) | IIa | A |
| En fibrinolisis | |||
| Aspirina | 150-325mg v.o. o 250–500mg i.v. | I | B |
| 75-100mg/día indefinido | I | A | |
| Clopidogrel | Carga de 300mg v.o. si ≤ 75 años | I | B |
| 75mg si ≥ 75 años | IIa | B | |
| Mantenimiento con 75mg/día | I | A | |
| Sin reperfusión | |||
| Aspirina | 150-325mg v.o. | I | A |
| Clopidogrel | 75mg v.o. | I | B |
ICP: intervención coronaria percutánea; i.v.: subcutáneo; v.o.: vía oral.
Su efecto se encuentra en la inhibición selectiva e irreversible del receptor plaquetario P2Y12 para el ADP, de esta manera impide la agregación plaquetaria. Hay tres receptores distintos para el ADP, y el clopidogrel bloquea sólo uno de ellos, por lo que la inhibición de la agregación plaquetaria que produce es incompleta. Precisa ser metabolizado por el sistema citocromo P450 hepático para adquirir actividad, por eso su inicio de acción se retrasa unos días. Sus contraindicaciones son hemorragia activa, embarazo y lactancia, o historia de hipersensibilidad al fármaco.
Actualmente, y después de la publicación de los estudios COMMIT-CCS-217 y CLARITY-TIMI 2818,19, el uso del clopidogrel está aprobado en el tratamiento del IAMCEST, tanto en los pacientes que se someten a intervención coronaria percutánea (ICP) primaria como los que reciben tratamiento de reperfusión con fibrinolítico17–20. En pacientes sometidos a ICP primaria, el clopidogrel se ha de administrar lo antes posible, con dosis de carga de al menos 300mg oral (mejor 600mg), seguido de 75mg diarios. En pacientes que reciben tratamiento fibrinolítico se recomienda dosis de carga de clopidogrel de 300mg oral, seguida de mantenimiento con 75mg al día, excepto en pacientes mayores de 75 años, en los que se recomienda iniciar directamente con 75mg, ya que no se conoce con certeza la eficacia y la seguridad de dar la dosis de carga en este grupo de edad. El COMMIT-CCS-2 también incluyó a pacientes que no se habían sometido a tratamiento de reperfusión. Tanto las guías de la Sociedad Europea de Cardiología, publicadas en 2008, como las de la ACC/AHA, de 2007, sobre el manejo del IAMCEST, recomiendan administrar 75mg diarios de clopidogrel también a los pacientes con IAMCEST sin reperfusión1,10.
Inhibidores de la glucoproteína IIb/IIIaEste tipo de inhibidores plaquetarios se unen al receptor plaquetario Gp IIb/IIIa, impiden la unión al fibrinógeno y así bloquean el paso final de la agregación plaquetaria. No tienen efecto en la adhesión plaquetaria y no bloquean los factores de la coagulación que se sitúan en las plaquetas activas y que generan trombina. Por eso, los inhibidores de la glucoproteína IIb/IIIa se administran con fármacos que inhiban la formación de trombina o su actividad.
Hay tres inhibidores de los receptores glucoproteínicos plaquetarios IIb/IIIa actualmente en el mercado: abciximab, eptifibatida y tirofibán. Han sido bien estudiados en el síndrome coronario agudo sin elevación del ST, y como coadyuvantes de los procedimientos de revascularización coronaria; sin embargo, su papel en el contexto del IAMCEST está menos establecido21.
Existen estudios angiográficos cuyo objetivo principal fue comparar las tasas de obtención de flujo TIMI 3 cuando se utilizaba terapia combinada de antagonistas de los receptores IIb/IIIa con dosis reducidas de fibrinolíticos22,23. Los resultados de estos estudios fueron favorecedores para la terapia combinada, pero los estudios clínicos posteriores no confirmaron estas expectativas. En el GUSTO-V, que comparó el tratamiento combinado fibrinolítico (mitad dosis de reteplasa) más abciximab con el tratamiento fibrinolítico aislado (dosis completa) en pacientes con infarto agudo de miocardio, se observó que el tratamiento combinado conseguía un beneficio clínico modesto (reducción de reinfartos y procedimientos de revascularización) en comparación con el fibrinolítico aislado, pero a costa de un incremento de la incidencia de hemorragias24. El ASSENT-3 aleatorizó a pacientes con IAMCEST a tres brazos de tratamiento: dosis completa de tenecteplasa con heparina no fraccionada ajustada por peso durante 48h; dosis completa de tenecteplasa con enoxaparina durante 7 días, y mitad de dosis de tenecteplasa y abciximab durante 12h. Esta última combinación no fue más eficaz que la combinación del fibrinolítico con enoxaparina, ya que produjo mayor incidencia de hemorragias25.
En el contexto de la ICP primaria también se ha tratado de explorar el beneficio potencial de los inhibidores de los receptores IIb/IIIa. La experiencia es amplia con abciximab y menor con eptifibatida y tirofibán. Diversos estudios aleatorizados observan efectos beneficiosos en la administración de abciximab intravenoso añadido a aspirina y heparina periprocedimiento26. En las guías de práctica clínica de la Sociedad Europea de Cardiología de 2008 sobre el manejo del IAMCEST, el tratamiento con abciximab intravenoso periprocedimiento en la ICP primaria resulta una recomendación IIa (nivel de evidencia A), con dosis de 0,25mg/kg en bolo, seguido de perfusión de 0,125μg/kg/min (máximo de 10μg/min, durante 12h)1.
ANTICOAGULANTESEl efecto procoagulante de la trombina se puede antagonizar bien mediante inactivación de la enzima o impidiendo su formación por las proteínas precursoras de la coagulación. Los inhibidores indirectos de la trombina, como la heparina de bajo peso molecular o la heparina no fraccionada, actúan activando la antitrombina, inhibidor de la trombina. Los inhibidores directos de la trombina actúan uniéndose directamente a la trombina e impidiendo su interacción con los sustratos (tabla 3).
Recomendaciones terapéuticas sobre anticoagulantes en la fase aguda según las guías de la Sociedad Europea de Cardiología sobre el infarto agudo de miocardio con elevación del segmento ST
| Fármaco | Dosis | Recomendación | Nivel de evidencia |
| Anticoagulantes | |||
| Con ICP primaria | |||
| Heparina | Bolo i.v. 100 U/kg (60 U/kg si se dan anti-IIb/IIIa), añadir para mantener ACT de 250–350s (200–250 si anti-IIb/IIIa). No mantener perfusión al finalizar | I | C |
| Bivalirudina | Bolo i.v. 0,75mg/kg seguido de infusión de 1,75mg/kg/h, suspender al finalizar | IIa | B |
| Fondaparinux | III | B | |
| Con fibrinolisis | |||
| Fibrinolítico selectivo | |||
| Enoxaparina | Si < 75 años y creatinina ≤ 2,5mg/ml (varones) o ≤ 2mg/ml (mujeres): bolo de 30mg seguido de 1mg/kg/12hs.c., toda la hospitalización, máximo 8 días | I | A |
| Si > 75 años no dar bolo, empezar con 0,75mg/kg/12h. Si filtrado glomerular < 30ml/min, misma dosis s.c. pero cada 24h | I | A | |
| Fibrinolítico no selectivo | |||
| Enoxaparina | Misma dosis que con fibrinolítico selectivo | IIa | B |
| Heparina | Bolo de 60 U/kg, máximo 4.000 U, seguido de perfusión 12 U/kg, máximo 1.000 U/h durante 24–48h. Conseguir TTPa 50–70s, control a las 3, 6, 12 y 24h | IIa | B |
| Fondaparinux | Bolo 2,5mg i.v. seguido de dosis de 2,5mg/24h, durante estancia hospitalaria, máximo 8 días, si creatinina ≤ 3mg/ml | IIa | B |
| Sin reperfusión | |||
| Enoxaparina | I | B | |
| Heparina | Misma dosis que para fibrinolisis | I | B |
| Fondaparinux | I | B | |
CT: tiempo de coagulación activado; ICP: intervención coronaria percutánea; i.v.: intravenoso; s.c.: subcutáneo; TTPa: tiempo de tromboplastina parcial activada.
Tanto la no fraccionada como la heparina de bajo peso molecular actúan sobre la antitrombina III, inactivando la trombina y el factor Xa, en similares proporciones en el caso de la heparina no fraccionada y con mayor efecto en el factor Xa en el caso de las heparinas de bajo peso molecular. Su efecto adverso más frecuente es la trombocitopenia inducida por heparina, más frecuente con la no fraccionada.
ICP primariaEl uso de heparina durante el intervencionismo percutáneo está estandarizado. Se administra bolo intravenoso de 100 U/kg de heparina no fraccionada (60 U/kg si se administran inhibidores de la glucoproteína IIb/IIIa concomitantemente) para mantener tiempo de coagulación activado de 250–350s (200–250s si se usan antagonistas de la glucoproteína IIb/IIIa). Posteriormente, no se continúa perfusión de heparina1.
Tratamiento fibrinolíticoEn pacientes tratados con alteplasa, tenecteplasa o reteplasa, el uso durante y luego de la fibrinolisis con heparina está estandarizado. La heparina no parece mejorar la permeabilidad coronaria en los pacientes tratados con fibrinolíticos no selectivos, como la estreptoquinasa. El estudio EXTRACTTIMI 25 evalúa la enoxaparina frente a la heparina no fraccionada en pacientes que reciben terapia fibrinolítica administrando dosis de enoxaparina ajustada por edad y función renal. Se observó reducción del riesgo de reinfarto y muerte a los 30 días con enoxaparina, pero con mayor incidencia de hemorragia no cerebral27. Las guías de la Sociedad Europea de Cardiología aconsejan, pues, con recomendación IA, en pacientes que reciben fibrinolíticos específicos, administrar enoxaparina a dosis de 30mg intravenosa inicial seguido, 15min después, de 1mg/kg subcutánea cada 12h durante toda la estancia hospitalaria, máximo de 8 días. En pacientes mayores de 75 años no se administra el bolo inicial y la dosis subcutánea es de 0,75mg/kg cada 12h. Si el filtrado glomerular es < 30ml/min, se administra la dosis subcutánea correspondiente, pero sólo 1 vez al día. Si no se dispone de enoxaparina, se administrará heparina no fraccionada a dosis de 60 U/kg intravenosa en bolo, máximo de 4.000 U, seguido de infusión de 12 U/kg, máximo de 1.000 U/h, durante 24–48h, con control del tiempo de tromboplastina parcial activada (50–70s) a las 3, 6, 12 y 24h. En pacientes que reciben tratamiento fibrinolítico con estreptoquinasa, la administración de enoxaparina y heparina no fraccionada, a mismas concentraciones que las anteriores, resulta indicación IIa (nivel de evidencia B para la enoxaparina y C para la no fraccionada)1.
Sin terapia de reperfusiónPueden usarse indistintamente ambas heparinas, a las mismas dosis que las utilizadas en el contexto de reperfusión con agentes fibrinolíticos.
BivalirudinaSu efecto se debe a la inhibición directa de la trombina circulante y la ligada a la fibrina.
En el HORIZONS-AMI28, realizado en pacientes sometidos a ICP primaria, la bivalirudina se asoció a menor riesgo de hemorragia y disminución de la mortalidad por cualquier causa, pero se asoció con mayor número de trombosis agudas del stent. Su administración en el contexto de ICP primaria se puede realizar mediante un bolo de 0,75mg/kg intravenoso, seguido de perfusión de 1,75mg/kg/h, normalmente suspendiéndola al final del procedimiento.
No está recomendada en pacientes sometidos a tratamiento fibrinolítico ni en aquellos que no han recibido terapia de reperfusión, aunque podría ser una alternativa a la heparina en aquellos que presentan el antecedente de trombocitopenia inducida por la heparina.
FondaparinuxEs un pentasacárido sintético que se une a la antitrombina III, e induce un incremento de la actividad anti-Xa, lo que resulta en una inhibición dependiente de la dosis del factor Xa.
En el IAMCEST, se puede administrar a los pacientes sometidos a reperfusión con estreptoquinasa o no reperfundidos, a los que no se administra heparina. En caso de precisar coronariografía o ICP, se tendrá que administrar bolo de 5.000 U de heparina intravenosa para evitar la trombosis del catéter29. Las dosis habituales de fondaparinux son 2,5mg intravenoso en bolo, seguido de 2,5mg subcutáneo una vez al día, durante 8 días si la creatinina es < 3mg/ml1.
TRATAMIENTO FARMACOLÓGICO GENERALBloqueadores betaTodos los pacientes deberían recibir tratamiento oral con bloqueadores beta si no presentan contraindicaciones. El uso de los bloqueadores beta intravenosos no está establecido30. Parece razonable administrarlos en las primeras 24h a los pacientes con hipertensión arterial y que no presenten signos de IC, evidencia de bajo gasto cardiaco, riesgo de shock cardiogénico o contraindicaciones para el bloqueador beta1 (tabla 4).
Recomendaciones terapéuticas sobre otros fármacos en la fase aguda según las guías de la Sociedad Europea de Cardiología sobre el infarto agudo de miocardio con elevación del segmento ST
| Fármaco | Recomendación | Nivel de evidencia |
| Bloqueadores beta orales | I | A |
| Bloqueadores beta i.v. | IIb | A |
| IECA | ||
| En pacientes de riesgo | I | A |
| En todos los pacientes | IIa | A |
| ARA-II si hay intolerancia a IECA | I | B |
| Eplerenona si FE ≤ 40% y signos de IC o DM, si Cr < 2,5mg/dl (varones) y < 2mg/dl (mujeres), con K < 5mmol/l | I | B |
| Antagonistas del calcio | III | B |
| Nitratos | IIb | A |
| AINE e inhibidores de la COX-2 | III | C |
| Lidocaína | III | B |
| Magnesio | III | A |
AINE: antiinflamatorios no esteroideos; ARA-II: antagonistas de la angiotensina II; COX-2: ciclooxigenasa-2; Cr: creatinina; DM: diabetes mellitus; FE: fracción de eyección; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de angiotensina; i.v.: intravenoso.
Todos los pacientes sin contraindicaciones deberán recibir tratamiento betabloqueante indefinidamente1,10.
Antagonistas del calcioNo se deben administrar en la fase aguda del infarto de forma profiláctica. En caso de necesidad por contraindicación de los bloqueadores beta y necesidad de controlar la angina o la frecuencia cardiaca, podrán administrarse siempre que no haya disfunción ventricular, signos de IC o bloqueo auriculoventricular1,2.
Inhibidores de la enzima de conversión de angiotensinaSe debe administrar IECA en las primeras 24h a los pacientes con infarto anterior extenso, fracción de eyección ventricular ≤ 40% o aquellos que han presentado clínica de IC durante la fase aguda del infarto, en ausencia de hipotensión u otras contraindicaciones9. La administración sistemática de estos fármacos a todos los pacientes que presenten un SCACEST y sin las características anteriores resulta indicación IIa, tanto en las guías de práctica clínica de la Sociedad Europea de Cardiología como las de la American Heart Association1,2.
En caso de intolerancia a IECA se puede considerar los ARA-II.
EplerenonaFármaco antagonista selectivo del receptor de la aldosterona. Está indicada su asociación con los IECA en pacientes con IAMCEST con disfunción ventricular e insuficiencia cardiaca o diabetes mellitus31.
Fármacos antiarrítmicosNo está justificado su uso sistemático.
Los pacientes que presenten arritmias malignas en la fase aguda del infarto deberán recibir cardioversión eléctrica y si a pesar de ello continúan con episodios, se iniciará fármacos como amiodarona intravenosa o lidocaína, juntamente con bloqueadores beta1.
El manejo de la fibrilación auricular será el habitual de control de ritmo (con amiodarona) y de la frecuencia cardiaca (con bloqueadores beta o antagonistas del calcio no dihidropiridínicos si hay contraindicación de los primeros), con especial cuidado de no administrar fármacos antiarrítmicos del grupo IC. En caso de inestabilidad hemodinámica, se optará por cardioversión eléctrica. Se decidirá anticoagulación según los criterios habituales1.
MagnesioNo está indicada su administración de forma sistemática.
EstatinasSu administración en un IAMCEST está indicada de forma aguda, dentro de las primeras 24h si es posible y a altas dosis32.
CONCLUSIONESEl manejo del paciente con IAMCEST en la fase aguda debe basarse en una terapia de reperfusión precoz acompañada de medidas generales de monitorización cardiaca y control del dolor, y la administración de fármacos anticoagulantes y antiagregantes, bloqueadores beta, IECA, en casos seleccionados, y estatinas. Con todas estas medidas terapéuticas se ha obtenido un descenso importante en la mortalidad del IAMCEST en las últimas décadas.