La insuficiencia tricuspídea (IT) ha recibido escasa atención de clínicos e investigadores, y en España pocos centros han publicado su experiencia con ella1. Nuestro grupo comunicó en 2013 sus resultados tras el tratamiento quirúrgico de la IT grave en una serie de 119 pacientes consecutivos intervenidos desde abril de 1996 hasta febrero de 2010, y se observó una mortalidad perioperatoria y a largo plazo elevada2. Dicha serie hoy se debe considerar histórica, y los resultados mostrados entonces no pueden servir de orientación para estimar los obtenidos recientemente tras el tratamiento quirúrgico de la IT. Así, el objetivo del presente trabajo es analizar los resultados clínicos y ecocardiográficos de una muestra reciente de pacientes con IT grave que recibieron tratamiento quirúrgico.
Para ello, se diseñó un estudio retrospectivo en el que se incluyó a 87 pacientes consecutivos con IT grave sometidos en nuestro centro a cirugía tricuspídea entre marzo de 2010 y diciembre de 2013. La indicación de cirugía tricuspídea se estableció por la presencia de una lesión tricúspide sintomática y grave según la definición ecocardiográfica descrita en nuestro trabajo previo2. El tratamiento se decidió mediante consenso entre cardiólogos, cirujanos cardiacos y el paciente. Se optó por la reparación siempre que la técnica fuera factible, fundamentalmente por la ausencia de daño orgánico significativo. Como excepción, se pudo optar por la sustitución valvular, según el criterio del cirujano, en los casos con daño funcional y cirugía cardiaca previa. Se analizó la morbimortalidad perioperatoria y a largo plazo, así como la aparición de nueva IT grave, y se estudiaron sus predictores.
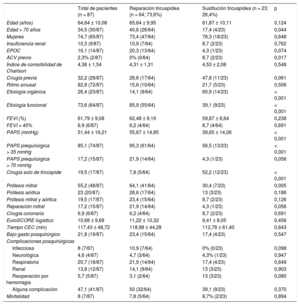
En el periodo analizado, se practicó anuloplastia sin anillo según la técnica de De Vega a 4 pacientes y anuloplastia con anillo a 60; 23 pacientes recibieron prótesis biológica y ninguno, prótesis mecánica. La tabla resume las características basales, las complicaciones tras la cirugía y la mortalidad perioperatoria. El 74,7% de los pacientes eran mujeres (media de edad, 64,64 ± 10,08 años). La etiología fue orgánica en el 60,9% de las sustituciones tricuspídeas, y funcional en el 85,9% de las reparaciones. En el grupo de las reparaciones se observaron edades mayores (> 70 años, el 40,6 frente al 17,4%; p = 0,044), mayores presiones pulmonares preoperatorias (presión sistólica de la arteria pulmonar, 55,67 ± 14,85 frente a 39,65 ± 14,06 mmHg; p < 0,001) y menor proporción de cirugía solo de tricúspide (el 7,8 frente al 52,2%; p < 0,001). El 47,1% de la muestra tuvo alguna complicación durante el posoperatorio, y la mortalidad perioperatoria fue del 8%.
Características basales y quirúrgicas de las muestras, complicaciones quirúrgicas y mortalidad perioperatoria
| Total de pacientes (n = 87) | Reparación tricuspídea (n = 64; 73,6%) | Sustitución tricuspídea (n = 23; 26,4%) | p | |
|---|---|---|---|---|
| Edad (años) | 64,64 ± 10,08 | 65,64 ± 9,95 | 61,87 ± 10,11 | 0,124 |
| Edad > 70 años | 34,5 (30/87) | 40,6 (26/64) | 17,4 (4/23) | 0,044 |
| Mujeres | 74,7 (65/87) | 73,4 (47/64) | 78,3 (18/23) | 0,648 |
| Insuficiencia renal | 10,3 (9/87) | 10,9 (7/64) | 8,7 (2/23) | 0,762 |
| EPOC | 16,1 (14/87) | 20,3 (13/64) | 4,3 (1/23) | 0,074 |
| ACV previo | 2,3% (2/87) | 0% (0/64) | 8,7 (2/23) | 0,017 |
| Índice de comorbilidad de Charlson | 4,36 ± 1,54 | 4,31 ± 1,31 | 4,53 ± 2,08 | 0,548 |
| Cirugía previa | 32,2 (28/87) | 26,6 (17/64) | 47,8 (11/23) | 0,061 |
| Ritmo sinusal | 82,8 (72/87) | 15,6 (10/64) | 21,7 (5/23) | 0,506 |
| Etiología orgánica | 26,4 (23/87) | 14,1 (9/64) | 60,9 (14/23) | < 0,001 |
| Etiología funcional | 73,6 (64/87) | 85,9 (55/64) | 39,1 (9/23) | < 0,001 |
| FEVI (%) | 61,79 ± 9,08 | 62,48 ± 9,19 | 59,87 ± 8,64 | 0,238 |
| FEVI < 45% | 6,9 (6/87) | 6,2 (4/64) | 8,7 (4/64) | 0,691 |
| PAPS (mmHg) | 51,44 ± 16,21 | 55,67 ± 14,85 | 39,65 ± 14,06 | < 0,001 |
| PAPS prequirúrgica > 35 mmHg | 85,1 (74/87) | 95,3 (61/64) | 56,5 (13/23) | < 0,001 |
| PAPS prequirúrgica > 70 mmHg | 17,2 (15/87) | 21,9 (14/64) | 4,3 (1/23) | 0,056 |
| Cirugía solo de tricúspide | 19,5 (17/87) | 7,8 (5/64) | 52,2 (12/23) | < 0,001 |
| Prótesis mitral | 55,2 (48/87) | 64,1 (41/64) | 30,4 (7/23) | 0,005 |
| Prótesis aórtica | 23 (20/87) | 26,6 (17/64) | 13 (3/23) | 0,186 |
| Prótesis mitral y aórtica | 19,5 (17/87) | 23,4 (15/64) | 8,7 (2/23) | 0,126 |
| Reparación mitral | 17,2 (15/87) | 21,9 (14/64) | 4,3 (1/23) | 0,056 |
| Cirugía coronaria | 6,9 (6/87) | 6,2 (4/64) | 8,7 (2/23) | 0,691 |
| EuroSCORE logístico | 10,68 ± 9,68 | 11,22 ± 10,32 | 9,41 ± 8,05 | 0,456 |
| Tiempo CEC (min) | 117,43 ± 48,72 | 118,98 ± 44,28 | 112,78 ± 61,40 | 0,643 |
| Bajo gasto posquirúrgico | 21,8 (19/87) | 23,4 (15/64) | 17,4 (4/23) | 0,547 |
| Complicaciones posquirúrgicas | ||||
| Infecciosa | 8 (7/87) | 10,9 (7/64) | 0% (0/23) | 0,098 |
| Neurológica | 4,6 (4/87) | 4,7 (3/64) | 4,3% (1/23) | 0,947 |
| Respiratoria | 20,7 (18/87) | 21,9 (14/64) | 17,4 (4/23) | 0,649 |
| Renal | 13,8 (12/87) | 14,1 (9/64) | 13 (3/23) | 0,903 |
| Reoperación por hemorragia | 5,7 (5/87) | 3,1 (2/64) | 13 (3/23) | 0,080 |
| Alguna complicación | 47,1 (41/87) | 50 (32/64) | 39,1 (9/23) | 0,370 |
| Mortalidad | 8 (7/87) | 7,8 (5/64) | 8,7% (2/23) | 0,894 |
ACV: accidente cerebrovascular; CEC: circulación extracorpórea; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; PAPS: presión arterial pulmonar sistólica.
Los valores expresan % (n/N) o media ± desviación estándar.
Para identificar los predictores de la mortalidad perioperatoria, se realizó un análisis mulitivariable en el que se incluyeron tanto la fracción de eyección del ventrículo izquierdo < 45%, única variable que se asoció de manera significativa con dicho evento en el análisis univariable (tabla del material suplementario), como las variables identificadas como predictoras en nuestro trabajo previo (edad y tiempo de circulación extracorpórea)2. El único factor predictor de mortalidad perioperatoria fue la fracción de eyección del ventrículo izquierdo < 45% (odds ratio = 10,531; intervalo de confianza del 95% [IC95%], 1,262-87,905; p = 0,030).
Tras el alta domiciliaria después de la cirugía, se evaluó la evolución de la IT de 66 de los 80 supervivientes (82,5%) en el seguimiento ecocardiográfico (mediana, 30 [intervalo intercuartílico, 20-44] meses). Sufrieron IT grave 4 pacientes, todos pertenecientes al grupo de anuloplastia sin anillo (el 7,1% de los pacientes con seguimiento en este grupo). No se evaluaron los predictores de la aparición de IT grave en el seguimiento, dada su baja incidencia.
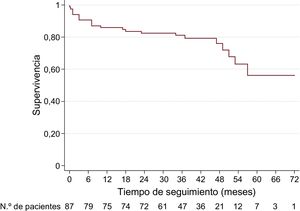
Se evaluó la mortalidad tras un seguimiento que incluyó al 100% de los supervivientes al perioperatorio (mediana, 38 [30,25-48] meses).
La mortalidad durante el seguimiento total fue del 18,8% de los pacientes vivos al alta hospitalaria, y la mortalidad total (perioperatoria y durante el seguimiento total) fue del 25,3%. Se realizó un análisis univariable de la mortalidad total (tabla del material suplementario) y se incluyeron en el análisis multivariable las variables con asociación estadísticamente significativa. El único predictor de la mortalidad total fue el tiempo de circulación extracorpórea (hazard ratio = 1,012; IC95%, 1,003-1,021; p = 0,009). La figura muestra la curva de supervivencia en el seguimiento de la cohorte de pacientes objeto de estudio.
En el presente trabajo se observa una mortalidad perioperatoria del 8%, comparable a la mostrada en otras series extensas de nuestro medio3, pero sensiblemente inferior al 18,5% que se obtuvo en nuestro estudio previo2. Las causas que explican la mejora en la mortalidad perioperatoria en nuestro centro no pueden inferirse de este estudio por su diseño. Como hipótesis, se postula que la indicación del tratamiento quirúrgico se ha realizado progresivamente en estadios clínicos más precoces, de acuerdo con los estudios que mostraron mayor mortalidad de pacientes con síntomas avanzados en el momento de la cirugía4. Además de esto, la experiencia quirúrgica y anestésica adquirida con el tiempo probablemente haya influido positivamente en los resultados obtenidos. Es previsible que estos resultados se mejoren aplicando a los pacientes con mayor riesgo las diversas técnicas percutáneas ya desarrolladas para el tratamiento de la IT grave, las cuales presentan baja morbimortalidad periprocedimiento5.
En nuestro trabajo, el tiempo de circulación extracorpórea se mostró como predictor de la mortalidad total, como en nuestra serie previa2. Se consideró que un tiempo de circulación extracorpórea largo refleja una mayor comorbilidad valvular, lo que respalda su valor pronóstico en el seguimiento.
Además de la imposibilidad para identificar los determinantes de la mejora en los resultados clínicos, otras limitaciones de este trabajo derivan de su carácter retrospectivo y unicéntrico y de la ausencia de datos con valor pronóstico como el volumen y la función ventricular derecha.
En conclusión, en nuestra serie de pacientes con IT grave tratados quirúrgicamente, se observaron unos resultados clínicos a corto y largo plazo que no se relacionan con los hallazgos subóptimos de nuestra serie previa. Se identificó como predictor de mortalidad perioperatoria la fracción de eyección del ventrículo izquierdo < 45%, y como predictor de mortalidad a largo plazo, el tiempo de circulación extracorpórea.