Avances recientes han asociado el aumento del estrés oxidativo con la disminución directa de la función del miocardio1. El ácido úrico (AU) es un marcador indirecto de estrés oxidativo, y se ha demostrado que el aumento de sus concentraciones séricas tiene valor predictivo de eventos adversos en pacientes con insuficiencia cardiaca (IC) y que se asocian con una peor situación hemodinámica2,3. En este sentido, algunos autores han demostrado que en pacientes con lC y AU elevado, el tratamiento de la hiperuricemia produce beneficios clínicos que se correlacionan con el grado de reducción del AU4. Sin embargo, faltan estudios que confirmen la asociación entre concentraciones séricas de AU y peor pronóstico en pacientes con IC aguda.
Nosotros evaluamos de forma retrospectiva el papel pronóstico, a corto y largo plazo, de los valores séricos de AU en pacientes mayores de 50 años que ingresaron en nuestro servicio de medicina interna por IC aguda descompensada, tanto de novo como crónica agudizada (según los criterios de la Sociedad Europea de Cardiología). De todos ellos, se registraron los datos demográficos, los antecedentes cardiovasculares, la capacidad funcional para las actividades básicas de la vida diaria a través del índice de Barthel, la comorbilidad a través del índice de Charlson y la clase funcional de la New York Heart Association, mediante los sistemas institucionales de información y de historia clínica electrónica. Se recogieron a su vez los valores clínicos y analíticos, los tratamientos y la ecocardiografía al ingreso, y se evaluó la mortalidad durante el ingreso índice y al final de un periodo de seguimiento de 12 meses. Posteriormente, se comparó a los pacientes con IC aguda e hiperuricemia al ingreso con los que presentaron cifras de AU normales, y se excluyó a los pacientes con enfermedad terminal en tratamiento paliativo. La medición de AU se realizó en las primeras 48 h de la asistencia en urgencias; se consideró hiperuricemia una concentración plasmática>8 mg/dl en varones y>7mg/dl en mujeres. Se utilizó la media±desviación estándar para las variables cuantitativas y el porcentaje para las variables categóricas. La comparación de las características de ambos grupos (hiperuricemia frente a normouricemia) se realizó mediante las pruebas de la χ2 y de la t de Student. Se utilizó un análisis de regresión logística y un análisis multivariable de riesgos proporcionales de regresión de Cox para evaluar la mortalidad intrahospitalaria y al año de seguimiento. El nivel de significación estadística se estableció en p<0,05.
Se evaluó a un total de 244 pacientes consecutivos ingresados por IC aguda, 128 mujeres (52,5%) y 116 varones, con una media de edad de 75±10 años y una comorbilidad media moderada (2,6 del índice de Charlson). Del total, 144 (59%) mostraron fracción de eyección del ventrículo izquierdo preservada (> 50%); usaban diuréticos 203 pacientes (83,1%) e inhibidores de la enzima de conversión de la angiotensina y antagonistas del receptor de la angiotensina II, 180 (73,7%). En una importante mayoría —167 (68,4%) de los 244 pacientes— se documentó hiperuricemia al ingreso, mujeres en mayor proporción, con mayor grado de dependencia funcional y mayores concentraciones séricas de creatinina que los pacientes con IC aguda y normouricemia. Los pacientes normouricémicos mostraron mayor tendencia a diabetes mellitus y obesidad (tabla).
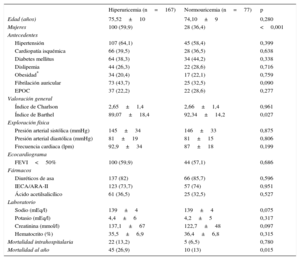
Características clínicas y analíticas de los pacientes con insuficiencia cardiaca aguda con y sin hiperuricemia
| Hiperuricemia (n=167) | Normouricemia (n=77) | p | |
|---|---|---|---|
| Edad (años) | 75,52±10 | 74,10±9 | 0,280 |
| Mujeres | 100 (59,9) | 28 (36,4) | <0,001 |
| Antecedentes | |||
| Hipertensión | 107 (64,1) | 45 (58,4) | 0,399 |
| Cardiopatía isquémica | 66 (39,5) | 28 (36,5) | 0,638 |
| Diabetes mellitus | 64 (38,3) | 34 (44,2) | 0,338 |
| Dislipemia | 44 (26,3) | 22 (28,6) | 0,716 |
| Obesidad* | 34 (20,4) | 17 (22,1) | 0,759 |
| Fibrilación auricular | 73 (43,7) | 25 (32,5) | 0,090 |
| EPOC | 37 (22,2) | 22 (28,6) | 0,277 |
| Valoración general | |||
| Índice de Charlson | 2,65±1,4 | 2,66±1,4 | 0,961 |
| Índice de Barthel | 89,07±18,4 | 92,34±14,2 | 0,027 |
| Exploración física | |||
| Presión arterial sistólica (mmHg) | 145±34 | 146±33 | 0,875 |
| Presión arterial diastólica (mmHg) | 81±19 | 81±15 | 0,806 |
| Frecuencia cardiaca (lpm) | 92,9±34 | 87±18 | 0,199 |
| Ecocardiograma | |||
| FEVI<50% | 100 (59,9) | 44 (57,1) | 0,686 |
| Fármacos | |||
| Diuréticos de asa | 137 (82) | 66 (85,7) | 0,596 |
| IECA/ARA-II | 123 (73,7) | 57 (74) | 0,951 |
| Ácido acetilsalicílico | 61 (36,5) | 25 (32,5) | 0,527 |
| Laboratorio | |||
| Sodio (mEq/l) | 139±4 | 139±4 | 0,075 |
| Potasio (mEq/l) | 4,4±6 | 4,2±5 | 0,317 |
| Creatinina (mmol/l) | 137,1±67 | 122,7±48 | 0,097 |
| Hematocrito (%) | 35,5±6,9 | 36,4±6,8 | 0,315 |
| Mortalidad intrahospitalaria | 22 (13,2) | 5 (6,5) | 0,780 |
| Mortalidad al año | 45 (26,9) | 10 (13) | 0,015 |
ARA-II: antagonistas del receptor de la angiotensina II; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los valores expresan n (%) o media±desviación estándar.
Durante el ingreso índice fallecieron 27 pacientes (11,1%) y durante el año de seguimiento, 28 pacientes, con una tasa de mortalidad acumulada a los 12 meses del 22,4%. La mortalidad durante el ingreso índice no mostró diferencias entre los grupos de pacientes con IC aguda con y sin hiperuricemia (el 13,2 frente al 6,5%; p=0,780); sin embargo, la mortalidad al año de seguimiento resultó significativamente más alta entre los pacientes con IC aguda e hiperuricemia (el 26,9 frente al 13,0%; p=0,015). Tras el análisis de regresión de Cox, los valores de AU altos mantuvieron su asociación con la mortalidad al año (hazard ratio [HR]=1,091; intervalo de confianza del 95% [IC95%], 1,018-1,169), junto con un efecto protector de un mejor índice de Barthel al ingreso (HR=0,979; IC95%, 0,969-0,989).
La hiperuricemia, por lo tanto, es un hallazgo frecuente en nuestros pacientes que requieren ingreso hospitalario por IC aguda, aunque probablemente su explicación sea multifactorial, ya sea debido al tratamiento diurético recibido, su frecuente asociación con la disfunción renal o la sobrexpresión de la xantina oxidasa mediada por el estado proinflamatorio4,5. En línea con los escasos estudios disponibles, nuestros resultados evidencian mayor riesgo de muerte a largo plazo para los pacientes ingresados por IC aguda con hiperuricemia, aunque no el de muerte hospitalaria durante el ingreso índice. Sin embargo, actualmente no hay consenso sobre si la hiperuricemia ejerce un papel patogénico miocárdico directo o se comporta como un simple marcador de gravedad subrogado.
Un interrogante que considerar es si la sola reducción del AU podría ser beneficiosa en pacientes con IC. Son necesarios trabajos que evalúen el efecto del tratamiento de la hiperuricemia en dichos pacientes6.