Full English text available from: www.revespcardiol.org/en
La neprilisina ha pasado a ser uno de los centros de interés en cardiología, debido a los impresionantes beneficios que se han demostrado con la combinación de una inhibición de la neprilisina y un antagonismo de los receptores de la angiotensina en el reciente ensayo clínico PARADIGM-HF, en el que se evaluó el empleo de LCZ696 (denominado ahora sacubitrilo/valsartán y comercializado por Novartis con el nombre de Entresto) en el tratamiento de la insuficiencia cardiaca sistólica con fracción de eyección reducida (ICFEr)1. Sin embargo, la neprilisina EC 3.4.24.11 (también denominada endopeptidasa neutra, endoproteasa 24.11, NEP, antígeno de leucemia linfoblástica aguda común [CALLA], antígeno de diferenciación de grupos de antígenos de neutrófilos 10 [CD10], metaloendopeptidasa de membrana EC 3.4.24.11 y encefalinasa) es una enzima muy versátil, que ha vuelto al primer plano después de una azarosa carrera de más de 40 años2.
En el sistema cardiovascular, la neprilisina fragmenta numerosos péptidos vasoactivos. Algunos de estos péptidos tienen efectos vasodilatadores (incluidos los péptidos natriuréticos, la adrenomedulina y la bradicinina), y otros ejercen efectos vasoconstrictores (angiotensina I y II y endotelina–1, entre otros). No obstante, la neprilisina muestra diversas afinidades relativas a diferentes sustratos; la máxima afinidad es la que tiene por el péptido natriurético auricular, el péptido natriurético de tipo C y las angiotensinas I y II, y su mínima afinidad, por el péptido natriurético tipo B (BNP), la endotelina–1 y la bradicinina3.
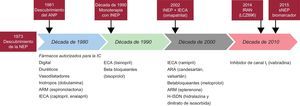
Durante décadas la neprilisina ha sido una diana biológica importante. El ámbito académico y la industria han llevado a cabo intensos esfuerzos combinados para buscar inhibidores de la neprilisina (INEP) que pudieran ser de utilidad en la práctica clínica. Inicialmente, a finales de la década de los ochenta y comienzos de los noventa, se evaluó el uso de INEP en monoterapia. El candoxatrilo mostró unos efectos preliminares prometedores sobre los parámetros hemodinámicos. Sin embargo, otro INEP, el ecadotrilo, conllevó un aumento de la mortalidad, sin que hubiera indicio alguno de eficacia clínica en comparación con placebo en los pacientes con insuficiencia cardiaca4,5. Por consiguiente, se abandonó el desarrollo de los INEP en monoterapia para la insuficiencia cardiaca. Posteriormente, algunos estudios mostraron evidencia que indicaba una activación concurrente del sistema renina-angiotensina-aldosterona, junto con potenciación de la bioactividad de los péptidos natriuréticos. Estas observaciones inspiraron el desarrollo y las pruebas de otros productos que combinan actividad de INEP e inhibidora de la enzima de conversión de la angiotensina (IECA), y ello condujo a los fármacos conocidos como inhibidores de vasopeptidasa. Se han desarrollado varios inhibidores de vasopeptidasa, como el omapatrilat, el fasidotrilo, el sampatrilat y el mixanprilo. Después de numerosos estudios, hubo en este campo un gran desánimo cuando se observó que el omapatrilat causaba un exceso de episodios de angiedema clínicamente relevante6. Después de más de una década de errar por el desierto, se desarrolló un nuevo concepto, la combinación de INEP y antagonistas del receptor de la angiotensina II (ARA–II), lo que condujo a una nueva clase de fármacos denominados inhibidores de los receptores de angiotensina y neprilisina (IRAN). El sacubitrilo/valsartán, un IRAN, es el primero de esta clase terapéutica, y ha mostrado unos resultados mejores que lo esperado en el ensayo PARADIGM–HF1 (figura).
Esquema de los hitos históricos en el desarrollo de la neprilisina. ANP: péptido natriurético auricular; ARA–II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralcorticoides; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; INEP: inhibidor de neprilisina; IRAN: inhibidores de los receptores de angiotensina y neprilisina; NEP: neprilisina; sNEP: neprilisina soluble.
El ensayo PARADIGM-HF es un estudio multinacional, aleatorizado y a doble ciego en el que participaron 8.442 pacientes. El objetivo era comparar sacubitrilo/valsartán con enalapril en pacientes adultos con insuficiencia cardiaca crónica (clase funcional de la New York Heart Association [NYHA] II-IV) y fracción de eyección del ventrículo izquierdo (FEVI) reducida (≤ 40%, que más tarde se modificó para utilizar el criterio de FEVIS ≤ 35%), añadidos a otros tratamientos para la insuficiencia cardiaca1. El objetivo principal era la combinación de los eventos muerte de causa cardiovascular u hospitalización por insuficiencia cardiaca. Antes de la participación en el estudio, se trató a los pacientes con el tratamiento estándar, que incluía IECA/ARA–II (> 99%), bloqueadores beta (94%), antagonistas del receptor mineralocorticoideo (58%) y diuréticos (82%). La mediana de seguimiento fue de 27 meses y los pacientes estuvieron en tratamiento durante un periodo de hasta 4,3 años.
Los pacientes debían interrumpir el tratamiento con IECA o ARA–II que estuvieran recibiendo e incorporarse a un periodo de preinclusión secuencial en un diseño con enmascaramiento simple. Durante el periodo de preinclusión, se les administró enalapril en dosis de 10 mg 2 veces al día, seguido de un tratamiento en diseño con enmascaramiento simple con sacubitrilo/valsartán a dosis de 100 mg 2 veces al día, que se aumentó a 200 mg 2 veces al día. A continuación se incorporaron al periodo doble ciego del estudio tras una aleatorización. Durante ese periodo, se trató a los pacientes con sacubitrilo/valsartán en dosis de 200 mg o enalapril en dosis de 10 mg 2 veces al día. La media de edad de la población estudiada era 64 años y un 19% tenía una edad ≥ 75 años. En el momento de la aleatorización, un 70% de los pacientes se encontraban en NYHA II, un 24% estaba en NYHA III y el 0,7%, en NYHA IV. La media de FEVI era del 29% y había 963 pacientes (11,4%) con FEVI basal > 35%≤ 40%. El estudio se interrumpió prematuramente como consecuencia de las abrumadoras reducciones de las muertes por causas cardiovasculares y del objetivo principal combinado (muerte de causa cardiovascular u hospitalización secundaria a insuficiencia cardiaca). Al ensayo PARADIGM-HF, se lo conoce también como el ensayo del 20% debido a las reducciones relativas homogéneas de ∼20% en todos los parámetros de valoración evaluados, incluido el objetivo principal combinado de muerte de causa cardiovascular, muerte súbita cardiaca y hospitalización por insuficiencia cardiaca (tabla 1).
Ensayo PARADIGM-HF: efectos del tratamiento en el objetivo principal combinado, sus componentes individuales y la mortalidad por cualquier causa tras una mediana de seguimiento de 27 meses
| Objetivos | HR (IC95%) | RRR, % | p |
|---|---|---|---|
| Objetivo principal combinado (muerte CV y hospitalización por IC) | 0,80 (0,73-0,87) | 20 | 0,0000002 |
| Componentes individuales del objetivo principal combinado | |||
| Muerte CV | 0,80 (0,71-0,89) | 20 | 0,00004 |
| Primera hospitalización por IC | 0,79 (0,71-0,89) | 21 | 0,00004 |
| Objetivo secundario | |||
| Mortalidad por cualquier causa | 0,84 (0,76-0,93) | 16 | 0,0005 |
HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; CV: cardiovascular; RRR: reducción riesgo relativo.
Aunque el sacubitrilo/valsartán ha presentado unos resultados enormemente prometedores, hay retos y cuestiones pendientes de abordar que requerirán nuevos estudios (tabla 2). Algunas de estas cuestiones se comentan en el informe de evaluación de la Agencia Europea del Medicamento sobre Entresto7.
Resumen de las preocupaciones existentes respecto a la seguridad de sacubitrilo/valsartán
| Riesgos importantes identificados | Hipotensión Disfunción renal Hiperpotasemia Edema angioneurótico |
| Riesgos posibles importantes | Hepatotoxicidad Deterioro cognitivo Interacción farmacológica con estatinas Trombocitopenia Neutropenia |
| Información no disponible | Pacientes pediátricos con IC Pacientes con deterioro grave de la función renal Datos a largo plazo sobre el uso del sacubitrilo/valsartán en la IC Efectos en pacientes con IC que no han recibido nunca IECA/ARA–II |
ARA–II: antagonistas del receptor de la angiotensina II; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina.
Modificado del Informe de Evaluación de la Agencia Europea del Medicamento7.
En primer lugar, para los pacientes con problemas de tolerancia (p. ej., presión arterial sistólica [PAS] ≤ 95mmHg, hipotensión sintomática, hiperpotasemia, disfunción renal), las recomendaciones actuales se decantan por realizar un ajuste de los fármacos concomitantes o ajustar a la baja o suspender temporalmente la administración de sacubitrilo/valsartán. De hecho, la Agencia Europea del Medicamento recomienda que no inicien el tratamiento los pacientes con valores de potasio en suero > 5,4 mmol/l o PAS < 100mmHg.
En segundo lugar, los datos relativos a los pacientes que ya están con dosis bajas o no reciben tratamiento con IECA o ARA–II son escasos. En consecuencia, las recomendaciones actuales para estos pacientes consisten en iniciar el tratamiento con una dosis de 50 mg 2 veces al día y ajustarla luego lentamente (aumentando al doble cada 3–4 semanas).
En tercer lugar, el sacubitrilo/valsartán nunca debe administrarse conjuntamente con un IECA/ARA–II. Cuando se emplea simultáneamente con un IECA, hay riesgo de angiedema. Por consiguiente, no debe iniciarse un tratamiento con sacubitrilo/valsartán antes de que hayan transcurrido como mínimo 36 h desde la interrupción del tratamiento con un IECA.
En cuarto lugar, no es necesario ajuste alguno de la dosis para los pacientes con disfunción renal leve (filtrado glomerular estimado, 60–90ml/min/1,73 m2). Sin embargo, se debe considerar la posibilidad de iniciar el tratamiento con dosis de 50 mg 2 veces al día para los pacientes con disfunción renal moderada (filtrado glomerular estimado, 30–60ml/min/1,73 m2). No hay datos de pacientes con enfermedad renal terminal, pero no se recomienda el uso de sacubitrilo/valsartán en estos casos.
En quinto lugar, debe tenerse precaución al iniciar tratamiento con sacubitrilo/valsartán para pacientes en NYHA IV, dado que la experiencia clínica existente con esa población es escasa.
En sexto lugar, el péptido natriurético cerebral deja de ser válido como biomarcador de la insuficiencia cardiaca en los pacientes tratados con sacubitrilo/valsartán, ya que el aquel es un sustrato de la neprilisina. Se recomienda su sustitución por el NT-proBNP como péptido natriurético biomarcador.
En séptimo lugar, hay un riesgo teórico asociado a la inhibición de la neprilisina relacionado con la acumulación del sustrato de la neprilisina, el amiloide β, en el cerebro8. En el ensayo PARADIGM-HF no se observó aumento de la incidencia de eventos adversos relacionados con la capacidad cognitiva o con demencia. Sin embargo, existe la posibilidad de que estos efectos no se hayan detectado hasta la fecha, ya que la demencia puede tardar en aparecer más tiempo que el actual periodo de observación de los participantes del ensayo. Además, no participaron en el estudio los pacientes con demencia leve. Sin embargo, en el estudio de fase III actualmente en curso, PARAGON-HF, se ha introducido una evaluación de la función cognitiva.
En octavo lugar, la administración conjunta de sacubitrilo/valsartán y atorvastatina aumentó la concentración máxima de atorvastatina y sus metabolitos en hasta 2 veces. En el ensayo PARADIGM-HF no hubo aumento significativo de los posibles eventos adversos asociados a las estatinas en los pacientes tratados con sacubitrilo/valsartán y con una estatina. No obstante, otros análisis más detallados han indicado que las dosis más altas de estatinas se asociaron con mayor frecuencia de eventos adversos al combinar sacubitrilo/valsartán o con enalapril. Sin embargo, los patrones fueron diferentes dependiendo de cuál fuera la estatina específica administrada. A la espera de los resultados de nuevos estudios, se ha recomendado precaución al utilizar estas combinaciones de fármacos7.
El ensayo PARADIGM-HF se centra en la insuficiencia cardiaca crónica con FEVI reducida. Por consiguiente, se plantea la siguiente cuestión: ¿que sucede al otro 50% de pacientes con insuficiencia cardiaca pero con FEVI conservada (ICFEp)? Actualmente no se dispone de ensayos clínicos con pacientes con ICFEp que pongan de manifiesto un beneficio terapéutico con los fármacos comúnmente utilizados para pacientes con FEVI reducida. Por consiguiente, los tratamientos para la ICFEp van dirigidos al control de los síntomas y los factores de riesgo cardiovascular. Sin embargo, en pacientes con ICFEp, el sacubitrilo/valsartán presentó unos resultados de seguridad y eficacia prometedores en un ensayo de fase 2. El PARAMOUNT es un ensayo aleatorizado, a doble ciego, de grupos paralelos y con tratamiento de control activo, en el que se comparó el sacubitrilo/valsartán con valsartán solo9. El objetivo principal era el cambio del NT-proBNP a las 12 semanas respecto al valor basal. Los grupos de tratamiento comparados tenían unas características basales similares. La mayoría de los pacientes eran de edad avanzada, mujeres, con sobrepeso y en NYHA II. Se detectó mayor reducción del NT-proBNP en la semana 4 de tratamiento en el grupo de sacubitrilo/valsartán que en el de valsartán, aunque no alcanzó significación estadística (p = 0,063). A las 12 semanas, el NT-proBNP se redujo significativamente en el grupo de sacubitrilo/valsartán en comparación con el de valsartán (p = 0,005). Los resultados del estudio PARAMOUNT indican que el sacubitrilo/valsartán puede tener efectos favorables en los pacientes con ICFEp. Está en curso un nuevo estudio en la población con ICFEp, el PARAGON, un ensayo multicéntrico, aleatorizado, a doble ciego, de grupos paralelos y con tratamiento de control activo. Su objetivo es evaluar la eficacia y la seguridad del sacubitrilo/valsartán en comparación con el valsartán en cuanto a morbilidad y mortalidad en pacientes con insuficiencia cardiaca (NYHA II–IV) y FEVI conservada.
Por último, recientemente se ha propuesto el uso de la neprilisina soluble (sNEP) circulante como posible biomarcador2. Actualmente, los datos disponibles sobre la sNEP indican que puede tener valor pronóstico tanto en la insuficiencia cardiaca crónica10 como en la descompensación aguda de la insuficiencia cardiaca11, aunque en la ICFEp los resultados son más controvertidos12. Tiene interés señalar que se observó que la sNEP circulante era catalíticamente activa13. Además, un estudio reciente ha demostrado que la sNEP puede incluso ser superior al NT-proBNP como biomarcador pronóstico indirecto del eje neurohormonal en la insuficiencia cardiaca14. Será imprescindible perfeccionar los ensayos de la sNEP antes de introducirla en la práctica clínica. Sin embargo, los datos presentados hasta el momento apuntan que puede llegar a ser un instrumento valioso para establecer el pronóstico de los pacientes y en última instancia orientar el tratamiento.
A modo de epílogo, es probable que el coste del tratamiento con este nuevo fármaco sea un obstáculo para su uso en la práctica clínica cotidiana, puesto que el coste de otros fármacos eficaces, como el IECA enalapril, es muy bajo (comparable al coste de un chicle en muchos países). Parece concebible que pueda proponerse la aplicación de una estrategia basada en un biomarcador para determinar el cambio preferente de un tratamiento con IECA a Entresto para los pacientes con insuficiencia cardiaca inestable. En esta misma línea, es de destacar que el uso de péptidos natriuréticos era uno de los criterios de inclusión de pacientes en el ensayo PARADIGM-HF. Se deberá investigar intensivamente la relación coste-efectividad y el coste por año de vida ganado ajustado por calidad con el uso de sacubitrilo/valsartán en comparación con enalapril en el tratamiento de la ICFEr en escenarios de práctica clínica real adaptados a las características de cada país y cada sistema de asistencia sanitaria15.
CONFLICTO DE INTERESESA. Bayes-Genis y J. Lupón han solicitado una patente para sNEP como biomarcador pronóstico, que está pendiente de aprobación. A. Bayes-Genis ha dictado conferencias y ha participado en Consejos Asesores de Novartis.