La miopatía autoinmunitaria necrosante (MAN) es una entidad muy poco frecuente pero grave, cuya forma de presentación puede ser el daño cardiaco1. Se presenta un excepcional caso de miocarditis por MAN que supuso un reto diagnóstico y pone de manifiesto la utilidad de los estudios de autoinmunidad en las miocarditis de origen incierto. Además, se lleva a cabo una revisión de esta enfermedad sistémica y su daño cardiaco.
Mujer de 82 años, con antecedentes de hipercolesterolemia sin tratamiento, sin historia de diabetes mellitus, hipertensión arterial o cardiopatía previa, acudió al servicio de urgencias por una disnea a moderados esfuerzos de 4 semanas de evolución, sin otros síntomas ni signos de insuficiencia cardiaca.
A su llegada se realizó analítica, en la que destacaban elevación de la troponina T y la creatincinasa (figura A), y un electrocardiograma con bloqueo completo de la rama izquierda, ya presente en los previos; el hemograma, la coagulación, la bioquímica básica y la radiografía de tórax no mostraron alteraciones. Con la sospecha de disnea como equivalente anginoso, se decidió ingresar a la paciente para completar los estudios.
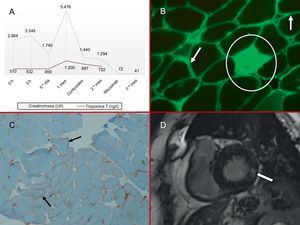
A: marcadores de daño miocárdico; elevación de ambas enzimas con predominio de la creatincinasa. B: biopsia muscular, inmunofluorescencia para IgG (×10); las flechas indican la acumulación de fibras musculares en la membrana plasmática y el círculo indica la fibra necrótica intramisial. C: biopsia muscular, tinción inmunohistoquímica para MCH1 (×10); sobreexpresión de anti-MCH1 de fibras musculares (flechas) en la membrana plasmática. D: resonancia magnética cardiaca, secuencia de realce tardío con gadolinio; la flecha indica la captación intramiocárdica inferolateral basal. MCH1: antígeno de histocompatibilidad de clase I.
La ecocardiografía transtorácica mostró unas funciones sistólicas general y segmentaria normales, sin valvulopatías; a la coronariografía no aparecían lesiones.
Dada la persistente elevación de los marcadores de daño miocárdico sin indicios de isquemia, se consideró la posibilidad de miocarditis. Una vez descartado el origen infeccioso o tóxico, con enzimas musculares persistentemente elevadas, se sospechó una miopatía, y se solicitó un perfil de anticuerpos específicos, que resultaron positivos para antipartículas de reconocimiento de señal (anti-SRP).
Con la sospecha de una MAN asociada con anticuerpos anti-SRP, se realizó tomografía computarizada toracoabdominopelviana y se determinaron los marcadores tumorales, que no mostraron neoplasia como desencadenante del cuadro autoinmunitario. El estudio neurofisiológico y la biopsia muscular eran compatibles con MAN (figura B y C).
Ante el daño miocárdico enzimático con una ecocardiografía transtorácica inespecífica, se solicitó resonancia magnética (RM) cardiaca, que mostró un ventrículo izquierdo no dilatado, con función sistólica normal, y áreas intramiocárdicas en los segmentos inferior y lateral basal de captación tardía de gadolinio compatibles con fibrosis (figura D).
Recibió tratamiento con ácido acetilsalicílico, bloqueadores beta y esteroides: 3 bolos de 250 mg de 6-metilprednisolona seguidos de prednisona a dosis de 0,4 mg/kg/día. Dado el pronóstico grave, se decidió administrar rituximab 1 g i.v., repetido a las 2 semanas. Siguió una pauta decreciente de prednisona, y a los 3 meses estaba sin disnea y se habían normalizado los marcadores de daño miocárdico.
Las miopatías inflamatorias autoinmunitarias (MIA) son un grupo heterogéneo de trastornos musculares caracterizados por debilidad muscular, elevación de la creatincinasa y alteraciones electromiográficas, además de hallazgos típicos en la biopsia muscular, como infiltrados inflamatorios, necrosis y/o expresión anómala del antígeno de histocompatibilidad de clase I (MCH1)1.
Clásicamente, las miopatías inflamatorias se clasificaban como polimiositis, dermatomiositis, miositis por cuerpos de inclusión, miositis necrosante e inespecíficas, con base en criterios anatomopatológicos y clínicos. En los últimos años, con la descripción de nuevos anticuerpos y la disponibilidad de técnicas para determinarlos, se ha propuesto una reclasificación con el término de MIA, dado que casi todas presentan diferentes anticuerpos2.
Nuestro caso muestra una MAN, en la que, a diferencia de otras MIA, la biopsia muscular muestra un patrón inflamatorio mínimo o ausente, pero marcadas áreas de necrosis y regeneración.
La MAN ocurre sola o junto con infecciones virales, cáncer, esclerodermia o fármacos (estatinas). Existen 2 anticuerpos asociados: anticuerpos anti-SRP y anticuerpos contra la 3-hidroxi-3-metilglutaril-coenzima A reductasa2, aunque hasta en un tercio de los pacientes son negativos.
Los anticuerpos anti-SRP son muy específicos y se asocian con formas más agudas, mayores concentraciones de creatincinasa y mayor daño de músculos respiratorios y esofágicos. El daño cardiaco es menos frecuente1–3.
Oppenheim describió el daño cardiaco en las MIA por primera vez en 1899. Su prevalencia está todavía por determinar (un 6-75%, según selección de pacientes y métodos para determinar el daño cardiaco), pero se considera que es una manifestación clínica mayor y una de las principales causas de muerte3,4.
La expresión clínica del daño cardiaco es relativamente infrecuente (3-6%); la miocarditis es la manifestación más común (40%). Se cree que la miocarditis recurrente podría llevar a la fibrosis del tejido de conducción, los vasos y el miocardio, y como consecuencia final produce insuficiencia cardiaca, que es la causa más frecuente de muerte cardiovascular (20%)5,6. Sin embargo, el daño subclínico oscilaría entre el 13 y el 72%, con amplia variedad de presentaciones: alteraciones electrocardiográficas (arritmias, alteraciones de conducción y repolarización), ecocardiográficas (disfunción diastólica, patrón de tako-tsubo) y en RM, que destaca como mejor técnica para detectar inflamación miocárdica inicial y fibrosis miocárdica en fase crónica3.
Nuestro caso pone de manifiesto la relevancia de alcanzar un diagnóstico etiológico del daño miocárdico no isquémico, además de la posibilidad de que el daño cardiaco sea la única manifestación de las MIA. Destacan la importancia de la RM cardiaca, los estudios de autoinmunidad y, sobre todo, la colaboración multidisciplinaria para un adecuado abordaje clínico de estas entidades.
CONFLICTO DE INTERESESC. Morís de la Tassa es proctor y advisory boards de Medtronic.