La ecocardiografía con speckle tracking bidimensional es un nuevo instrumento para evaluar la función del miocardio. El objetivo de este estudio fue evaluar los parámetros de rotación y strain del ventrículo izquierdo mediante la ecocardiografía con speckle tracking bidimensional en un gran grupo de adultos sanos de una amplia gama de edades, con objeto de establecer los valores de referencia de dichos parámetros y determinar la influencia de la edad, el sexo y los factores hemodinámicos.
MétodosSe realizaron ecocardiografías transtorácicas a 247 voluntarios sanos (139 mujeres; media de edad, 44 ± 16 [intervalo, 18-80] años). Efectuamos determinaciones de los valores de strain sistólico máximo longitudinal, circunferencial y radial, así como de la rotación y el giro del ventrículo izquierdo.
ResultadosLos valores medios de strain total longitudinal, radial y circunferencial fueron –21,5% ± 2,0%, 40,1 ± 11,8% y –22,2 ± 3,4%, respectivamente. El strain longitudinal fue significativamente más negativo en las mujeres, mientras que el strain radial y el circunferencial y los parámetros rotacionales fueron similares en ambos sexos. En consecuencia, los límites inferiores de la normalidad para los componentes del strain fueron –16,9% en los varones y –18,5% en las mujeres para el strain longitudinal, –15,4% para el strain circunferencial y 24,6% para el strain radial, con independencia del sexo. Los valores de strain longitudinal fueron más negativos en la base que en los segmentos apicales. Los valores medios de la rotación fueron–6,9 ± 3,5° en la base, 13,0 ± 6,5° para la rotación apical y 20,0 ± 7,3° para el giro neto.
ConclusionesPresentamos una evaluación detallada de la deformación normal del miocardio y la mecánica rotacional en una cohorte amplia de voluntarios sanos. Observamos que las mujeres presentan un strain longitudinal más negativo, lo cual explica su mayor fracción de eyección del ventrículo izquierdo. La disponibilidad de valores de referencia de esos parámetros puede facilitar su aplicación en la práctica clínica habitual.
Palabras clave
Se ha descrito que la función sistólica del ventrículo izquierdo (VI) es un predictor potente de la supervivencia a largo plazo de los pacientes afectados de una amplia gama de enfermedades cardiacas1–3. El parámetro ecocardiográfico más ampliamente utilizado para cuantificar la función sistólica del VI es la fracción de eyección del VI (FEVI). Aunque la FEVI es un potente predictor de mortalidad y se emplea para seleccionar a pacientes para implante de dispositivos4, intervenciones quirúrgicas5 y tratamientos farmacológicos6, es un parámetro con una extrema dependencia de la carga, su determinación mediante ecocardiografía depende de manera crucial del conocimiento experto del operador y, además, se ve afectado por una variabilidad intraobservador e interobservadores significativa1.
La función general del VI es el resultado de la contracción y relajación de una compleja arquitectura de fibras miocárdicas y un continuo transmural entre dos geometrías de fibras helicoidales, en el que la geometría helicoidal de giro derecho en la capa subendocárdica de la pared miocárdica se transforma gradualmente en una geometría de giro izquierdo en la capa subepicárdica7,8. La contracción de las fibras miocárdicas determina cambios en el tamaño y la forma del VI que son el resultado del acortamiento longitudinal, la rotación circunferencial y el engrosamiento radial simultáneos del miocardio. La FEVI proporciona un índice general de la función de la cámara del VI, sin tener en cuenta el papel relativo de los diferentes componentes de la función miocárdica (deformación en diversas direcciones y rotación), que pueden verse afectados en grados diversos en distintas enfermedades cardiacas, a pesar de que la FEVI continúe estando en valores normales9.
La ecocardiografía por seguimiento de marcas, o speckle tracking, bidimensional ha surgido recientemente como una técnica novedosa para la evaluación objetiva y cuantitativa de la función miocárdica general y regional, de manera independiente del ángulo de insonación miocárdica10–12. Los datos de deformación miocárdica (strain [¿]) se obtienen mediante una medición automática, fotograma a fotograma, de la distancia entre dos puntos de cada segmento del VI durante el ciclo cardiaco, en tres dimensiones (radial [R¿], circunferencial [C¿] y longitudinal [L¿]).
Además, la ecocardiografía con speckle tracking bidimensional puede usarse para evaluar la mecánica rotacional del VI. La rotación del VI puede medirse con proyecciones de eje corto bidimensionales obtenidas en la base y en los niveles apicales, para permitir el cálculo con y sin giro. Varios estudios han relacionado la dinámica del giro cardiaco con la función sistólica del VI13,14.
Sin embargo, para que resulte clínicamente útil, todos estos nuevos parámetros de la función miocárdica y del VI requieren valores de referencia con los que comparar los datos obtenidos de los pacientes en que se sospechen enfermedades miocárdicas. Hasta la fecha, los valores de referencia obtenidos para los parámetros rotacionales y de deformación han sido escasos, heterogéneos y, a veces, discrepantes15–18.
En consecuencia, diseñamos este estudio prospectivo observacional para utilizar la ecocardiografía con speckle tracking bidimensional en voluntarios sanos para obtener valores de referencia para L¿, C¿, R¿ y rotación y giro del VI, así como para evaluar su relación con el sexo y la edad.
MÉTODOSPoblación en estudioSe seleccionó una cohorte de 260 voluntarios caucásicos sanos, seleccionados de manera prospectiva en un único centro de asistencia de nivel terciario entre empleados del hospital, médicos en formación, sus familiares y personas que acudían a visitas médicas para obtener permisos de conducir o de trabajo y que cumplían los criterios de inclusión. Los criterios prospectivos para la inclusión fueron: edad > 17 años, ausencia de antecedentes de enfermedades cardiovasculares o pulmonares, ausencia de síntomas, ausencia de factores de riesgo cardiovascular (hipertensión, tabaquismo, diabetes mellitus o dislipemia), ausencia de tratamientos cardioactivos o vasoactivos y resultados normales en la electrocardiografía y la exploración física. Los criterios de exclusión fueron el entrenamiento deportivo, el embarazo y un índice de masa corporal > 30. Se determinó la presión arterial (PA) de todos los participantes inmediatamente antes de realizar el examen ecocardiográfico. Se determinó la talla y el peso con un estadiómetro calibrado y una báscula, y se calculó el área de superficie corporal con la fórmula de Dubois y Dubois19. Se calculó el índice de masa corporal dividiendo el peso en kilogramos por el cuadrado de la talla en metros.
El estudio recibió la aprobación del Comité de Ética de la Universidad de Padua (protocolo número 2380 P, aprobado el 6 de octubre de 2011) y se obtuvo el consentimiento informado por escrito de todos los voluntarios antes de realizar el examen de selección inicial para determinar la elegibilidad para el estudio.
EcocardiografíaSe examinó a los participantes en el estudio mediante ecocardiografía transtorácica en decúbito lateral izquierdo, utilizando un ecógrafo comercial (Vivid E9, GE Vingmed; Noruega) equipado con un transductor de 2,5 MHz. Se obtuvieron proyecciones bidimensionales (escala de grises) con un abordaje apical (proyecciones de cuatro y dos cámaras y de eje largo) y paraesternal (proyecciones de eje corto a nivel de la válvula mitral, a nivel del músculo papilar y a nivel apical). Se obtuvieron registros de tres ciclos cardiacos consecutivos de cada proyección mientras el sujeto aguantaba la respiración al final de la espiración. Se tuvo especial cuidado en obtener imágenes apicales y de eje corto correctas utilizando puntos de referencia anatómicos estándares y verificando el escorzo de la perspectiva10. Para obtener la proyección de eje corto apical, se colocó el transductor sobre la pared torácica a la altura del impulso apical y luego se desplazó un espacio intercostal hacia arriba y se aplicó la angulación correcta para obtener una proyección de eje corto circular del VI con el área mínima del ventrículo derecho20. Todas las imágenes se obtuvieron con la misma frecuencia de fotogramas (50-80 cuadros/s). Se determinó el momento de cierre de la válvula aórtica examinando el movimiento de dicha válvula en la proyección apical de eje largo. Todos los exámenes se registraron digitalmente y se transfirieron a una estación de trabajo dedicada para su posterior análisis.
Se midieron los volúmenes telesistólico y telediastólico del VI mediante regla de sumación de disco biplanar y se calculó la FEVI21.
El análisis de las imágenes de speckle tracking se realizó con un programa informático comercial (EchoPAC BT 12, GE-Vingmed; Noruega). El límite del endocardio en el VI se trazó a mano ligeramente por dentro del miocardio. A continuación se generó automáticamente un segundo círculo concéntrico mayor cerca del epicardio, para incluir todo el miocardio del VI. Luego, el programa dividió automáticamente cada proyección del VI en seis segmentos iguales y realizó el speckle tracking fotograma a fotograma.
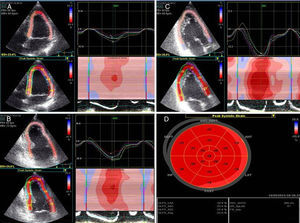
Se utilizaron las tres proyecciones apicales para las determinaciones del L¿. Se utilizaron las proyecciones de eje corto para la medición del R¿, el C¿ y la rotación. Concretamente, el R¿ y el C¿ se determinaron en la proyección de eje corto obtenida a nivel del músculo papilar (parte media del ventrículo), mientras que la rotación se determinó en las proyecciones de eje corto obtenidas a nivel basal y apical. El programa dividió automáticamente cada proyección ecocardiográfica en seis segmentos, proporcionó una confirmación automatizada del tracking (que el operador debe verificar) y generó los valores de ¿, expresados en porcentaje. Si había más de tres de los 16 segmentos del VI con un tracking inadecuado, se excluía al paciente del análisis final. Se excluyó de los análisis a 13 sujetos sanos debido al tracking inadecuado. Los valores de L¿ miocárdico se presentan en forma de diagrama de ojo de buey (mapa polar) (figura 1).
Perfiles de strain de tres proyecciones apicales. Análisis de ecocardiografía con speckle tracking en las proyecciones apicales de cuatro (A) y dos cámaras (B) y de eje largo (C) con las respectivas mediciones en la ecocardiografía con speckle tracking. Se utiliza la media de los valores segmentarios de cada segmento para generar una presentación en «ojo de buey» (mapa polar) de la deformación miocárdica del ventrículo izquierdo (D).
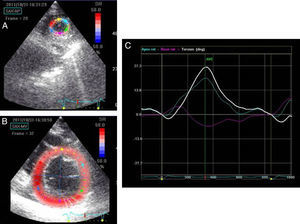
La rotación es un desplazamiento angular de un segmento miocárdico en una proyección de eje corto alrededor del eje longitudinal del VI en un solo plano11. Para medir la rotación del VI, el programa definía el centroide ventricular para la línea media miocárdica en cada fotograma y calculaba la rotación de dominio temporal para cada segmento en las proyecciones de eje corto basal y apical. Se utilizó la media de rotaciones VI de seis segmentos para la medición de la rotación a nivel basal y a nivel apical. El programa indicaba la calidad del tracking de cada segmento, y se excluyeron los segmentos con tracking insuficiente. La rotación media se determinó en el momento de cierre de la válvula aórtica. La rotación en sentido antihorario se expresa con valores positivos cuando se visualiza desde el vértice, y la rotación en sentido horario se expresa con valores negativos. El giro se calculó como la diferencia neta entre la rotación apical y la basal (figura 2). La rotación y el giro se expresan en grados.
Proyecciones de eje corto del ventrículo izquierdo a nivel apical (A) y basal (B) con la región de interés a cada nivel. Curvas de perfiles de rotación y giro del ventrículo izquierdo (C). La línea blanca indica el giro ventricular izquierdo. Las líneas azul y rosa indican las rotaciones apical y basal. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Se verificó que la distribución de los datos fuera normal con la prueba de Kolmogorov-Smirnov. Los datos se resumen como media ± desviación estándar. Se estratificó a los participantes incluidos por edad (18–35, 36–55 y 56–80 años) y sexo. Se compararon los valores de strain de varones y mujeres de diferentes grupos de edad y segmentos o paredes mediante la prueba de la t de Student bilateral para datos no apareados ANOVA (análisis de la varianza) según fuera apropiado. Los datos se analizaron con el programa SPSS para Windows versión 17.0 (SPSS Inc.; Chicago, Illinois, Estados Unidos) y se consideró estadísticamente significativos los valores de p<0,05.
ReproducibilidadLa reproducibilidad interobservadores de las determinaciones del strain se evaluó en 18 pacientes elegidos aleatoriamente; dos observadores independientes realizaron un análisis de los datos sin conocer los resultados del otro. La reproducibilidad intraobservador se evaluó con un observador que analizó los conjuntos de datos dos veces, con más de 1 mes de separación entre ellas. Tanto para la reproducibilidad intraobservador como para la interobservadores, se realizaron análisis de Bland-Altman (sesgo–limites de coincidencia) y se calculó el coeficiente de correlación intraclase.
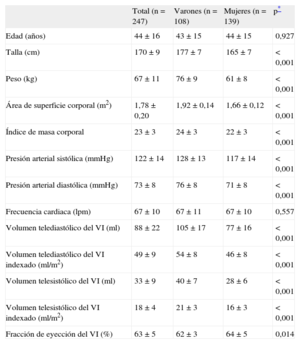
RESULTADOSSe incluyó en el estudio a un total de 247 voluntarios sanos, de los que 139 (56,2%) eran mujeres. La media de edad era 44 ± 16 (intervalo, 18-80) años. En la tabla 1 se indican las características demográficas y la geometría y la función del VI de la población en estudio. Los varones presentaban área de superficie corporal, índice de masa corporal y PA en valores más altos que las mujeres (p<0,001 en todos los casos). Los varones tenían también valores superiores de los volúmenes del VI; en las mujeres, la FEVI era significativamente mayor (p=0,014) que la de los varones.
Características demográficas y geometría y función del ventrículo izquierdo en la población en estudio
| Total (n=247) | Varones (n=108) | Mujeres (n=139) | p* | |
| Edad (años) | 44 ± 16 | 43 ± 15 | 44 ± 15 | 0,927 |
| Talla (cm) | 170 ± 9 | 177 ± 7 | 165 ± 7 | <0,001 |
| Peso (kg) | 67 ± 11 | 76 ± 9 | 61 ± 8 | <0,001 |
| Área de superficie corporal (m2) | 1,78 ± 0,20 | 1,92 ± 0,14 | 1,66 ± 0,12 | <0,001 |
| Índice de masa corporal | 23 ± 3 | 24 ± 3 | 22 ± 3 | <0,001 |
| Presión arterial sistólica (mmHg) | 122 ± 14 | 128 ± 13 | 117 ± 14 | <0,001 |
| Presión arterial diastólica (mmHg) | 73 ± 8 | 76 ± 8 | 71 ± 8 | <0,001 |
| Frecuencia cardiaca (lpm) | 67 ± 10 | 67 ± 11 | 67 ± 10 | 0,557 |
| Volumen telediastólico del VI (ml) | 88 ± 22 | 105 ± 17 | 77 ± 16 | <0,001 |
| Volumen telediastólico del VI indexado (ml/m2) | 49 ± 9 | 54 ± 8 | 46 ± 8 | <0,001 |
| Volumen telesistólico del VI (ml) | 33 ± 9 | 40 ± 7 | 28 ± 6 | <0,001 |
| Volumen telesistólico del VI indexado (ml/m2) | 18 ± 4 | 21 ± 3 | 16 ± 3 | <0,001 |
| Fracción de eyección del VI (%) | 63 ± 5 | 62 ± 3 | 64 ± 5 | 0,014 |
VI: ventrículo izquierdo.
Los datos expresan media ± desviación estándar.
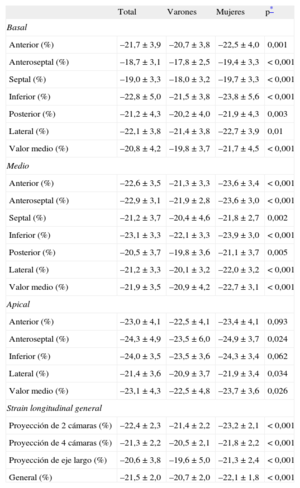
El valor de L¿ general fue –21,5 ± 2,0% y más negativo en las mujeres que en los varones (p<0,001) (tabla 2), lo cual explica que su FEVI fuera más alta. En consecuencia, el límite inferior de la normalidad (media – 2 desviaciones estándar) fue –16,9% en los varones y –18,5% en las mujeres. El valor de L¿ general fue similar en los tres grupos de edad (p=0,106) (tabla 3).
Valores de strain regional y general en el conjunto de la población en estudio y comparaciones entre varones y mujeres
| Total | Varones | Mujeres | p* | |
| Basal | ||||
| Anterior (%) | –21,7 ± 3,9 | –20,7 ± 3,8 | –22,5 ± 4,0 | 0,001 |
| Anteroseptal (%) | –18,7 ± 3,1 | –17,8 ± 2,5 | –19,4 ± 3,3 | < 0,001 |
| Septal (%) | –19,0 ± 3,3 | –18,0 ± 3,2 | –19,7 ± 3,3 | < 0,001 |
| Inferior (%) | –22,8 ± 5,0 | –21,5 ± 3,8 | –23,8 ± 5,6 | < 0,001 |
| Posterior (%) | –21,2 ± 4,3 | –20,2 ± 4,0 | –21,9 ± 4,3 | 0,003 |
| Lateral (%) | –22,1 ± 3,8 | –21,4 ± 3,8 | –22,7 ± 3,9 | 0,01 |
| Valor medio (%) | –20,8 ± 4,2 | –19,8 ± 3,7 | –21,7 ± 4,5 | < 0,001 |
| Medio | ||||
| Anterior (%) | –22,6 ± 3,5 | –21,3 ± 3,3 | –23,6 ± 3,4 | < 0,001 |
| Anteroseptal (%) | –22,9 ± 3,1 | –21,9 ± 2,8 | –23,6 ± 3,0 | < 0,001 |
| Septal (%) | –21,2 ± 3,7 | –20,4 ± 4,6 | –21,8 ± 2,7 | 0,002 |
| Inferior (%) | –23,1 ± 3,3 | –22,1 ± 3,3 | –23,9 ± 3,0 | < 0,001 |
| Posterior (%) | –20,5 ± 3,7 | –19,8 ± 3,6 | –21,1 ± 3,7 | 0,005 |
| Lateral (%) | –21,2 ± 3,3 | –20,1 ± 3,2 | –22,0 ± 3,2 | < 0,001 |
| Valor medio (%) | –21,9 ± 3,5 | –20,9 ± 4,2 | –22,7 ± 3,1 | < 0,001 |
| Apical | ||||
| Anterior (%) | –23,0 ± 4,1 | –22,5 ± 4,1 | –23,4 ± 4,1 | 0,093 |
| Anteroseptal (%) | –24,3 ± 4,9 | –23,5 ± 6,0 | –24,9 ± 3,7 | 0,024 |
| Inferior (%) | –24,0 ± 3,5 | –23,5 ± 3,6 | –24,3 ± 3,4 | 0,062 |
| Lateral (%) | –21,4 ± 3,6 | –20,9 ± 3,7 | –21,9 ± 3,4 | 0,034 |
| Valor medio (%) | –23,1 ± 4,3 | –22,5 ± 4,8 | –23,7 ± 3,6 | 0,026 |
| Strain longitudinal general | ||||
| Proyección de 2 cámaras (%) | –22,4 ± 2,3 | –21,4 ± 2,2 | –23,2 ± 2,1 | < 0,001 |
| Proyección de 4 cámaras (%) | –21,3 ± 2,2 | –20,5 ± 2,1 | –21,8 ± 2,2 | < 0,001 |
| Proyección de eje largo (%) | –20,6 ± 3,8 | –19,6 ± 5,0 | –21,3 ± 2,4 | < 0,001 |
| General (%) | –21,5 ± 2,0 | –20,7 ± 2,0 | –22,1 ± 1,8 | < 0,001 |
Los datos expresan media ± desviación estándar.
Cambios relacionados con la edad en los valores generales de strain longitudinal, circunferencial y radial
| Grupos de edad (años) | p* | |||
| 18-35 (n=77) | 36-55 (n=107) | 56-80 (n=63) | ||
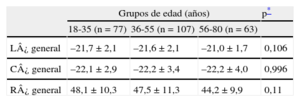
| L¿ general | –21,7 ± 2,1 | –21,6 ± 2,1 | –21,0 ± 1,7 | 0,106 |
| C¿ general | –22,1 ± 2,9 | –22,2 ± 3,4 | –22,2 ± 4,0 | 0,996 |
| R¿ general | 48,1 ± 10,3 | 47,5 ± 11,3 | 44,2 ± 9,9 | 0,11 |
C¿: strain circunferencial; L¿: strain longitudinal; R¿: strain radial.
Los niveles basal, medio y apical corresponden a los niveles de válvula mitral, músculo papilar y vértice respectivamente.
Los datos expresan media ± desviación estándar.
A nivel segmentario, se determinaron valores de L¿ menos negativos en los segmentos basales y el L¿ se hacía más negativo al desplazarse de la base hacia el vértice (p=0,009) (tabla 2). De entre los segmentos basales del VI, el septal y el anteroseptal mostraban un L¿ menos negativo, y la pared inferior mostró el valor más negativo de L¿. De entre los segmentos del VI a nivel medio del ventrículo, el que tuvo un L¿ menos negativo fue el de la pared posterior, y el L¿ más negativo se dio en las paredes inferior y anteroseptal. De entre los segmentos apicales, el que tuvo un L¿ menos negativo fue el de la pared lateral, y el L¿ más negativo, la pared anteroseptal.
La media de los valores de L¿ promedio en la base, la pared media del ventrículo y el vértice fue más negativa en las mujeres que en los varones, lo cual explica el mayor valor de L¿ general obtenido en las mujeres (tabla 2).
En los voluntarios sanos que participaron en este estudio, no hubo una correlación significativa entre los parámetros hemodinámicos, como frecuencia cardiaca y PA sistólica y diastólica, y los valores de L¿ general (r=0,01, p=0,84; r=0,12, p=0,05 y r=0,12, p=0,06 respectivamente). Sin embargo, se observó una correlación positiva entre los valores de L¿ general y el índice de masa corporal (r=0,25; p<0,001) o el área de superficie corporal (r=0,24; p<0,001).
Strain circunferencial y radialEl C¿ general y el R¿ general fueron –22,2 ± 3,4% y 46,9 ± 10,7%, respectivamente, y no mostraron diferencias entre varones y mujeres (C¿, –22% ± 3,4% frente a –22,3 ± 3,4%, p=0,526; R¿, 47,4 ± 9,2% frente a 46,7 ± 11,7%, p=0,655). En consecuencia, el límite inferior de la normalidad puede establecerse en –15,4% para el C¿ y 24,6% para el R¿ con independencia del sexo del paciente.
De manera similar a lo observado en el L¿, no hubo diferencias significativas en el R¿ y el C¿ generales entre los tres grupos de edad (tabla 3).
Rotación y giro del ventrículo izquierdoDe los 247 participantes incluidos en el estudio, en 194 (78,5%) se dispuso de proyecciones de eje corto de calidad suficiente para permitir la medición de la rotación del VI a nivel apical y a nivel basal. En cada proyección, se exigió un mínimo de cuatro segmentos con una puntuación de tracking excelente para medir la rotación. La factibilidad (en especial la adquisición de proyecciones apicales adecuadas) fue similar en las mujeres (83%) y en los varones (73%) (p=0,09).
En el momento del cierre de la válvula aórtica, la rotación basal fue –6,9 ± 3,5° en sentido horario, y la rotación apical fue 13,0 ± 6,5° en sentido antihorario. No hubo diferencias significativas entre varones y mujeres a niveles basal y apical (p > 0,05). Los valores medios de rotación apical y basal en el momento del cierre de la válvula aórtica en la población en estudio se muestran en la tabla 4.
Mecánica rotacional del ventrículo izquierdo y comparación de los valores de varones y mujeres
| Total | Varones | Mujeres | p* | |
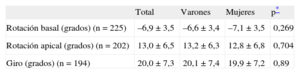
| Rotación basal (grados) (n=225) | –6,9 ± 3,5 | –6,6 ± 3,4 | –7,1 ± 3,5 | 0,269 |
| Rotación apical (grados) (n=202) | 13,0 ± 6,5 | 13,2 ± 6,3 | 12,8 ± 6,8 | 0,704 |
| Giro (grados) (n=194) | 20,0 ± 7,3 | 20,1 ± 7,4 | 19,9 ± 7,2 | 0,89 |
Los valores de rotación positivos y negativos indican rotación en sentido antihorario y horario respectivamente.
Los datos expresan media ± desviación estándar.
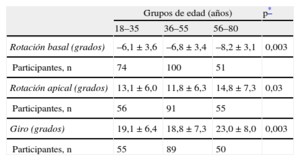
El giro aumentaba con el avance de la edad, y ello se acompañaba de un aumento constante de la rotación basal, mientras que la rotación apical aumentaba después de los 55 años (tabla 5). El giro y la rotación apical de los grupos de 18-35 años y 36-55 años años fueron comparables (diferencias no significativas), mientras que aumentaron de manera significativa en el grupo de 56–80 años (p<0,05 en ambos casos). La rotación basal del VI mostró también una correlación con el avance de la edad (r=–0,23; p=0,001).
Cambios relacionados con la edad en la rotación y el giro del ventrículo izquierdo
| Grupos de edad (años) | p* | |||
| 18–35 | 36–55 | 56–80 | ||
| Rotación basal (grados) | –6,1 ± 3,6 | –6,8 ± 3,4 | –8,2 ± 3,1 | 0,003 |
| Participantes, n | 74 | 100 | 51 | |
| Rotación apical (grados) | 13,1 ± 6,0 | 11,8 ± 6,3 | 14,8 ± 7,3 | 0,03 |
| Participantes, n | 56 | 91 | 55 | |
| Giro (grados) | 19,1 ± 6,4 | 18,8 ± 7,3 | 23,0 ± 8,0 | 0,003 |
| Participantes, n | 55 | 89 | 50 | |
Los valores de rotación positivos y negativos indican rotación en sentido antihorario y horario respectivamente.
Los datos expresan media ± desviación estándar.
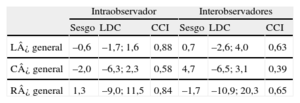
La reproducibilidad intraobservador e interobservadores de los parámetros de strain bidimensional del VI se presentan en la tabla 6.
Reproducibilidad de los parámetros del strain ventricular izquierdo en la ecocardiografía bidimensional
| Intraobservador | Interobservadores | |||||
| Sesgo | LDC | CCI | Sesgo | LDC | CCI | |
| L¿ general | –0,6 | –1,7; 1,6 | 0,88 | 0,7 | –2,6; 4,0 | 0,63 |
| C¿ general | –2,0 | –6,3; 2,3 | 0,58 | 4,7 | –6,5; 3,1 | 0,39 |
| R¿ general | 1,3 | –9,0; 11,5 | 0,84 | –1,7 | –10,9; 20,3 | 0,65 |
CCI: coeficiente de correlación intraclase; C¿: strain circunferencial; LDC: límites de coincidencia; L¿: strain longitudinal; R¿: strain radial. VI: ventrículo izquierdo.
Los estudios que presentan evaluaciones detalladas de la mecánica del VI de adultos sanos, con la inclusión de datos de la deformación miocárdica y la mecánica rotacional y de la influencia de la edad y el sexo en dichos parámetros, son escasos. Los principales resultados de este estudio pueden resumirse como sigue: a) se presentan valores de referencia para todos los componentes principales de la deformación (L¿, C¿ y R¿) así como para la mecánica de rotación, obtenidos en una cohorte amplia de voluntarios sanos; b) los valores de L¿ general fueron significativamente más negativos en las mujeres que en los varones, lo cual explica que la FEVI sea más alta en las mujeres con valores de C¿ y R¿ similares en ambos sexos; c) la edad no mostró un efecto significativo en la deformación miocárdica del VI, y d) la mecánica de rotación del VI es similar en varones y mujeres y aumenta en las décadas de la vida más tardías.
Valores de referencia para la deformación miocárdica del ventrículo izquierdoEn estudios previos que han presentado valores de referencia del L¿ general, se han utilizado cohortes relativamente pequeñas o se ha incluido a pacientes remitidos por indicaciones clínicas a examen ecocardiográfico que posteriormente resultó normal16. A pesar de la recomendación de que los valores de referencia para las variables ecocardiográficas se obtengan a partir de muestras aleatorias de voluntarios sanos22, tan solo en un estudio se utilizó a individuos completamente sanos procedentes de la población general23. Los criterios de inclusión de la población en estudio diferencian el presente ensayo de la mayor parte de los previos que han aportado intervalos de referencia para los parámetros de deformación miocárdica.
Hay mucha incertidumbre respecto a los valores de referencia de L¿, C¿ y R¿. Marwick et al17 incluyeron en su estudio a 242 individuos sanos sin factores de riesgo cardiovascular ni antecedentes de enfermedad cardiovascular, y observaron que el valor normal del L¿ general del VI era –18,6 ± 0,1%. Hurlburt et al18 describieron los valores de referencia de C¿ y R¿. Reckefuss et al16 presentaron valores de referencia regionales para el L¿ general y observaron que el L¿ era inferior en los segmentos basales y mostraba un aumento significativo de la base al vértice. Finalmente, indicaron una media del L¿ general de –20,6 ± 2,6% en su cohorte de casos iniciales normales. Según un reciente metanálisis que incluyó 24 estudios con un total de 2.597 sujetos (edad, 47 ± 11 años; el 51 ± 24% varones), los valores normales del L¿ general oscilaron entre –15,9 y –22,1% (media, –19,7%); el C¿ general normal, entre –20,9 y –27,8% (media, –23,3%), y el R¿ general, entre el 35,1 y el 59,0% (media, 47,3%). Además, estos autores observaron que todos los componentes direccionales del strain mostraban heterogeneidad y discrepancias entre los estudios23.
En el presente estudio se observaron unos valores más negativos del L¿ y menos negativos del C¿ en comparación con lo descrito en la literatura médica. Los datos de R¿ son similares a los descritos en la literatura médica,, pero es notable la falta de uniformidad, con lo que la desviación estándar es amplia. Esto puede explicarse por factores técnicos más que biológicos. El R¿ es una medida bastante inexacta, sobre todo en los segmentos laterales y basales, debido a que la distancia entre endocardio y epicardio es pequeña y la resolución espacial en esta dirección del tracking es baja.
Efecto de la edad en la deformación miocárdica del ventrículo izquierdoLos efectos de la edad en la deformación miocárdica siguen siendo motivo de controversia. Mientras que algunos estudios han mostrado una reducción de los valores de ¿ con el avance de la edad24,25, otros han descrito ausencia de cambios16,26. En un estudio muy reciente, Sun et al27 señalaron que el L¿ general pasaba a ser menos negativo con el avance de la edad, mientras que el C¿ general se hacía más negativo y el R¿ se mantenía inalterado. De manera análoga, Zghal et al28 indicaron que el L¿ general pasaba a ser menos negativo en los pacientes ancianos, pero no observaron cambios significativos en el R¿ y el C¿ generales. En otro estudio se utilizó un marcador tisular con resonancia magnética tridimensional y se comparó a adultos sanos según la edad; se observaron valores de L¿ y C¿ menos negativos en los ancianos, con un cambio que era mayor en el vértice que en la base29.
En la población de nuestro estudio, en la que se incluyó a participantes de entre 18 y 80 años de edad, no hubo correlación alguna entre la edad y la deformación miocárdica. Una posible razón puede ser el número de ancianos incluidos en la serie relativamente bajo (solo 34 > de 60 años). Sin embargo, no resulta fácil encontrar participantes sanos > 60 años de edad empleando nuestros criterios estrictos. Además, nuestros resultados concuerdan con los del metanálisis de Yingchoncharoen et al23, en el que no se documentó un efecto significativo de la edad en el L¿ general.
Diferencias entre los sexos en la deformación miocárdica del ventrículo izquierdoEl efecto del sexo en la deformación miocárdica del VI continúa siendo objeto de controversia. En varios estudios no se observaron diferencias en las determinaciones del ¿ entre varones y mujeres17,23,26,30. Sin embargo, Kuznetsova et al24 describieron valores de R¿ en mujeres mayores que en varones. Recientemente, Cheng et al31 observaron que, en promedio, el L¿ era un 1,7% más negativo en las mujeres que en los varones. Hurlburt et al18 observaron que el L¿ y el C¿ generales eran significativamente más negativos en las mujeres que en los varones. Estos resultados fueron confirmados por Reckefuss et al16, que observaron valores de L¿ más negativos en las mujeres. Por último, el estudio HUNT indicó que la deformación miocárdica era uniformemente superior en las mujeres, excepto en el grupo de edad > 60 años25.
En nuestro estudio, se observó que las mujeres presentan unos valores de L¿ más negativos, mientras que los valores de C¿ general, R¿ y rotación del VI fueron similares en varones y mujeres. Esto puede explicar las cifras de FEVI más altas en mujeres sanas que en varones sanos que tanto nosotros como otros autores hemos observado de manera uniforme32,33.
Efecto de los factores hemodinámicos y el tamaño corporal en las determinaciones del strainUn metanálisis recientemente publicado, con un total de 2.597 sujetos, indica que la PA sistólica se asocia a cambios en los valores de L¿ general normales23. Aparte de la PA sistólica, las diferencias en cuanto al fabricante y otras variables como edad, sexo e índice de masa corporal no se asociaron de manera significativa al valor medio de L¿ general en los pacientes sanos23. Aunque este metanálisis indica que la PA sistólica es un importante factor determinante del strain, nosotros no confirmamos esta observación en nuestro estudio. Además, la talla, la PA sistólica y la frecuencia cardiaca no mostraron correlación con el L¿ general en un amplio estudio realizado en voluntarios sanos17. Nuestro estudio mostró que los parámetros de tamaño corporal se correlacionan con el L¿ general. Estos datos tienden a ser controvertidos en la literatura médica: un estudio publicado con anterioridad confirma nuestra observación34, pero el metanálisis recientemente publicado indica que el índice de masa corporal no es un significativo factor determinante para la banda de normalidad del L¿ general23.
Mecánica rotacional del ventrículo izquierdoSe ha demostrado que tanto la rotación como la torsión del VI son importantes factores determinantes de la función del VI32. La rotación apical suele ser superior a la rotación basal y muestra una correlación más estrecha con la función general del VI35. Takahashi et al15 presentaron valores normales para diferentes grupos de edad. Estos autores observaron que las rotaciones basal y apical eran de 4,9 ± 2,0° y 10,1 ± 1,9°, respectivamente, en 20 sujetos normales de 33-40 años de edad. Nuestros datos muestran valores superiores de rotación del VI, en especial a la altura del vértice. Las razones de estas diferencias son difíciles de explicar. Aunque no se puede descartar un factor étnico, la explicación más probable puede estar en el nivel de la proyección de eje corto apical del VI. Van Dalen et al20 han puesto claramente de manifiesto lo crucial que es este factor y el grado en que las mediciones pueden cambiar si se desplaza la proyección tan solo unos pocos milímetros en sentido apical o caudal. Lamentablemente, no hay ningún punto de referencia anatómico claro que permita estandarizar esta proyección. En este estudio se ha tenido mucho cuidado en obtener la proyección más apical (justo antes de que desaparezca el vértice ventricular derecho) y circular posible. Sin embargo, el valor elevado de la desviación estándar en los datos de rotación debe motivar cautela respecto a la exactitud general de nuestros valores de referencia. En el presente estudio, el giro y la rotación apical de los grupos de 18-35 años y 36-55 años fueron comparables. Sin embargo, ambos parámetros mostraron un aumento significativo en el grupo de 56-80 años. De igual modo, Maharaj et al36 señalaron que el giro se modifica sustancialmente a partir de los 40 años.
Zhang et al37 observaron una rotación apical en los participantes de 55–65 años significativamente mayor (9,65 ± 1,56°) que en los de 45–55 años (7,94 ± 1,20°). Maharaj et al36 indicaron que las rotaciones apical y basal y el giro neto aumentan con el avance de la edad. Nuestros datos concuerdan con estos resultados. El giro del VI aumenta con la edad y ello se debe principalmente al aumento de la rotación del VI a la altura del vértice38. Este aumento muy probablemente esté relacionado con un desequilibrio entre las capas subendocárdica y subepicárdica, con mayor predominio de las fibras epicárdicas con el avance de la edad38.
LimitacionesEste estudio tiene algunas limitaciones. Los valores de la deformación dependen del equipo utilizado, lo cual apunta a que los valores de referencia pueden cambiar según el aparato de ecografía utilizado para la obtención de las imágenes y según el programa informático utilizado para analizarlas33,39. Los datos son aplicables únicamente a pacientes examinados con el equipo empleado en este estudio. En el futuro, es de esperar que se alcance una estandarización de los valores de strain obtenidos con aparatos de diferentes fabricantes40.
Todos los participantes eran caucásicos europeos. En consecuencia, no se puede extrapolar los resultados de este estudio a otros grupos étnicos.
CONCLUSIONESSe presenta una evaluación detallada de la deformación normal del miocardio y la mecánica rotacional del VI en una cohorte amplia de voluntarios sanos de una gran variedad de edades. Se observó que las mujeres tenían valores de L¿ más negativos que los varones, lo cual explica los valores más elevados de la FEVI en las mujeres. Además, la edad es un importante factor determinante de los valores de rotación en personas sanas, con aumento de la rotación apical y del giro del VI en los ancianos.
La disponibilidad de valores de referencia para esos parámetros puede facilitar su aplicación en la práctica clínica habitual. Según los resultados, se debe tener en cuenta el sexo del paciente al evaluar los cambios patológicos de la función miocárdica, mientras que la edad es un factor determinante de la mecánica rotacional significativo.
FINANCIACIÓNGonenc Kocabay y Sorina Mihaila han recibido una subvención de investigación financiada por la European Association of Cardiovascular Imaging.
CONFLICTO DE INTERESESDenisa Muraru y Luigi P. Badano han recibido subvenciones para equipamiento y honorarios por conferencias de GE Vingmed. Luigi P. Badano forma parte del panel de conferenciantes de esta empresa.