Los avances en los programas informáticos de fusión de imágenes tridimensionales (3D) han permitido una aplicación sencilla de las exploraciones de imagen antes de la intervención, como la tomografía computarizada (TC) y la resonancia magnética (RM), para obtener un mapa fiable para una manipulación rápida en una anatomía cardiaca compleja1,2. En un artículo publicado en Revista Española de Cardiología, Sandoval et al.3 han realizado una elegante presentación de un caso de fusión de imágenes de un mapa 3D basado en TC para el implante de un stent aórtico.
Hemos realizado una revisión retrospectiva de los implantes de stent guiados con un nuevo programa de fusión de imágenes (VesselNavigator, Philips Healthcare) durante los primeros 9 meses tras su introducción (figura). Se examinaron las características de los pacientes y los datos del cateterismo prestando especial atención a las imágenes de fusión previas a la intervención y a la guía durante esta, incluidas las estructuras empleadas para el registro, la exactitud de la superposición para la reconstrucción 3D y la necesidad de reajustes del mapa durante la intervención.
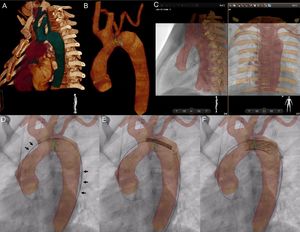
Implante de stent en el arco aórtico, asistido con el programa VesselNavigator, en un paciente de 12 años, después del tratamiento quirúrgico de una interrupción del arco aórtico (vídeo del material suplementario). La reconstrucción tridimensional (3D) automática se manipuló para trazar el arco aórtico, las ramas proximales y la aorta torácica (A). Se colocó un anillo de marcación (verde) en la parte más estrecha y un punto de marcación (amarillo) en el extremo proximal del stent (B). Se colocaron otros 2 anillos (azules) para indicar el origen de cada arteria subclavia. Se utilizó la fluoroscopia grabada en 2 proyecciones perpendiculares para la alineación manual del mapa y la fluoroscopia en vivo con las estructuras óseas utilizadas como puntos de referencia (C). La introducción del sistema de aplicación produjo una ligera distorsión de la anatomía, que se refleja en la posición de la guía en la curvatura externa de la reconstrucción 3D (D, flechas negras). El stent se colocó (E) y se desplegó (F) utilizando como guía solo el mapa 3D. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Se utilizó el programa VesselNavigator en todos los pacientes consecutivos de los que se disponía de imágenes de TC o RM previas al cateterismo. El flujo de trabajo en 4 etapas del programa VesselNavigator, que incluye segmentación, planificación, registro y guía en vivo, se ha descrito en otras publicaciones4,5. Para el registro, las imágenes bidimensionales de fluoroscopia grabadas se fusionaron con el mapa 3D (registro 2D-3D) utilizando una combinación de marcadores internos, como estructuras óseas, la silueta cardiaca, áreas de calcificación, dispositivos implantados con anterioridad y bordes de los vasos visualizados con la inyección de una pequeña cantidad de medio de contraste.
En 18 pacientes se practicó un implante percutáneo de stent para crear una «zona de aterrizaje» antes del implante percutáneo de válvula pulmonar (n=7), estenosis de la arteria pulmonar (n=5), coartación de aorta (n=3; vídeo del material suplementario), colateral aortopulmonar (n=2) o conducto arterioso (n=1) (tabla). Se elaboró un mapa 3D a partir de los conjuntos de datos de TC (n=17) o RM (n=1) existentes. Para el registro, se utilizaron la columna vertebral y las vértebras (n=17; 94%), calcificaciones (n=7; 39%), una angiografía de prueba (n=5; 28%) o un dispositivo colocado con anterioridad (n=4; 22%) como puntos de referencia para la orientación del mapa 3D frente a la fluoroscopia en vivo. Se pudo realizar la superposición en todos los pacientes excepto 2 (11%), y en otros 2 pacientes (11%) fue necesaria una realineación durante la intervención debido a la introducción de una guía rígida y el ensamblaje de balón/stent. Todos los stents se desplegaron en las localizaciones deseadas, sin que hubiera ninguna complicación. En 13 pacientes (72%), el stent se colocó y se implantó sin inyección previa de contraste.
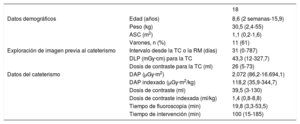
Características de los pacientes y datos de la intervención
| 18 | ||
|---|---|---|
| Datos demográficos | Edad (años) | 8,6 (2 semanas-15,9) |
| Peso (kg) | 30,5 (2,4-55) | |
| ASC (m2) | 1,1 (0,2-1,6) | |
| Varones, n (%) | 11 (61) | |
| Exploración de imagen previa al cateterismo | Intervalo desde la TC o la RM (días) | 31 (0-787) |
| DLP (mGy·cm) para la TC | 43,3 (12-327,7) | |
| Dosis de contraste para la TC (ml) | 26 (5-73) | |
| Datos del cateterismo | DAP (μGy·m2) | 2.072 (86,2-16.694,1) |
| DAP indexado (μGy·m2/kg) | 118,2 (35,9-344,7) | |
| Dosis de contraste (ml) | 39,5 (3-130) | |
| Dosis de contraste indexada (ml/kg) | 1,4 (0,8-8,8) | |
| Tiempo de fluoroscopia (min) | 19,8 (3,3-53,5) | |
| Tiempo de intervención (min) | 100 (15-185) |
ASC:área de superficie corporal; DAP:producto de área y dosis; DLP:producto de longitud y dosis; RM:resonancia magnética; TC:tomografía computarizada.
Hasta la fecha, y hasta donde nosotros sabemos, esta es la primera serie presentada que se centra en la aplicación de los conjuntos de datos 3D pregrabados exclusivamente para guiar el implante del stent en pacientes con cardiopatías congénitas. Nuestra experiencia inicial indica que, con los programas informáticos modernos de fusión de imágenes, las imágenes 3D obtenidas con técnicas no invasivas pueden reutilizarse de manera sencilla y efectiva para el posicionamiento y el implante de stents en diversas localizaciones2,4,5. Un protocolo de registro sencillo requiere solo la fluoroscopia grabada en 2 proyecciones, similar a la disposición habitual de un isocentro al inicio de cada cateterismo cardiaco, y utiliza una combinación de puntos de referencia anatómicos o iatrogénicos o la inyección de un pequeño volumen de contraste. Este registro 2D-3D permitió reducir la duración de las técnicas de intervención y la exposición al contraste y la radiación6. En varios pacientes más recientes, se ha tenido la confianza suficiente para realizar el implante del stent sin inyección previa de contraste.
Para poner a prueba la reproducibilidad de estos prometedores resultados individuales, hemos iniciado un registro prospectivo internacional con aportaciones de Berlín (Alemania), Sejong (Corea del Sur), Ciudad de México (México), Denver (Estados Unidos) y Lodz (Polonia).
En conclusión, la fusión de imágenes 3D facilita un implante preciso del stent en diversas localizaciones anatómicas. En pacientes seleccionados, puede obviarse la inyección de contraste antes del implante del stent.