La taquicardia ventricular polimórfica catecolaminérgica (TVPC) es una enfermedad hereditaria caracterizada por arritmias ventriculares (AV) polimórficas o bidireccionales desencadenadas por estrés físico o emocional en jóvenes con corazón estructuralmente normal. El pilar del tratamiento son los bloqueadores beta y recientemente se ha incorporado la flecainida al arsenal terapéutico. El objetivo de este trabajo es exponer nuestra experiencia con su uso.
MétodosDe un total de 174 pacientes pertenecientes a 7 familias afectadas de TVPC con genotipo positivo, se analizó a los que tomaron flecainida. Se valoraron la indicación, los efectos secundarios, la dosificación, los eventos clínicos, las AV y la ventana arrítmica en las pruebas de esfuerzo y las descargas del desfibrilador automático (DAI).
ResultadosRecibieron flecainida 18 pacientes (10,4%); 17 en combinación con bloqueadores beta y 1 como tratamiento único por intolerancia al bloqueador beta. Ningún paciente sufrió efectos secundarios. La indicación fue la persistencia de AV complejas en la prueba de esfuerzo en 13 pacientes (72,2%) y descargas frecuentes del DAI en los otros 5 (27,8%). En el 66,7% de la familia 1, la puntuación cuantitativa de AV en la prueba de esfuerzo se redujo más de un 50% (32,76 ± 84,06 frente a 74,38 ± 153,86 lpm; p = 0,018). La ventana arrítmica fue menor (5,8 ± 11,9 frente a 19,69 ± 21,27 lpm; p = 0,007) y 4 de los 5 pacientes con descargas apropiadas del DAI no sufrieron más descargas.
ConclusionesEn pacientes con TVPC, la flecainida reduce los eventos clínicos, las AV, la ventana arrítmica y las descargas del DAI y los pacientes la toleran bien.
Palabras clave
La taquicardia ventricular polimórfica catecolaminérgica (TVPC) es una enfermedad genética caracterizada por síncopes o muerte súbita en jóvenes sin cardiopatía estructural en contexto de estrés físico o emocional. Presenta una prevalencia baja, que en Europa se estima en 1:10.000, pero una alta letalidad, siendo la muerte súbita la primera manifestación de la enfermedad hasta en un 30% de los sujetos menores de 40 años sin tratamiento1. Hasta la fecha se han descrito mutaciones en 6 genes que dan diagnóstico genético al 70% de los casos de TVPC, de los cuales el 60% son portadores de mutación en el gen que codifica el receptor cardiaco de la rianodina (RyR2)2,3.
Los pacientes presentan un electrocardiograma en reposo y una ecocardiografía normal, y las claves diagnósticas están en la prueba de esfuerzo (PE) que desencadena arritmias ventriculares (AV) de mayor complejidad a mayor esfuerzo y/o el estudio genético que identifica una mutación patogénica4. Dado que el resultado de la PE no es reproducible —incluso puede ser negativa5—, el estudio genético es fundamental para diagnosticar a los portadores de la mutación sin expresión fenotípica4.
El pronóstico fatal de los pacientes con TVPC ha mejorado tras el uso de los bloqueadores beta, a los que se considera el pilar del tratamiento farmacológico en la TVPC4. Los bloqueadores beta no selectivos, como el nadolol o el propranolol, son los más recomendados, pues se ha demostrado mayor reducción de las AV y la ventana arrítmica durante la PE6. Sin embargo, su protección es incompleta4 y su tolerabilidad es una limitación a su uso. Además, en el seguimiento, hasta a un 30% de los pacientes con TVPC se les implanta un desfibrilador automático implantable (DAI)7, pero sus posibles complicaciones y la falta de eficacia con algunas AV son un problema de esta terapia8–12, por lo que evitar choques del DAI utilizando la medicación adecuada es muy importante en la TVPC.
La flecainida tiene un papel cada vez más relevante. En las últimas guías de práctica clínica al respecto se recomienda en pacientes con síncope recurrente o AV persistentes pese al tratamiento con bloqueadores beta4.
El objetivo es analizar las características de los pacientes con TVPC genotipo positivo en tratamiento con flecainida y estudiar su eficacia y su seguridad.
MÉTODOSSe trata de un estudio multicéntrico y bidireccional, en el que se identificó a 252 pacientes con TVPC genotipo positivo pertenecientes a 7 familias en Canarias. Para la familia 1, el estudio fue prospectivo de intervención y para las demás familias, retrospectivo. Previa firma de un consentimiento informado, se incluyó en el estudio a 174 pacientes con diagnóstico clínico y/o una mutación patogénica en el gen RyR2, que completaron el seguimiento entre diciembre de 2007 y octubre de 2015.
Análisis genéticoSe realizó a los probandos de la familia 1 un estudio genético Sanger de los genes RyR2 y CASQ2 y posteriormente un estudio de secuenciación masiva de 195 genes para descartar otros genes implicados. Por el método de secuenciación masiva, también se realizó un estudio de 195 genes a los probandos de las familias 2 y 6, y de 10 y 8 genes a los casos índice de las familias 4 y 7 respectivamente. De las familias 3 y 5, no se dispone de datos sobre el número de genes analizados. Una vez identificada la mutación en RyR2, se realizó un cribado genético en cascada.
Protocolo clínicoEn el momento del diagnóstico, se realizó a todos los individuos un electrocardiograma, un ecocardiograma, una PE y un estudio genético, así como un seguimiento clínico y una PE, según el clínico responsable lo considerara oportuno. Los miembros de la familia 1 se sometieron a un protocolo de seguimiento y tratamiento consistente en PE seriadas con titulación de las dosis del bloqueadores beta13.
Se realizó un análisis de todos los pacientes que tomaron flecainida sin modificar la dosis basal de bloqueadores beta que tenían previamente. La flecainida se inició en 2 dosis diarias hasta alcanzar la dosis máxima tolerada o un máximo de 200 mg/día.
Definición de síntoma y evento arrítmicoSe definió síntoma como la aparición de síncopes (no vasovagal) o mareos relacionados con esfuerzo o emoción. Se consideró evento arrítmico la aparición de descarga apropiada del DAI, síncope o muerte súbita.
Definición y cuantificación de las arritmias ventricularesSe definió AV como cualquier AV, incluidas las extrasístoles ventriculares, el bigeminismo, el duplete y la taquicardia ventricular sostenida o no sostenida, y AV compleja como cualquier AV a excepción de la extrasístole ventricular.
Para la cuantificación de las AV en la PE, se utilizó la puntuación cualitativa propuesta por Van der Werf et al.14, en la que se elige la puntación más alta obtenida en la PE, y la puntuación cuantitativa propuesta por Wangüemert et al.13, en la que se suman todas las AV durante la PE y se otorga una serie de puntos según su gravedad.
En la familia 1 se valoró la ventana arrítmica6, que refleja el rango de frecuencias cardiacas (FC) en que tienen lugar las AV en la PE, y se mide desde la FC de inicio de las AV hasta la FC máxima alcanzada.
La PE se realizó en tapiz rodante con el protocolo BRUCE. Se eligió la PE realizada antes del inicio de la flecainida y la primera con dosis máximas, sin modificar la dosis de bloqueadores beta. A todos los pacientes se les hizo un análisis cualitativo de las AV que sufrieron en las PE, y de los pacientes de la familia 1 se obtuvieron todas las AV detectadas, el tiempo de las pruebas, la FC máxima y basal, la ventana arrítmica y la puntuación cuantitativa.
Análisis estadísticoLa descripción de las variables cualitativas se realizó con valores absolutos y porcentajes y la de las variables cuantitativas, con media ± desviación estándar. Para determinar la asociación entre las variables cuantitativas y cualitativas, se emplearon el test de Wilcoxon y el test de McNemar respectivamente. Para variables cualitativas dicotómicas y diferentes variables continuas, se empleó la prueba de la t de Student o la U de Mann Whitney. En el análisis de medidas repetidas, debido al pequeño número de observaciones, se emplearon el test de Wilcoxon y el test de McNemar para variables cuantitativas y cualitativas respectivamente. Se consideró estadísticamente significativo un valor de p < 0,05. El análisis de los datos se realizó con el paquete estadístico SPSS.
RESULTADOSCaracterísticas de los pacientesTras un seguimiento medio de 5,6 años, de un total de 174 pacientes, 31 (17,8%) no recibieron tratamiento farmacológico por voluntad propia, se trató a 142 (81,6%) con bloqueadores beta y 1 paciente (0,6%) recibió monoterapia con flecainida. Al final del seguimiento, el 53,4% de los pacientes se encontraban en tratamiento con bloqueadores beta no selectivos, principalmente propranolol. A pesar de estar en tratamiento con bloqueadores beta, el 15% de los pacientes sufrieron algún evento arrítmico y ninguno falleció en el seguimiento.
Tomaron flecainida 18 pacientes (10,4%), 17 en combinación con bloqueadores beta y 1 como tratamiento único por intolerancia a distintos bloqueadores beta (bradicardia sintomática).
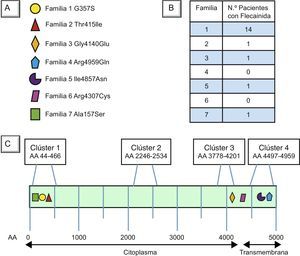
La media de edad de quienes tomaron flecainida era 32,3 ± 15,8 años; el 50% eran varones. El seguimiento medio de los pacientes tras el inicio de la flecainida fue de 2,63 ± 1,28 (intervalo, 0,47-5,75) años. Las características de los pacientes se detallan en la tabla 1. Las mutaciones diagnosticadas en cada familia aparecen en la figura 1A, el número de pacientes en tratamiento con flecainida y bloqueadores beta de cada familia se refleja en la figura 1B y la estructura, los clusters mutacionales y las mutaciones en RyR2 de las familias de nuestra cohorte se representan en la figura 1C.
Características basales de los pacientes con flecainida
| Casos índice | 6 (33,3) |
| Familiares con genotipo positivo | 12 (66,6) |
| Edad al diagnóstico (años) | 28,3 ± 16,1 |
| Sexo (varones/mujeres) | 10/18 (55,5/45,5) |
| Edad de inicio de flecainida (años) | 32,3 ± 15,8 |
| En tratamiento con bloqueadores beta no selectivos (n = 17) | 13 (76) |
| Portadores de DAI | 14 (77,8) |
| Denervación simpática cardiaca izquierda | 2 (11) |
DAI: desfibrilador automático implantable.
Los valores expresan n (%) o media ± desviación estándar.
Localización de las mutaciones en el gen RyR2 de las 7 familias afectadas de taquicardia ventricular polimórfica catecolaminérgica en Canarias. A: las mutaciones de cada familia de nuestra cohorte, y su símbolo representativo de localización en B. B: número de pacientes de cada familia en tratamiento con flecainida y bloqueador beta. C: representación esquemática de la proteína RyR2. Los clusters 1, 2, 3 y 4 representan las regiones de la proteína donde se localiza la mayor parte de las mutaciones descritas en la literatura (hot-spots3). AA: aminoácido.
Todos los pacientes siguen vivos y ninguno sufrió efectos secundarios que obligaran a suspender el tratamiento.
La indicación de añadir flecainida al tratamiento con bloqueadores beta fue en 13 pacientes (72,2%) la persistencia de AV complejas en la PE y en 5 (27,8%), la reiteración de descargas apropiadas del DAI.
De los que estaban en tratamiento con flecainida, 14 pacientes (77,8%) eran portadores de un DAI. A 11 pacientes se les pautó el tratamiento con flecainida después del implante del DAI, y la media de tiempo tras el implante del DAI hasta la introducción del antiarrítmico fue de 6,1 años.
A 2 de los pacientes se les realizó una denervación simpática cardiaca izquierda, a 1 de ellos antes del inicio de flecainida.
Dosis de flecainidaLa dosis media de flecainida al final del seguimiento era de 159,38 mg (2,3 mg/kg/día). Ningún paciente sobrepasó la dosis de 200mg/día, todos tuvieron una dosis mayor de 100mg/día y la dosis media de los pacientes con reducción superior al 50% en la puntuación cuantitativa de AV de la familia 1 fue de 123,80 ± 38,31 mg.
Repercusión clínicaDespués de asociar el antiarrítmico, 1 paciente permaneció sintomático y sufrió un síncope (5,5%), y otro (5,5%) tuvo una descarga apropiada del DAI durante el seguimiento.
Repercusión en la carga arrítmica en la prueba de esfuerzoSe realizó un total de 65 pruebas de esfuerzo a 17 pacientes (se excluyó a 1 miembro de la familia 1 sin PE posterior al inicio del fármaco). Ningún paciente tuvo una carga arrítmica mayor en las PE de seguimiento, el 61% presentó supresión completa de la carga arrítmica en la PE, y solo 1 paciente (5,5%) sufrió algunas AV complejas en las PE consecutivas de seguimiento. De los 13 pacientes de la familia 1 en los que se comparó la puntuación cuantitativa, en el 66,7% se redujo las AV en más de un 50% en las PE (tabla 2).
Comparación de los resultados entre la prueba de esfuerzo previa al inicio de flecainida y la hecha con dosis máxima en la familia 1
| N.o | Antes de flecainida | Después de flecainida | p | |
|---|---|---|---|---|
| FC basal (lpm) | 12 | 62,33 ± 9,61 | 61,41 ± 13,03 | 0,814* |
| FC máxima (lpm) | 13 | 144,23 ± 16,78 | 128,76 ± 19,79 | 0,008* |
| FC EV | 13 | 124,53 ± 26,44 | 122,92 ± 18,85 | 0,60* |
| MET | 13 | 12,43 ± 3,10 | 12,64 ± 2,80 | 0,76* |
| Puntuación AV cualitativa | 13 | 1,61 ± 1,12 | 1,15 ± 0,55 | 0,059* |
| Puntuación AV cuantitativa | 13 | 74,38 ± 153,86 | 32,76 ± 84,06 | 0,018* |
AV: arritmias ventriculares; FC: frecuencia cardiaca; FC EV: FC de aparición de las extrasístoles ventriculares.
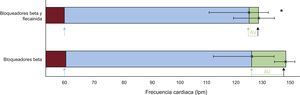
Como se muestra en la figura 2, la ventana arrítmica con el tratamiento con ambos fármacos fue significativamente menor que solo con bloqueadores beta (5,8 ± 11,9 frente a 19,69 ± 21,27 lpm; p = 0,007), y no hubo diferencias estadísticamente significativas en lo referente a la FC basal —62,3 lpm (intervalo de confianza del 95% [IC95%], 56,9-67,7) frente a 61,4 (IC95%, 54,0-68,8)— y la FC de aparición de las AV en la PE —124,5 lpm (IC95%, 110,2-138,9) frente a 122,9 (IC95%, 112,7-133,2)—. La flecainida en combinación con bloqueadores beta redujo significativamente la FC máxima respecto a los bloqueadores beta solos —128,76 lpm (IC95%, 118,0-139,5) frente a 144,23 (IC95%, 135,1-153,3); p < 0,008—, sin que variara la carga de trabajo en la PE (12,43 frente a 12,64 MET; p = 0,76).
Ventana arrítmica de los pacientes durante el tratamiento con bloqueadores beta y durante el tratamiento con bloqueadores beta y flecainida. Las barras azules indican la FC libre de arritmias durante la PE. Las barras granates indican la FC de reposo y las verdes, la frecuencia cardiaca en la que ocurren las AV. Las flechas azules indican la FC al inicio de la PE; las flechas verdes, la FC a la que se inician las AV y las negras, la FC máxima. Las líneas verdes horizontales indican la ventana arrítmica. AV: arritmia ventricular; FC: frecuencia cardiaca; PE: prueba de esfuerzo. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
De los 50 pacientes portadores de DAI de toda la cohorte de pacientes con TVPC, 14 (28%) recibieron tratamiento con flecainida, y en 11 de ellos (22%) el tratamiento con flecainida se pautó después de implantar el DAI. Se agregó flecainida a 5 pacientes por descargas apropiadas del DAI reiteradas, y 4 de ellos no volvieron a tener descargas en un seguimiento medio de 2,5 años desde el inicio del antiarrítmico. La media de seguimiento desde el implante del DAI hasta la introducción de la flecainida fue de 6,1 años.
De los 11 pacientes con flecainida pautada después del implante del DAI, 5 (45,5%) sufrieron algún tipo de evento arrítmico (síntomas o descargas apropiadas del DAI) antes de la introducción de la flecainida y 1 (9%), tras su inicio.
DISCUSIÓNEl arsenal terapéutico en la TVPC se compone actualmente de los bloqueadores beta, DAI y, recientemente, flecainida y simpatectomía4. Ninguno es completamente eficaz y todos conllevan riesgos.
La flecainida es un antiarrítmico de la clase I C que ha demostrado eficacia en la TVPC15. La acción principal de la flecainida se basa en el bloqueo selectivo de la corriente rápida de entrada de sodio en las células cardiacas y la inhibición de la apertura de los canales K (especialmente en el canal IKr)15. Sin embargo, esto es insuficiente para explicar su eficacia en la TVPC, y recientemente se han propuesto mecanismos adicionales implicados, como el bloqueo de los canales de RyR2 en su estado abierto, que reduce la liberación espontánea del calcio del retículo sarcoplásmico16,17.
Nuestro estudio demuestra que la flecainida reduce las AV, los síntomas y las descargas del DAI de los pacientes con TVPC genotipo RyR2 positivo, tratados con bloqueadores beta. Este dato es importante, ya que en nuestra serie el 15% de los pacientes seguían con síntomas a pesar de los bloqueadores beta13.
La indicación principal para agregar la flecainida a los pacientes fue la persistencia de AV complejas a pesar del tratamiento con bloqueadores beta en las PE de seguimiento (72,2%), algo similar a lo indicado previamente, pues se empleó por este motivo en el 78% de los pacientes8.
La seguridad de la flecainida en nuestra cohorte fue del 100%. Ningún paciente abandonó el tratamiento por efectos secundarios. Esta seguridad ya se había señalado en una serie de pacientes con TVPC y genotipo negativo, de la que ningún paciente suspendió el tratamiento por efectos secundarios18; sin embargo, en la serie previa de Van der Werf et al.14 se suspendió la flecainida a 1 paciente (3%) por efectos secundarios17, y en la serie de Roston et al.8 se señala que se suspendió el tratamiento en 5 pacientes (10%) por efectos adversos persistentes o crecientes en un seguimiento de 1,3 años (frente a 2,63 años en nuestra cohorte).
La flecainida añadida al bloqueador beta fue eficaz desde el punto de vista clínico y arritmogénico. Se ha descrito que hasta un 53% de los pacientes a los que se añadió la flecainida permanecieron asintomáticos, y el 38% siguió sufriendo AV8, cifras mayores que las obtenidas en nuestra cohorte.
Aunque es sabido que la carga arrítmica de un mismo paciente afectado de TVPC puede variar de una PE a otra sin modificación del tratamiento14, los resultados de la PE pueden tener relación con futuros eventos cardiacos19, de ahí que se suela usar la PE como guía de tratamiento en la práctica clínica. A los pacientes de la familia 1, la flecainida les redujo de manera significativa la puntuación de AV cuantitativa, y el 66,7% tuvo una reducción de las AV en la PE > 50%. Comparando este resultado con otras series, Van der Werf et al.14 publicaron una reducción del 75% de las AV en la PE en 33 pacientes (similar en nuestra cohorte).
Como se representa en la figura 2, en la familia 1 la flecainida añadida a los bloqueadores beta redujo de manera significativa la FC máxima sin que se modificara la FC de aparición de la primera AV, y esto resultó en una reducción de la ventana arrítmica estadísticamente significativa. La reducción de la FC podría inhibir las despolarizaciones tardías, cuya amplitud está directamente relacionada con la FC20, así como estrechar el tiempo en que el paciente puede sufrir AV y, con ello, disminuir la oportunidad de que puedan producirse AV más graves 6. Sin embargo, aunque este efecto ya se vio en una comparación de nadolol frente a bloqueadores beta 1 selectivos6, no se sabe con exactitud cuál es el mecanismo causal, y es probable que haya otras acciones propias de la flecainida que expliquen esta reducción de arritmias con el esfuerzo.
Leren et al.6 muestran que el nadolol, comparado con los bloqueadores beta 1 selectivos, reduce de modo significativo la FC máxima, la ventana arrítmica y la puntuación de arritmias cualitativa de Van der Werf et al.14 (la misma puntuación cualitativa empleada en nuestro estudio). Aunque no sea posible compararlos porque la metodología es diferente, en la tabla 3 se muestran los valores obtenidos en la serie de Leren et al.6 y en la familia 1.
Resumen de los datos obtenidos en la prueba de esfuerzo de la serie de Leren et al.6 y nuestra cohorte
| Leren et al.6, β1 selectivos* | Leren et al.6, Nadolol* | Familia 1, BB solo | Familia 1, BB + flecainida | |
|---|---|---|---|---|
| FC basal (lpm) | 56 ± 14 | 54 ± 10 | 62 ± 9 | 61 ± 13 |
| FC máxima (lpm) | 139 ± 24 | 122 ± 21 | 144 ± 16 | 128 ± 19 |
| FC EV (lpm) | 113 ± 19 | 113 ± 21 | 124 ± 26 | 122 ± 18 |
| Ventana arrítmica (lpm) | 32 ± 26 | 17 ± 10 | 19 ± 21 | 5 ± 11 |
| Puntuación AV cualitativa | 2,5 ± 0,8 | 1,6 ± 0,9 | 1,6± 1,1 | 1,1 ± 0,5 |
AV: arritmias ventriculares; BB: bloqueadores beta; FC: frecuencia cardiaca; FC EV: FC de aparición de las extrasístoles ventriculares.
Los resultados se presentan como media ± desviación estándar.
Se puede apreciar que en la serie de Leren et al.6 los pacientes con nadolol tienen una puntuación cualitativa y una ventana arrítmica similares a las la familia 1 con bloqueadores beta solos. De los 13 pacientes de la familia 1 analizados, 10 (77%) estaban con propranolol, un bloqueador beta no selectivo, al igual que el nadolol. Posiblemente por este hecho la puntuación es similar. La FC basal en el grupo de Leren et al.6 es más baja, lo que podría deberse a un bloqueo beta de menor grado, aunque no lo parece, o a que los pacientes de la familia 1 portadores de la mutación tuvieran una FC basal mayor que con las otras mutaciones que afectan a este gen, hecho que no ha sido estudiado. Los pacientes de nuestra cohorte tenían la dosis máxima tolerada de bloqueador beta y, de hecho, todos alcanzaron en la PE una FC < 85% de la máxima prevista por edad —7 de ellos (54%), ≤ 80%— lo que refleja un buen grado de bloqueo beta. También se aprecia en nuestra cohorte una FC de aparición de la primera extrasístole ventricular más alta que en la cohorte de Leren et al.6, tanto en el grupo con bloqueadores beta solos como con la flecainida añadida. Esto también podría deberse a que la FC de aparición de la primera extrasístole ventricular fuera mayor en la familia 1, quizá por el tipo de mutación, si bien esto, como ocurre con la FC basal, no ha sido estudiado. Si el nadolol ya disminuye la ventana arrítmica respecto a los bloqueadores beta 1 selectivos, queda demostrado que la combinación de bloqueadores beta, fundamentalmente propranolol y flecainida, la reduce aún más.
Para los pacientes con TVPC, es importante que se intente evitar o reducir las descargas del DAI, tanto apropiadas como inapropiadas, ya que pueden generar más arritmias al incrementar el tono simpático, y ello puede desencadenar una tormenta arrítmica que incluso suponga la muerte10,12. El uso de la flecainida combinada con bloqueadores beta supuso en nuestra serie de pacientes portadores de DAI una reducción del número de descargas y síntomas.
Esto podría ser relevante a la hora de valorar los casos en los que la indicación de implante del DAI sea la persistencia de AV en la PE, ya que podría reducir las indicaciones de DAI y el número de descargas y los síntomas de los pacientes portadores de DAI, evitar los efectos indeseados de las descargas, tanto inapropiadas como apropiadas, y suponer un ahorro de costes y posibles complicaciones.
A diferencia de lo que ocurre en la mayoría de los estudios, no hubo eventos de muerte súbita no recuperada en nuestra cohorte. Esto puede deberse a que es fundamental tener un protocolo diagnóstico uniforme para todas las familias con cribado genético y tratamiento universal con bloqueadores beta, preferiblemente no selectivos, titulados con PE seriadas13.
Alcanzar la dosis máxima de bloqueadores beta puede llevar a que los pacientes incumplan la pauta de tratamiento o lo abandonen. Se estima que aproximadamente el 5% de las muertes súbitas de pacientes con TVPC son de incumplidores del tratamiento17. Hay casos en la literatura en los que se demuestra eficacia clínica y supresión de AV con una dosis alta de flecainida (5mg/kg) y dosis bajas de bloqueadores beta para evitar el efecto secundario de estos y mejorar la adherencia al tratamiento17.
La dosis óptima de flecainida y bloqueadores beta está aún por definir, pero en artículos previos se ha publicado que la flecainida tiene un efecto dosis-respuesta y que dosis de 150-300mg/día son las óptimas para reducir las AV, pues son insuficientes las dosis < 100 mg14. Es importante resaltar que en nuestra serie la dosis media de flecainida necesaria para reducir más de un 50% la puntuación cuantitativa de AV fue de 123,8 mg y la dosis máxima, 200 mg. Por ello se considera apropiado optimizar las dosis de tanto bloqueadores beta como del antiarrítmico con PE seriadas, intentando alcanzar al menos esta dosis.
LimitacionesEl tamaño de la población a la que se añadió la flecainida a los bloqueadores beta o se usó en monoterapia es pequeño. Actualmente hay pocos estudios al respecto, todos retrospectivos y con pocos pacientes14,18, si bien es cierto que está en marcha un ensayo clínico para probar la eficacia de la flecainida en pacientes con TVCP respecto a placebo (clinicalTrials.gov ID NCT01117454).
Para la valoración de las AV, se eligió la PE antes del inicio de la flecainida y la primera tras alcanzar dosis máxima. Las AV de un mismo paciente podían ser diferentes entre las PE de antes de iniciar la flecainida y las realizadas con la dosis máxima de flecainida aunque no se variase nunca la dosis de bloqueadores beta.
Todos los pacientes de nuestra cohorte tienen mutaciones en el gen RyR2, y el análisis de las AV y la ventana arrítmica en las PE antes y después de agegar la flecainida al tratamiento se realizó principalmente en la familia 1, con mutación missense en heterocigosis Gly357Ser. Por ello, se debe tomar con cautela los datos, ya que no son necesariamente extrapolables a pacientes con TVPC y genotipo negativo o con otras mutaciones patogénicas de TVPC. No todas las mutaciones en RyR2 tienen un mismo comportamiento, y se cree que diferentes mutaciones en RyR2 supongan diferentes mecanismos de la enfermedad y conlleven un efecto diferente en la acción de la flecainida21.
Finalmente, el estudio de las familias 2 a 7 se realizó sin seguir un único protocolo de seguimiento y tratamiento.
CONCLUSIONESNuestro estudio demuestra que la flecainida añadida a los bloqueadores beta tiene una buena tolerancia y eficacia, y reduce las AV en el ejercicio, la ventana arrítmica y la FC máxima, los síntomas y las descargas del DAI de los pacientes con TVPC genotipo RyR2 positivo.
FINANCIACIÓNBeca Grupo de Trabajo de DAI: «Tratamiento con flecainida en pacientes con taquicardia ventricular polimórfica catecolaminérgica portadores de DAI».
CONFLICTO DE INTERESESNo se declara ninguno.
- –
Recientemente se ha incorporado a las guías de práctica clínica el uso de la flecainida en el tratamiento de pacientes con TVPC. Se recomienda su uso para pacientes con TVPC que, a pesar de un tratamiento con bloqueadores beta optimizado (o sin bloqueadores beta por intolerancia), persistan sintomáticos, tengan descargas apropiadas e inapropiadas del DAI y sufran AV complejas en las pruebas de esfuerzo (indicación II A–C).
- –
Nuestro estudio demuestra que la flecainida es segura y eficaz en pacientes con TVPC genotipo positivo, y se revela una mayor seguridad frente a estudios previos. Es el primer estudio que analiza la ventana arrítmica y la carga cuantitativa de AV en las PE de pacientes en tratamiento con bloqueadores beta únicamente frente a bloqueadores beta y flecainida. Se objetiva una reducción de las AV, la FC máxima y la ventana arrítmica en las PE y de las descargas apropiadas del DAI reiteradas cuando se combina la flecainida con bloqueadores beta.