El tratamiento y la estratificación del riesgo de los pacientes con fibrilación auricular (FA) y síndromes coronarios agudos son todo un reto. El objetivo es evaluar el impacto pronóstico de la FA, ya sea al ingreso como la aparecida durante la hospitalización por síndrome coronario agudo, así como las tendencias en los tratamientos y el resultado.
MétodosSe analizaron retrospectivamente los datos procedentes de 35.958 pacientes incluidos entre 2004 y 2015 en el registro AMIS Plus.
ResultadosHabía FA preexistente (FApre) en 1.644 pacientes (4,7%), mientras que se evidenció FA de nueva aparición (FAnueva) en 309 (0,8%). La presentación con infarto agudo de miocardio con elevación del segmento ST y la necesidad de asistencia hemodinámica fueron frecuentes en los pacientes con FA, especialmente aquellos con FA nueva. Se observó un cambio en los enfoques médicos e intervencionistas, con un progresivo aumento de la prescripción de anticoagulación oral y las derivaciones para angiografías e intervenciones coronarias percutáneas de pacientes con FApre. A pesar de los diferentes perfiles de riesgo iniciales y presentaciones clínicas, ambos grupos de FA mostraron grandes y comparables mortalidades hospitalaria y a 1 año (FAnueva frente a FApre: mortalidad hospitalaria, OR = 0,79; IC95%, 0,53-1,17; p = 0,246; mortalidad a 1 año, OR = 0,72; IC95%, 0,31-1,67; p = 0,448). La FApre, pero no la FAnueva, predijo de manera independiente la mortalidad hospitalaria. Si bien la mortalidad de aquellos con FApre disminuyó durante el periodo de estudio, se mantuvo estable entre los pacientes con FAnueva.
ConclusionesMientras que la FApre se asocia de manera independiente con la mortalidad hospitalaria, la FA nueva puede reflejar un peor impacto hemodinámico del síndrome coronario agudo, lo que en última instancia determina el pronóstico.
Palabras clave
Tratar a los pacientes con fibrilación auricular (FA) y síndrome coronario agudo (SCA) es un reto debido a la escasez de datos sobre los riesgos hemorrágico y embólico concretos del paciente y sobre el tratamiento antitrombótico apropiado1. A falta de ensayos clínicos aleatorizados especializados, las pruebas disponibles proceden principalmente de análisis de subgrupos de ensayos con stents o con FA, así como de registros. En general, en el contexto del SCA, los pacientes con FA tendrían peor pronóstico y menos acceso a los tratamientos invasivos que los pacientes sin FA2–11. No obstante, sigue siendo tema de debate si la FA tiene una influencia adversa en el pronóstico de SCA per se o es un marcador de que hay comorbilidades, lo cual determinaría los resultados2,5,6,8,9,11.
Aunque en la mayoría de los casos la FA es crónica y no está relacionada con el SCA, a veces los pacientes sufren FA aguda. Los mecanismos fisiopatológicos, la influencia clínica relativa sobre los resultados a corto y largo plazo y el tratamiento de la FA en estas dos circunstancias difieren de manera considerable5,6,8–11. Además, todavía se desconoce si la aparición de FA durante un SCA es un predictor de mortalidad hospitalaria o un marcador de inestabilidad hemodinámica, que es lo que determina el pronóstico.
El objetivo de este estudio es evaluar el impacto diferencial pronóstico de la FA, independientemente de su presencia al ingreso o su aparición durante la hospitalización por SCA, así como tendencias en los tratamientos y resultados en función del momento de aparición de la FA.
MÉTODOSPoblación de pacientesEl Acute Myocardial Infarction in Switzerland (AMIS) Plus es un registro prospectivo de ámbito nacional que desde 1997 incluye a los pacientes ingresados por SCA, con o sin elevación del segmento ST, en más de 80 hospitales12,13. Los pacientes participan de manera voluntaria tras firmar el consentimiento informado por escrito. Los centros participantes proporcionan datos sobre cada paciente a través de un cuestionario estandarizado que consta de 200 preguntas.
La recopilación de los datos está centralizada en el Instituto de Medicina Social y Preventiva de la Universidad de Zúrich. Todos los datos son comprobados por el centro de datos de AMIS Plus en busca de completitud, plausibilidad y consistencia, y se pregunta a los médicos responsables en caso de que los datos estén incompletos. Desde 2010, se lleva a cabo regularmente un control externo en hospitales seleccionados aleatoriamente. El registro fue aprobado por el Swiss Federal Ethics Committee for Clinical Studies, el Swiss Board for Data Security y las respectivas Cantonal Ethics Commissions. El protocolo del estudio se ajusta a las directrices éticas de la Declaración de Helsinki.
En este análisis, se tuvo en cuenta a los pacientes inscritos entre el 1 de enero de 2004 y el 1 de julio de 2015. Se dispuso de los antecedentes clínicos, los tratamientos hospitalarios médicos o quirúrgicos y las complicaciones, y el tratamiento y el estado vital al alta de todos los pacientes. También se proporcionaron datos de los pacientes evaluados por angiografía coronaria. Se calculó el índice de comorbilidad de Charlson, una estimación cuantitativa de las comorbilidades14,15.
Entre todas las complicaciones hospitalarias recopiladas en el registro, las que se tuvieron en cuenta en el presente análisis se definieron como: a) shock cardiogénico: hipotensión persistente (presión arterial sistólica < 90 mmHg) con signos clínicos de reducción grave del índice cardiaco; b) ictus o accidente isquémico transitorio: cualquier evento debido a alteraciones isquémicas, trombóticas o hemorrágicas confirmadas por un neurólogo o técnicas de neuroimagen; c) reinfarto: signos o síntomas clínicos de isquemia con cambios en el electrocardiograma indicativos de nueva isquemia (nuevos cambios en el segmento ST o un nuevo bloqueo de rama izquierda) y un nuevo aumento de los biomarcadores tras el infarto inicial, y d) hemorragias: registradas cuando el médico responsable del paciente las consideró clínicamente relevantes, sin utilizar ningún sistema de clasificación.
En el momento de la primera hospitalización, los pacientes incluidos en el registro pueden autorizar individualmente el seguimiento telefónico a 1 año. En consecuencia, el seguimiento a 1 año del presente estudio refleja los eventos que tuvieron lugar entre el momento del alta hospitalaria y 1 año después en el subgrupo de pacientes que aceptó la visita telefónica de seguimiento.
Para evaluar mejor el impacto clínico y pronóstico de diferentes momentos de aparición de la FA en el SCA, se clasificó a los pacientes en función de cuándo la arritmia se hizo clínicamente evidente. A los pacientes con FA documentada al ingreso se los clasificó como pacientes con FA preexistente (FApre). Así pues, este grupo incluye a pacientes con FA permanente o persistente y aquellos cuya FA apareció antes del ingreso hospitalario. A los pacientes en ritmo sinusal al ingreso que durante la hospitalización sufrieron una FA que persistió hasta el alta se los consideró pacientes con episodios de FA de nueva aparición (FAnueva).
Análisis estadísticoLos datos se presentan como la proporción de casos válidos para variables discretas y como media ± desviación estándar y/o mediana [intervalo intercuartílico] para las variables continuas. Las diferencias relacionadas con las características basales se compararon utilizando la prueba de la t para datos no emparejados o la prueba de la U de Mann-Whitney, en su caso, y la prueba de la χ2 de Pearson. En caso de múltiples comparaciones, se adoptó la corrección de Bonferroni. Los estadísticos de cada tabla se basan en todos los casos con datos válidos en los intervalos especificados para todas las variables de cada tabla.
Se realizaron análisis univariables y multivariables utilizando el análisis de regresión logística con un enfoque gradual para identificar predictores de mortalidad hospitalaria en el conjunto de la población. Los resultados de la regresión logística se presentan como odds ratio (OR) y su intervalo de confianza del 95% (IC95%). Para el análisis de tendencias, se utilizó la prueba lineal de Mantel Haenszel mediante la prueba de la χ2 de asociación lineal con 1 grado de libertad. Se consideró significativo un valor p < 0,05. Para el resto de análisis estadísticos se utilizó el software IBM SPSS Statistics Version 22 (IBM Corp.; Armonk, Nueva York).
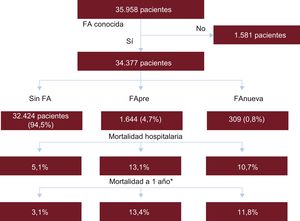
RESULTADOSCaracterísticas de los pacientesEl registro AMIS Plus contaba con 35.958 pacientes ingresados por SCA en el periodo de estudio preestablecido y se dispuso de datos sobre el ritmo cardiaco al ingreso de 34.377. De estos, 1.644 (4,7%) presentaban FA en el momento del ingreso. Sufrieron episodios de FA durante la hospitalización 309 pacientes (0,8%) con ritmo sinusal estable al ingreso. La figura 1 proporciona el flujo de pacientes según la asignación al grupo junto con las mortalidades hospitalaria y a 1 año, mientras que la tabla 1 proporciona las características basales.
Flujo de pacientes según su grupo junto las mortalidades hospitalaria y a 1 año. FA: fibrilación auricular; FAnueva: pacientes con FA de nueva aparición; FApre: pacientes con FA preexistente. *Subgrupos de pacientes en el seguimiento a 1 año. En total, 8.534 no sufrieron FA, 357 tenían FA al ingreso y 68, durante la hospitalización.
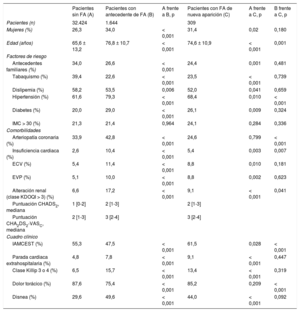
Características clínicas basales
| Pacientes sin FA (A) | Pacientes con antecedente de FA (B) | A frente a B, p | Pacientes con FA de nueva aparición (C) | A frente a C, p | B frente a C, p | |
|---|---|---|---|---|---|---|
| Pacientes (n) | 32.424 | 1.644 | 309 | |||
| Mujeres (%) | 26,3 | 34,0 | < 0,001 | 31,4 | 0,02 | 0,180 |
| Edad (años) | 65,6 ± 13,2 | 76,8 ± 10,7 | < 0,001 | 74,6 ± 10,9 | < 0,001 | 0,001 |
| Factores de riesgo | ||||||
| Antecedentes familiares (%) | 34,0 | 26,6 | < 0,001 | 24,4 | 0,001 | 0,481 |
| Tabaquismo (%) | 39,4 | 22,6 | < 0,001 | 23,5 | < 0,001 | 0,739 |
| Dislipemia (%) | 58,2 | 53,5 | 0,006 | 52,0 | 0,041 | 0,659 |
| Hipertensión (%) | 61,6 | 79,3 | < 0,001 | 68,4 | 0,010 | < 0,001 |
| Diabetes (%) | 20,0 | 29,0 | < 0,001 | 26,1 | 0,009 | 0,324 |
| IMC > 30 (%) | 21,3 | 21,4 | 0,964 | 24,1 | 0,284 | 0,336 |
| Comorbilidades | ||||||
| Arteriopatía coronaria (%) | 33,9 | 42,8 | < 0,001 | 24,6 | 0,799 | < 0,001 |
| Insuficiencia cardiaca (%) | 2,6 | 10,4 | < 0,001 | 5,4 | 0,003 | 0,007 |
| ECV (%) | 5,4 | 11,4 | < 0,001 | 8,8 | 0,010 | 0,181 |
| EVP (%) | 5,1 | 10,0 | < 0,001 | 8,8 | 0,002 | 0,623 |
| Alteración renal (clase KDOQI > 3) (%) | 6,6 | 17,2 | < 0,001 | 9,1 | < 0,001 | 0,041 |
| Puntuación CHADS2, mediana | 1 [0-2] | 2 [1-3] | 2 [1-3] | |||
| Puntuación CHA2DS2-VASC, mediana | 2 [1-3] | 3 [2-4] | 3 [2-4] | |||
| Cuadro clínico | ||||||
| IAMCEST (%) | 55,3 | 47,5 | < 0,001 | 61,5 | 0,028 | < 0,001 |
| Parada cardiaca extrahospitalaria (%) | 4,8 | 7,8 | < 0,001 | 9,1 | < 0,001 | 0,447 |
| Clase Killip 3 o 4 (%) | 6,5 | 15,7 | < 0,001 | 13,4 | < 0,001 | 0,319 |
| Dolor torácico (%) | 87,6 | 75,4 | < 0,001 | 85,2 | 0,209 | < 0,001 |
| Disnea (%) | 29,6 | 49,6 | < 0,001 | 44,0 | < 0,001 | 0,092 |
ECV: enfermedad cerebrovascular; EVP: enfermedad vascular periférica; FA: fibrilación auricular; IAMCEST: infarto de miocardio con elevación del segmento ST; IMC: índice de masa corporal; KDOQI: Kidney Disease Outcomes Quality Initiative.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
Los pacientes con FApre eran mayores y mostraban mayor carga de comorbilidades como hipertensión, diabetes mellitus, arteriopatía coronaria/periférica conocida, insuficiencia cardiaca y enfermedad cerebrovascular que aquellos sin la arritmia. Cabe destacar que los ingresos por infarto agudo de miocardio con elevación del segmento ST (IAMCEST) o dolor torácico típico fueron menos frecuentes, mientras que los cuadros clínicos más graves, como el shock cardiogénico con sobrecarga pulmonar y la parada cardiaca extrahospitalaria, fueron más frecuentes en los pacientes con FApre que en aquellos sin FA.
Los pacientes con FAnueva mostraron algunas peculiaridades que los distinguen de los pacientes sin FA y con FApre. De hecho, aunque eran de más edad que los pacientes sin FA, eran considerablemente más jóvenes que los pacientes con FA conocida y tenían menos comorbilidades. De los 3 grupos, los pacientes con FAnueva mostraron las tasas más altas de IAMCEST (61,5%) y parada cardiaca extrahospitalaria (9,1%).
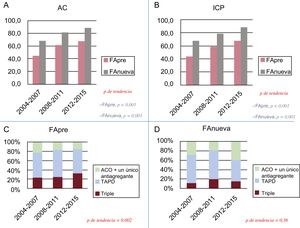
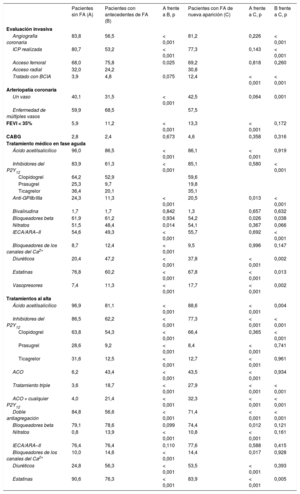
Tratamiento agudoLa tabla 2 proporciona los tratamientos agudos al ingreso hospitalario y el tratamiento al alta de los pacientes en función de su grupo. Los pacientes con FApre se sometieron con menor frecuencia a diagnósticos invasivos e intervenciones coronarias percutáneas (ICP) que aquellos sin FA (angiografías, el 56,5 del grupo con FApre frente al 83,8% del grupo sin FA; p < 0,001; ICP, el 53,2 frente al 80,7%; p < 0,001) (tabla 2). En pacientes con FApre se constató una tendencia hacia un aumento de las derivaciones para angiografía coronaria e ICP entre 2004 y 2015, con un aumento del número de ICP aproximadamente al doble (figuras 2A y B). Cuando se realizaron angiografías, se eligió el acceso transfemoral para 3 de cada 4 pacientes.
Tratamiento agudo hospitalario y tratamientos al alta
| Pacientes sin FA (A) | Pacientes con antecedentes de FA (B) | A frente a B, p | Pacientes con FA de nueva aparición (C) | A frente a C, p | B frente a C, p | |
|---|---|---|---|---|---|---|
| Evaluación invasiva | ||||||
| Angiografía coronaria | 83,8 | 56,5 | < 0,001 | 81,2 | 0,226 | < 0,001 |
| ICP realizada | 80,7 | 53,2 | < 0,001 | 77,3 | 0,143 | < 0,001 |
| Acceso femoral | 68,0 | 75,8 | 0,025 | 69,2 | 0,818 | 0,260 |
| Acceso radial | 32,0 | 24,2 | 30,8 | |||
| Tratado con BCIA | 3,9 | 4,8 | 0,075 | 12,4 | < 0,001 | < 0,001 |
| Arteriopatía coronaria | ||||||
| Un vaso | 40,1 | 31,5 | < 0,001 | 42,5 | 0,064 | 0,001 |
| Enfermedad de múltiples vasos | 59,9 | 68,5 | 57,5 | |||
| FEVI < 35% | 5,9 | 11,2 | < 0,001 | 13,3 | < 0,001 | 0,172 |
| CABG | 2,8 | 2,4 | 0,673 | 4,6 | 0,358 | 0,316 |
| Tratamiento médico en fase aguda | ||||||
| Ácido acetilsalicílico | 96,0 | 86,5 | < 0,001 | 86,1 | < 0,001 | 0,919 |
| Inhibidores del P2Y12 | 83,9 | 61,3 | < 0,001 | 85,1 | 0,580 | < 0,001 |
| Clopidogrel | 64,2 | 52,9 | 59,6 | |||
| Prasugrel | 25,3 | 9,7 | 19,8 | |||
| Ticagrelor | 36,4 | 20,1 | 35,1 | |||
| Anti-GPIIb/IIIa | 24,3 | 11,3 | < 0,001 | 20,5 | 0,013 | < 0,001 |
| Bivalirudina | 1,7 | 1,7 | 0,842 | 1,3 | 0,657 | 0,632 |
| Bloqueadores beta | 61,9 | 61,2 | 0,934 | 54,2 | 0,026 | 0,038 |
| Nitratos | 51,5 | 48,4 | 0,014 | 54,1 | 0,367 | 0,066 |
| IECA/ARA–II | 54,6 | 49,3 | < 0,001 | 55,7 | 0,692 | < 0,001 |
| Bloqueadores de los canales del Ca2+ | 8,7 | 12,4 | < 0,001 | 9,5 | 0,996 | 0,147 |
| Diuréticos | 20,4 | 47,2 | < 0,001 | 37,8 | < 0,001 | 0,002 |
| Estatinas | 76,8 | 60,2 | < 0,001 | 67,8 | < 0,001 | 0,013 |
| Vasopresores | 7,4 | 11,3 | < 0,001 | 17,7 | < 0,001 | 0,002 |
| Tratamientos al alta | ||||||
| Ácido acetilsalicílico | 96,9 | 81,1 | < 0,001 | 88,6 | < 0,001 | 0,004 |
| Inhibidores del P2Y12 | 86,5 | 62,2 | < 0,001 | 77,3 | < 0,001 | < 0,001 |
| Clopidogrel | 63,8 | 54,3 | < 0,001 | 66,4 | 0,365 | < 0,001 |
| Prasugrel | 28,6 | 9,2 | < 0,001 | 8,4 | < 0,001 | 0,741 |
| Ticagrelor | 31,6 | 12,5 | < 0,001 | 12,7 | < 0,001 | 0,961 |
| ACO | 6,2 | 43,4 | < 0,001 | 43,5 | < 0,001 | 0,934 |
| Tratamiento triple | 3,6 | 18,7 | < 0,001 | 27,9 | < 0,001 | < 0,001 |
| ACO + cualquier P2Y12 | 4,0 | 21,4 | < 0,001 | 32,3 | < 0,001 | < 0,001 |
| Doble antiagregación | 84,8 | 56,6 | < 0,001 | 71,4 | < 0,001 | < 0,001 |
| Bloqueadores beta | 79,1 | 78,6 | 0,099 | 74,4 | 0,012 | 0,121 |
| Nitratos | 0,8 | 13,9 | < 0,001 | 10,8 | < 0,001 | 0,161 |
| IECA/ARA–II | 76,4 | 76,4 | 0,110 | 77,6 | 0,588 | 0,415 |
| Bloqueadores de los canales del Ca2+ | 10,0 | 14,6 | < 0,001 | 14,4 | 0,017 | 0,928 |
| Diuréticos | 24,8 | 56,3 | < 0,001 | 53,5 | < 0,001 | 0,393 |
| Estatinas | 90,6 | 76,3 | < 0,001 | 83,9 | < 0,001 | 0,005 |
ACO: anticoagulante oral; anti-GPIIb/IIIa: antagonistas de la glucoproteína IIb/IIIa; ARA–II: antagonsitas del receptor de la angiotensina II; BCIA: balón de contrapulsación intraaórtico; CABG: cirugía de revascularización aortoconaria; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los valores expresan n (%).
A y B: tendencia en la remisión a AC e ICP en función del momento de aparición de la fibrilación auricular. C y D: tendencias en la prescripción de tratamiento triple (ACO + TAPD) o ACO + cualquier antiagregante plaquetario (ACO + un único agente antiagregante plaquetario, ya sea ácido acetilsalicílico o cualquier inhibidor del P2Y12) al alta según el momento de inicio de la FA. AC: angiografía coronaria; ACO: anticoagulante oral; FA: fibrilación auricular; FAnueva: FA de nueva aparición; FApre: FA preexistente; ICP: intervención coronaria percutánea; TAPD: tratamiento antiagregante plaquetario doble.
Para los pacientes con FApre se optó con menos frecuencia por un tratamiento intensivo con ácido acetilsalicílico, inhibidores del P2Y12, antagonistas de la glucoproteína IIb/IIIa, inhibidores del receptor de la enzima de conversión de la angiotensina y bloqueadores beta que para los pacientes sin FA. Al contrario, se prescribieron a menudo vasopresores y tratamiento sintomático con bloqueadores de los canales del Ca2+ y diuréticos.
No se observaron diferencias en cuanto a remisión a diagnósticos invasivos e ICP entre los pacientes con FAnueva y sin FA. Al igual que en los pacientes con FApre, se evidenció una tendencia al aumento de las derivaciones para angiografía coronaria e ICP durante el periodo de estudio. Y en ese caso, el acceso femoral fue el elegido para la mayoría de los pacientes. La asistencia hemodinámica con vasopresores o balón de contrapulsación tuvieron relativa frecuencia en los pacientes con FAnueva, pues fueron necesarios en casi 1 de cada 5. Se evidenció más a menudo disfunción grave del ventrículo izquierdo en los pacientes con FApre (11,2%) y FAnueva (13,3%) que en aquellos sin arritmia (5,9%; ambos grupos con FA frente a sin FA, p < 0,001).
El tratamiento intensivo de los pacientes con FAnueva mediante inhibidores del P2Y12 fue comparable al de aquellos sin FA.
Se prescribió ácido acetilsalicílico a la mayoría de los pacientes, mientras que el tratamiento antiagregante plaquetario doble se prescribió menos a los pacientes con FApre (56,6%) y FAnueva (71,4%) que a aquellos sin FA (ambos, p < 0,001). Sin embargo, se evidenció en los pacientes con FApre un aumento progresivo del tratamiento triple a expensas de la reducción en la administración de un agente antiagregante plaquetario solo + anticoagulación oral, pero no en los pacientes con FAnueva (para las tendencias, p = 0,002 y p = 0,36) (figuras 2C y D).
En ambos subgrupos de FA, se prescribió un anticoagulante oral solo a aproximadamente el 40% de los pacientes (y se dio el alta y se derivó a centros de atención especializada mientras seguían con heparina i.v. o subcutánea a casi una cuarta parte). Tanto la triple terapia (la combinación de ácido acetilsalicílico + un inhibidor del P2Y12 + un anticoagulante oral) como el tratamiento antiagregante plaquetario doble se prescribieron más a menudo a los pacientes con FAnueva que al grupo de FApre (el 27,9 frente al 18,7%; p < 0,001 y el 71,4 frente al 56,6%; p < 0,001). Los bloqueadores beta se utilizaron con menos frecuencia para los pacientes con FA, aunque se prescribieron considerablemente más medicamentos sintomáticos, como nitratos y diuréticos, a los pacientes sin FA.
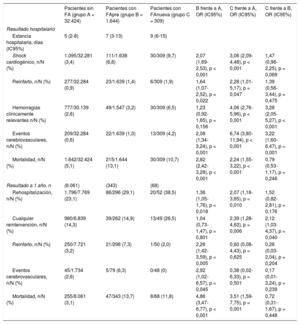
Resultado hospitalarioLa tabla 3da detalles sobre el resultado hospitalario y a 1 año.
Resultados hospitalario y a 1 año
| Pacientes sin FA (grupo A = 32.424) | Pacientes con FApre (grupo B = 1.644) | Pacientes con FAnueva (grupo C = 309) | B frente a A, OR (IC95%) | C frente a A, OR (IC95%) | C frente a B, OR (IC95%) | |
|---|---|---|---|---|---|---|
| Resultado hospitalario | ||||||
| Estancia hospitalaria, días (IC95%) | 5 (2-8) | 7 (3-13) | 9 (6-15) | |||
| Shock cardiogénico, n/N (%) | 1.095/32.281 (3,4) | 111/1.638 (6,8) | 30/309 (9,7) | 2,07 (1,69-2,53), p < 0,001 | 3,06 (2,09-4,48), p < 0,001 | 1,47 (0,96-2,25), p = 0,069 |
| Reinfarto, n/N (%) | 277/32.284 (0,9) | 23/1.639 (1,4) | 6/309 (1,9) | 1,64 (1,07-2,52), p = 0,022 | 2,28 (1,01-5,17), p = 0,047 | 1,39 (0,56-3,44), p = 0,475 |
| Hemorragias clínicamente relevantes n/N (%) | 777/30.139 (2,6) | 49/1.547 (3,2) | 30/309 (6,5) | 1,23 (0,92-1,65), p = 0,156 | 4,06 (2,76-5,96), p < 0,001 | 3,28 (2,05-5,27), p < 0,001 |
| Eventos cerebrovasculares, n/N (%) | 209/32.284 (0,6) | 22/1.639 (1,3) | 13/309 (4,2) | 2,08 (1,34-3,24), p = 0,001 | 6,74 (3,80-11,94), p < 0,001 | 3,22 (1,60-6,47), p = 0,001 |
| Mortalidad, n/N (%) | 1.642/32.424 (5,1) | 215/1.644 (13,1) | 30/309 (10,7) | 2,82 (2,42-3,28), p < 0,001 | 2,24 (1,55-3,22), p < 0,001 | 0,79 (0,53-1,17), p = 0,246 |
| Resultado a 1 año, n | (8.061) | (343) | (68) | |||
| Rehospitalización, n/N (%) | 1.796/7.769 (23,1) | 86/296 (29,1) | 20/52 (38,5) | 1,36 (1,05-1,76), p = 0,018 | 2,07 (1,18-3,65), p = 0,010 | 1,52 (0,82-2,81), p = 0,176 |
| Cualquier reintervención, n/N (%) | 980/6.839 (14,3) | 39/262 (14,9) | 13/49 (26,5) | 1,04 (0,73-1,47), p = 0,801 | 2,39 (1,28-4,62), p = 0,006 | 2,12 (1,03-4,37), p = 0,040 |
| Reinfarto, n/N (%) | 250/7.721 (3,2) | 21/298 (7,3) | 1/50 (2,0) | 2,26 (1,42-3,59), p = 0,005 | 0,60 (0,08-4,43), p = 0,625 | 0,26 (0,03-2,04), p = 0,204 |
| Eventos cerebrovasculares, n/N (%) | 45/1.734 (2,6) | 5/79 (6,3) | 0/48 (0) | 2,92 (1,02-6,57), p = 0,045 | 0,38 (0,02-6,33), p = 0,501 | 0,17 (0,01-3,24), p = 0,239 |
| Mortalidad, n/N (%) | 255/8.061 (3,1) | 47/343 (13,7) | 8/68 (11,8) | 4,86 (3,47-6,77), p < 0,001 | 3,51 (1,59-7,75), p = 0,001 | 0,72 (0,31-1,67), p = 0,448 |
FA: fibrilación auricular; FAnueva: FA de nueva aparición; FApre: FA preexistente; IC95%: intervalo de confianza del 95%; OR: odds ratio.
Los pacientes con FApre tuvieron una estancia hospitalaria más larga ––7 [3–13] frente a 5 [2–8] días (p < 0,001)–– y mostraron mayor incidencia de complicaciones hospitalarias el shock cardiogénico (odds ratio [OR] = 2,07; intervalo de confianza del 95% [IC95%], 1,69-2,53; p < 0,001), reinfarto (OR = 1,64; IC95%, 1,07-2,52; p = 0,022) y eventos cerebrovasculares (OR = 2,08; IC95%, 1,34-3,24; p = 0,001), aunque no se evidenciaron diferencias en las hemorragias clínicamente relevantes (OR = 1,23; IC95%, 0,92-1,65; p = 0,156), en comparación con los pacientes sin FA. La mortalidad hospitalaria sin ajustar también resultó mayor (el 5,1% sin FA frente al 13,1% con FApre; OR = 2,82; IC95%, 2,24-3,28; p < 0,001).
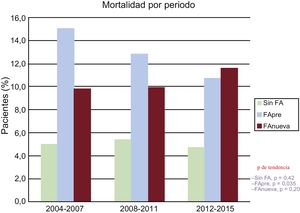
Entre el primero y el último tercio del periodo de estudio analizado (es decir, 2004-2007 y 2015), la mortalidad hospitalaria disminuyó del 15,0 al 10,7% de los pacientes con FApre (p de tendencia = 0,035).
De los 3 grupos, los pacientes con FAnueva mostraron las mayores incidencias de hemorragia hospitalaria y eventos cerebrovasculares. Las mortalidades hospitalarias de ambos grupos de pacientes con FA fueron comparables (FAnueva frente a FApre, OR = 0,79; IC95%, 0,57-1,17; p = 0,246).
Durante todo el periodo de estudio la mortalidad hospitalaria de los pacientes con FAnueva permaneció muy estable (p de tendencia = 0,42). La figura 3 describe las tendencias de la mortalidad hospitalaria según la presencia y el tipo de FA durante el primero, el segundo y el último tercio del periodo de estudio.
Resultado en el seguimientoDe la subpoblación de pacientes programados para el seguimiento a 1 año (n = 8.959, el 24,9% de toda la población), aquellos con FA al ingreso padecieron más rehospitalizaciones por cualquier causa cardiovascular (OR = 1,36; IC95%, 1,07-1,76; p = 0,01), reinfarto (OR = 2,26; IC95%, 1,42-3,59; p = 0,001) y eventos cerebrovasculares (OR = 2,92; IC95%, 1,02-6,57; p = 0,045) que los pacientes sin FA, aunque no se evidenciaron diferencias significativas en lo que respecta a procedimientos invasivos recurrentes como angiografías, ICP, cirugía de revascularización coronaria o implante de marcapasos/desfibrilador implantable (OR = 1,04; IC95%, 0,73-1,47; p = 0,801). La mortalidad a 1 año fue 4 veces mayor en los pacientes con FApre que en aquellos sin FA (el 13,7 frente al 3,1%; OR = 4,86; IC95%, 3,47-6,77; p < 0,001).
En el seguimiento a 1 año, más de 1 de cada 3 pacientes que ya sufrieron episodios de FA durante el ingreso índice requirieron rehospitalización por cualquier causa cardiovascular (frente a sin FA, OR = 2,07; IC95%, 1,18-3,65; p = 0,01) o remisión a procedimientos invasivos (OR = 2,39; IC95%, 1,28-4,62; p = 0,006), aunque las incidencias de eventos isquémicos recurrentes (OR = 0,60; IC95%, 0,08-4,43; p = 0,625) y cerebrovasculares (OR = 0,38; IC95%, 0,02-6,33; p = 0,501) fueron similares a la observada en los pacientes sin FA.
En los pacientes con FAnueva no se evidenciaron ictus en el seguimiento. La mortalidad a 1 año fue del 11,8%, mayor que la observada en los pacientes sin FA (OR = 3,51; IC95%, 1,59-7,75; p = 0,001), pero comparable a la de los pacientes con FApre (OR = 0,72; IC95%, 0,31-1,67; p = 0,625).
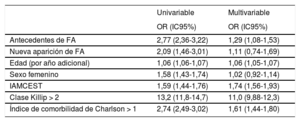
Predictores de resultadoLa tabla 4 muestra los resultados de los análisis univariable y multivariable.
Predictores independientes de la mortalidad hospitalaria de los pacientes con síndrome coronario agudo
| Univariable | Multivariable | |
|---|---|---|
| OR (IC95%) | OR (IC95%) | |
| Antecedentes de FA | 2,77 (2,36-3,22) | 1,29 (1,08-1,53) |
| Nueva aparición de FA | 2,09 (1,46-3,01) | 1,11 (0,74-1,69) |
| Edad (por año adicional) | 1,06 (1,06-1,07) | 1,06 (1,05-1,07) |
| Sexo femenino | 1,58 (1,43-1,74) | 1,02 (0,92-1,14) |
| IAMCEST | 1,59 (1,44-1,76) | 1,74 (1,56-1,93) |
| Clase Killip > 2 | 13,2 (11,8-14,7) | 11,0 (9,88-12,3) |
| Índice de comorbilidad de Charlson > 1 | 2,74 (2,49-3,02) | 1,61 (1,44-1,80) |
FA: fibrilación auricular; IAMCEST: infarto de miocardio con elevación del segmento ST; IC95%: intervalo de confianza del 95%; OR: odds ratio.
Todas las variables mostradas se utilizaron en el modelo ajustado.
Se realizó un análisis multivariable que incluyó antecedentes de FA, episodios intercurrentes de FA, edad, sexo femenino, cuadro clínico de STEMI, clase Killip > 2 al ingreso e índice de comorbilidad de Charlson > 1. Los antecedentes de FA (OR = 1,29; IC95%, 1,08-1,53; p = 0,005), la edad (por año adicional, OR = 1,06; IC95%, 1,05-1,07; p < 0,001), la presentación con IAMCEST (OR = 1,74; IC95%, 1,56-1,93; p < 0,001), la clase Killip > 2 (OR = 11,0; IC95%, 9,88-12,3; p < 0,001) y el índice de comorbilidad de Charlson > 1 (OR = 1,61; IC95%, 1,45-1,80; p < 0,001) resultaron predictores independientes de la mortalidad hospitalaria, mientras que la FAnueva durante la hospitalización no mostró una asociación independiente (OR = 1,02; IC95%, 0,74-1,69; p = 0,614).
DISCUSIÓNEn nuestro conocimiento, este es el mayor registro europeo contemporáneo que evalúe el impacto relativo en la morbilidad y la mortalidad de los pacientes con FA preexistente frente a aquellos con FA de nueva aparición en el contexto de un SCA.
De nuestros datos se extraen las siguientes líneas clave:
- •
A pesar de los distintos perfiles clínicos basales, las mortalidades hospitalaria y a 1 año son grandes y comparables, tanto de los pacientes con FApre como de aquellos con FAnueva.
- •
La FApre es un predictor independiente de la mortalidad hospitalaria, pero no la FAnueva.
- •
La FAnueva, a menudo en relación con IAMCEST, parada cardiaca extrahospitalaria y riesgo de deterioro hemodinámico, es un marcador del peor impacto hemodinámico del SCA.
- •
En los 10 años evaluados, se observa un aumento progresivo de las remisiones a ICP, con una reducción concomitante de la mortalidad de los pacientes con FApre. Por el contrario, la mortalidad de los pacientes con FAnueva se mantuvo muy estable y alta.
Estudios previos han analizado las características clínicas y el impacto pronóstico de la FA conocida y de nueva aparición asociada con un SCA. Los datos derivados de los registros GRACE/CANRACE y Medicare mostraron que la incidencia de FA conocida oscilaba entre el 7,6 y el 22,1% de los pacientes con SCA. Los pacientes con FA eran mayores, con mayor carga de factores de riesgo cardiovascular y enfermedad coronaria, insuficiencia cardiaca y disfunción renal, con menos acceso a los tratamientos basados en la evidencia y una notable mortalidad hospitalaria2,5,10. Además, se enfatiza el paradigma de que la FA preexistente difiere de la FA de reciente aparición en cuanto a presentación, fisiopatología y resultado hospitalario y a largo plazo y se hipotetiza un papel pronóstico de la FA de reciente aparición5.
Nuestros datos proponen una interpretación inclusiva de ambos tipos de FA. Pese a las diferencias en características clínicas y mecanismos fisiopatológicos, las mortalidades hospitalaria y a 1 año observadas en ambos grupos de FA, comparables y altas, unifican las 2 entidades desde una perspectiva de pronóstico. Independientemente de las distintas modalidades y el momento de aparición, en ambos grupos de FA se observaron parecidas mortalidades hospitalarias altas, lo que constituye un marcador de interés clínico.
Hay pruebas contradictorias con respecto a la función relativa de las 2 formas de FA. Mientras algunos autores no dan una importancia clara a la FA preexistente2,5,16,17 como predictor de la mortalidad hospitalaria ––por lo que no atribuyen directamente a la FA el peor resultado hospitalario, sino más bien a factores pronósticos concomitantes, como la edad o un peor estado clínico general en el momento de acudir a urgencias—, otros postulan un efecto causal8,9.
Nuestro análisis muestra que la FApre es un predictor independiente de la mortalidad hospitalaria, pero no la FAnueva. Esta observación subraya la importancia de la arritmia como factor pronóstico en el SCA que considerar junto con las puntuaciones recomendadas para la estimación del riesgo actuales o futuras18,19. Por otro lado, la aparición de nuevos episodios de FA se relacionaba a menudo con presentación de IAMCEST, parada cardiaca extrahospitalaria, deterioro hemodinámico que requiere asistencia mecánica o farmacológica, que resaltan cómo el impacto hemodinámico del SCA desencadena la FA20. Se consideró que esas concomitancias son los factores que llevaban a la ausencia de significación de la FAnueva como predictor de la mortalidad hospitalaria en nuestra población. Sin embargo, independientemente de la ausencia de significación estadística, se mantiene la importancia clínica de los nuevos episodios de FA en el tipo de FA. De hecho, a pesar de la edad más joven y la menor carga de comorbilidades observadas en los pacientes con FAnueva, el impacto hemodinámico del SCA anula su mejor situación general basal y causa un aumento de la morbimortalidad.
El análisis de tendencias insiste claramente en un declive progresivo de la mortalidad hospitalaria de los pacientes con FApre. Esto confirma una tendencia evidente en la literatura, con mortalidades hospitalaria y a 1 año que superaban el 20 y el 40% a mediados de la década de los noventa5, el 15 y el 30% a principios de los dos mil9 y el 10% en series más contemporáneas7,10. Aunque esta tendencia es clara en los pacientes con FApre, la mortalidad de los pacientes con FAnueva se mantuvo estable y alta, lo que refuerza una vez más la importancia clínica de esta entidad.
Además, aunque a partir de nuestros datos no puede extraerse ninguna relación causal, entre el primer y el último año analizados (es decir, 2004 y 2014), la disminución de la mortalidad hospitalaria observada en los pacientes con FApre se reflejó en más remisiones a ICP. Esto constituye una interesante observación generadora de hipótesis, que puede estar relacionada con las recientes mejoras en las herramientas y las técnicas intervencionistas (como la adopción del acceso radial o los stents de tercera generación, que permiten acortar los tratamientos antiagregantes plaquetarios), que además podrían aumentar las ventajas de la revascularización percutánea incluso en los pacientes frágiles.
Además de las implicaciones pronósticas, los médicos tienen que afrontar decisiones terapéuticas difíciles cuando tratan la FA en la fase aguda de un evento isquémico coronario, y tienen que sopesar los riesgos embólico y hemorrágico; estas decisiones a menudo se basan en un consenso de expertos, debido a la falta de confirmaciones basadas en la evidencia1,21,22.
Nuestros datos muestran claramente que se adoptan múltiples tratamientos, que pueden llevar a consecuencias engañosas sobre la morbilidad y la mortalidad. Tanto la infrautilización de tratamientos anticoagulantes/antiagregantes como las revascularizaciones en pacientes con FApre pueden explicar la mayor incidencia de reinfarto y eventos cerebrovasculares observada a 1 año. Además, en el contexto de la FAnueva, se observó una mayor incidencia de hemorragias y eventos cerebrovasculares hospitalarios, probablemente debido a una sobrestimación del riesgo embólico.
También debería fomentarse la adopción de medidas de eficacia probada para reducir las complicaciones hemorrágicas y la mortalidad, tales como el acceso radial23.
Puntos fuertes y limitacionesSe debe mencionar varios puntos fuertes y limitaciones del estudio.
Este análisis, que evalúa la relación entre la FA y el SCA y proviene de los datos del registro nacional suizo, proporciona una visión general occidental y actualizada que permite describir un escenario nacional real y proporcionar pistas para optimizar los tratamientos de referencia actuales. Sin embargo, como investigación observacional no aleatorizada, los datos están sujetos a algunas limitaciones, la falta de datos y la selección de los pacientes, u otros factores de confusión imprevistos. En primer lugar, el gran número de pacientes con FA tanto al ingreso como con episodios intercurrentes es una limitación a la validez externa de las observaciones. Si bien se disponía del estado vital al alta de todo el conjunto de los pacientes inscritos, en lo que al seguimiento se refiere solo se disponía de datos de una gran parte pero no de toda la población, lo que solo permitió publicar una estimación de la morbilidad/mortalidad posteriores al alta. Además, los avances en los tratamientos clínicos/intervencionistas se reflejan en las transformaciones del registro. E incluso en un periodo de observación relativamente corto como este, se han introducido algunas innovaciones importantes, como definiciones estandarizadas de las complicaciones hospitalarias o datos relativos a tratamientos disponibles solo de parte de los pacientes. Por último, el diseño del registro no permitió clasificar a los pacientes según el tipo de FA (paroxística, persistente o crónica) o excluir la posibilidad de que cierto porcentaje de pacientes clasificados como con FAnueva hubieran sufrido el inicio de la arritmia poco antes del ingreso hospitalario, lo que podría estar relacionado con un SCA. De igual modo, no se proporcionaron datos sobre el resultado de alteración del ritmo en el seguimiento.
CONCLUSIONESLos datos confirman que la FA en el contexto del SCA es un problema clínico importante. Tanto los pacientes con antecedentes de FA como aquellos con FA de nueva aparición mostraron complicaciones hospitalarias y un aumento significativo y comparable de las mortalidades hospitalaria y a 1 año. Aunque el antecedente de FA tiene asociación independiente con la mortalidad hospitalaria, los episodios de FA de nueva aparición pueden reflejar un peor impacto hemodinámico del SCA, lo que termina por influir en el pronóstico. A pesar de las diferencias en características clínicas, carga de comorbilidades y mecanismo fisiopatológico y la morbilidad hospitalaria, la FA preexistente y la de nueva aparición comparten una elevada y comparable mortalidad aguda y a largo plazo.
FINANCIACIÓNEl registro AMIS Plus se financia por subvenciones sin restricción procedentes de la Swiss Heart Foundation y Abbot AG, Amgen AG, AstraZeneca AG, Bayer (Schweiz) AG, Biotronik AG, Boston Scientific AG, B. Braun Medical AG, Daiichi-Sankyo /Lilly AG, GE Healthcare AG, Johnson & Johnson AG–Cordis Division, Medtronic AG, A. Menarini AG, Merck Sharp & Dohme AG, Mepha Pharma AG, Novartis Pharma Schweiz AG, Sanofi-Aventis (Schweiz) AG, Servier (Suisse) AG, St. Jude Medical (Schweiz) AG y Vascular Medical GmbH, todos en Suiza. Los patrocinadores no desempeñaron ningún papel en el diseño, la obtención de datos, el análisis o la interpretación del registro.
CONFLICTO DE INTERESESNo se declara ninguno.
- –
En el contexto del SCA, es sabido que los pacientes con FA tienen un peor pronóstico y menos acceso a los tratamientos invasivos. Sin embargo, sigue siendo tema de debate si la FA influye de manera adversa en el pronóstico del SCA per se o si es un marcador de comorbilidad. Además, se discute el impacto relativo de la FA preexistente frente a la de nueva aparición.
- –
Pese a ser intrínsecamente distintas en su fisiopatología, tanto la FA preexistente como la de nueva aparición mostraron elevadas y comparables mortalidades hospitalaria y a 1 año. Aunque la FA preexistente es un predictor independiente de la mortalidad hospitalaria, la FA de nueva aparición, a menudo relacionada con IAMCEST, parada cardiaca extrahospitalaria y riesgo de deterioro hemodinámico, se interpretó como un marcador del peor impacto hemodinámico del SCA.