No se ha estudiado bien la incidencia y los predictores de la reestenosis recurrente tras angioplastia con balón farmacoactivo (BFA) en reestenois de stents farmacoactivos (SFA). Nuestro objetivo es analizar la incidencia y los predictores de la reestenosis recurrente en los estudios aleatorizados en que se utilizaron BFA para el tratamiento de la reestenosis del SFA.
MétodosLos datos clínicos y anatómicos de los pacientes incluidos en 6 estudios aleatorizados sobre BFA para el tratamiento de reestenosis de SFA se analizaron en conjunto. Se asignó a todos los pacientes incluidos en este análisis a tratamiento con el BFA de paclitaxel SeQuent Please (B Braun; Melsungen, Alemania). El análisis se centró en los pacientes que tenían seguimiento angiográfico a los 6-9 meses. Se evaluó tanto la incidencia de reestenosis (definida como estenosis ≥ 50% del diámetro luminal en el análisis por segmento durante el seguimiento angiográfico tardío) como sus predictores clínicos y angiográficos.
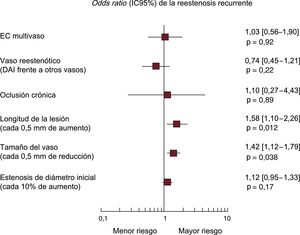
ResultadosLos datos de 546 pacientes se incluyeron en una única base de datos. De 484 pacientes (88,6%), con un total de 518 lesiones tratadas, se disponía de seguimiento angiográfico tardío, y se detectó recurrencia de reestenosis en 101 pacientes (20,8%). En el análisis multivariable, la longitud de la lesión (por cada incremento de 5 mm, OR=1,58; IC95%, 1,10-2,26; p=0,012) y el tamaño del vaso (por cada reducción de 0,5mm, OR=1,42; IC95%, 1,12-1,79; p=0,003) se asociaron de manera independiente con la recurrencia de reestenosis.
ConclusionesEste estudio, el mayor disponible de pacientes tratados con BFA por reestenosis de SFA con seguimiento angiográfico tardío, demuestra que la recurrencia de reestenosis se produce en 1 de cada 5 de estos pacientes. Los predictores de la reestenosis recurrente son la longitud de la lesión y el tamaño del vaso.
Palabras clave
Los stents farmacoactivos (SFA) contemporáneos han reducido notablemente la necesidad de reintervenciones en comparación con los stents metálicos sin recubrimiento y los SFA de primera generación. Sin embargo, la aparición de reestenosis como consecuencia de la proliferación neointimal o la neoateroesclerosis en el interior de los segmentos donde se han implantado stents continúa siendo la principal causa de fallo de los SFA1. Además, el tratamiento óptimo de la reestenosis de los SFA continúa siendo objeto de controversia y se asocia con altas tasas de recurrencia de la reestenosis2.
Para los pacientes con reestenosis de un SFA, la guía europea recomienda el tratamiento con balón farmacoactivo (BFA) o nuevo implante de SFA; las recomendaciones en favor de ambas opciones están respaldadas por un nivel de evidencia similar3. El balón farmacoactivo es una opción de tratamiento atractiva, que aporta eficacia antiproliferativa sin necesidad de implantar un nuevo stent4. Aunque en estudios recientes de pacientes con reestenosis de un SFA se ha considerado que por su potencia antirreestenótica los BFA son el segundo tratamiento más eficaz, después del implante de un nuevo stent liberador de everolimus5, este tratamiento podría ser la opción preferida para los pacientes, ya que preocupan los resultados clínicos tardíos en los pacientes tratados con múltiples capas de stents6.
El seguimiento mediante angiografía es la modalidad de elección para detectar un nuevo estrechamiento luminal tras una intervención coronaria, así como para evaluar la eficacia del dispositivo7. Sin embargo, hasta la fecha, las investigaciones sobre la incidencia y los factores predictivos de la recurrencia de reestenosis tras una angioplastia con BFA por reestenosis de un SFA continúan siendo escasas. Además, la identificación de los factores de riesgo clínicos, angiográficos y de la intervención que predicen el riesgo de reestenosis recurrente en la angiografía de seguimiento pueden aportar fundamento para optimizar el tratamiento o individualizar las estrategias de revascularización de subgrupos específicos de pacientes y lesiones. En esta presentación se evalúan la incidencia y los predictores de reestenosis recurrente en una cohorte de pacientes tratados con angioplastia mediante BFA por una reestenosis en SFA, en el contexto de ensayos controlados y aleatorizados.
MÉTODOSOrigen de los datos y criterios de elegibilidadPara la inclusión en el presente análisis, se identificaron los ensayos aleatorizados del tratamiento con BFA de pacientes con enfermedad coronaria estable o inestable a causa de una reestenosis en SFA, mediante búsqueda en MEDLINE, EMBASE y el Cochrane Central Register of Controlled Trials (CENTRAL) de los resúmenes de congresos científicos y páginas web de interés. No se aplicaron restricciones por lo que respecta al idioma o el tipo de publicación. Se examinaron también las listas de bibliografía de todos los estudios aptos para la inclusión y los metaanálisis previos sobre este tema5,8, con objeto de identificar otras referencias bibliográficas. Los términos de búsqueda incluyeron las palabras clave y los correspondientes Medical Subject Headings para “drug-coated (-eluting) balloon”, “paclitaxel-coated (-eluting) balloon”, “drug-eluting stent(s)”, “restenosis”, “trial” y “randomized trial”. Los criterios de inclusión fueron un diseño aleatorizado y la disponibilidad de datos de angiografía de seguimiento entre 6 y 9 meses después de la intervención de cualificación para el estudio (intervención índice). No se consideraron aptos para la inclusión los estudios sobre angioplastia con BFA por indicaciones distintas de la reestenosis en SFA. La última búsqueda se llevó a cabo el 22 de junio de 2016.
Obtención de los datos de los participantes individuales y evaluación de la calidadDos investigadores (S. Cassese y R.A. Byrne) evaluaron de manera independiente las publicaciones para determinar si eran aptas para el análisis mediante el título o el resumen. Las discrepancias se resolvieron por consenso. Los estudios que cumplían los criterios de inclusión fueron seleccionados para el ulterior análisis. Se evaluó la ausencia de sesgo en cada estudio según el método de la Cochrane Collaboration9. No se asignaron puntuaciones de calidad combinadas10.
De los 8 estudios identificados mediante la búsqueda electrónica, 2 ensayos aleatorizados11 se excluyeron porque el porcentaje total de pacientes tratados mediante angioplastia con BFA por reestenosis en SFA fue < 5%. Finalmente quedaron 6 ensayos aleatorizados12–17 para la inclusión en el presente análisis. Se contactó con los investigadores principales de estos estudios para obtener los datos individuales de los participantes aleatorizados a angioplastia con BFA. Los datos se transfirieron sin los parámetros de identificación de los pacientes al ISAResearch Center (Deutsches Herzzentrum Mu¿nchen, Technische Universität München, Múnich, Alemania) y se combinaron en una única base de datos agrupada. Se verificó que la base de datos final fuera completa y consistente, y se comparó con los resultados de las publicaciones previas. Cuando fueron necesarios datos adicionales, se contactó directamente con los investigadores principales. El análisis de los datos se llevó a cabo aplicando el principio de intención de tratar. Cada uno de los estudios incluidos en el presente análisis fue aprobado por el consejo de revisión interno o el comité de ética de cada centro participante, y todos los pacientes dieron su consentimiento informado por escrito antes de que se les aplicara el tratamiento asignado.
Datos angiográficos y definiciones del estudioLas coronariografías basales, tras la intervención y en el seguimiento se registraron digitalmente y se evaluaron off-line con sistemas automáticos de detección de bordes por evaluadores independientes en todos los estudios12–17. Las características de las lesiones se describieron según definiciones estándares, mientras que la morfología de las reestenosis se clasificó según los criterios modificados por Mehran et al.18.
Los parámetros angiográficos y de la intervención obtenidos para el presente análisis fueron el tamaño del vaso, la longitud de la lesión, el diámetro inicial de la estenosis, la presión máxima del balón, el diámetro luminal final y el diámetro final de la estenosis. Se calculó el cociente balón/vaso mediante el diámetro máximo del balón hinchado dividido por el tamaño del vaso coronario. El porcentaje de estenosis del diámetro se calculó como (1 – diámetro luminal mínimo/diámetro del vaso de referencia) × 100. La reestenosis (angiográfica o binaria), que fue la variable de valoración principal de interés para esta presentación, se definió como una estenosis ≥ 50% del diámetro en el área del segmento afectado (definida como el área tratada con el balón y los segmentos de 5 mm proximal y distal al área tratada).
Síntesis de los datos y análisis estadísticoLos datos de variables discretas se presentan mediante el número y la proporción (porcentaje). Los datos de variables continuas se presentan con la mediana [intervalo intercuartílico] o la media ± desviación estándar, según proceda. Se evaluó la normalidad de la distribución de los datos con la prueba de Kolmogorov-Smirnov. Para los datos de paciente, la significación de las diferencias entre los grupos se evaluó con la prueba de la t de Student o la prueba de Kruskal-Wallis (variables continuas) o con la prueba de la χ2 o la exacta de Fisher si el valor esperado en las celdas era < 5 (variables discretas). Para los datos de lesión, la significación estadística de las diferencias entre los grupos se evaluó con ecuaciones de estimación generalizada (programa R, gee) con objeto de abordar la correlación intraindividual en los pacientes con intervenciones de lesiones múltiples. Según fuera la naturaleza de la variable dependiente, se utilizó la familia gaussiana o la binomial para las variables continuas y discretas respectivamente. Se utilizó la función de vínculo intercambiable. Los predictores de reestenosis recurrente se estudiaron mediante un análisis multivariable. Los datos basales no disponibles se imputaron con la función predictiva de emparejamiento medio (programa R, mice) y la selección de las variables para el modelo multivariable se llevó a cabo con el método de regresión LASSO (Least Absolute Shrinkage and Selection Operator) tras la introducción de todas las características iniciales y de la intervención como parámetros candidatos (programa R, glmnet). Por último, se utilizó un modelo de regresión logística estatificado según el ensayo para la reestenosis recurrente después de introducir también un término de agrupamiento para tener en cuenta la presencia de múltiples lesiones tratadas en el mismo paciente. Como estadísticas de resumen, se utilizaron las odds ratio (OR) ajustadas junto con los intervalos de confianza del 95% (IC95%). Se consideró significativo un valor de p < 0,05. Todos los análisis se realizaron con el programa R (versión 3.3.2, R Foundation for Statistical Computing; Viena, Austria). La presentación de este estudio se atuvo a lo establecido en las normas Preferred Reporting Items for a Systematic Review and Meta-analysis of Individual Participant Data (tabla 1 del material suplementario)19.
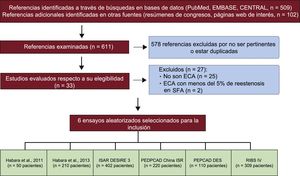
RESULTADOSEn la figura 1 se muestra el diagrama de flujo del proceso de selección de los ensayos, mientras que en la tabla 1 se presentan las principales características de los estudios seleccionados. De manera resumida, se incluyó a los pacientes de 6 ensayos aleatorizados con datos clínicos o instrumentales que indicaran una enfermedad coronaria estable o inestable y una estenosis ≥ 50% del diámetro en un segmento anteriormente tratado con un SFA12–17. El tratamiento con BFA consistió en una angioplastia con balón utilizando un catéter SeQuent Please (B Braun; Melsungen, Alemania). El recubrimiento del BFA estudiado consta del fármaco antirreestenótico paclitaxel a una dosis de 3 μg/mm2 de superficie del balón y medio de contraste (iopromida) como vehículo del fármaco. El tratamiento de comparación fue la angioplastia con balón convencional12–15 o un nuevo implante de SFA15–17. En todos los ensayos excepto uno14, el objetivo principal fueron las medidas angiográficas de la eficacia después de un periodo de 6-9 meses. Es de destacar que los participantes en el ensayo con un objetivo principal clínico fueron el 9,7% de la cohorte total disponible para esta presentación. A todos los pacientes se les administró ácido acetilsalicílico en el momento de la intervención índice y una dosis de carga de inhibidores del receptor de adenosina difosfato plaquetario. La anticoagulación durante las intervenciones coronarias se obtuvo administrando heparina no fraccionada o bivalirudina. En el momento del alta se recomendó tratamiento con ácido acetilsalicílico indefinidamente a todos los participantes, mientras que los inhibidores del receptor de la adenosina difosfato plaquetario se prescribieron durante un periodo de 3-12 meses, según la forma de presentación clínica o los requisitos específicos del protocolo. La evaluación del riesgo de sesgo en los distintos estudios se presenta en la tabla 2 del material suplementario.
Diagrama de flujo del proceso de selección de los ensayos. CENTRAL: Cochrane Central Register of Controlled Trials; ECA: ensayo controlado y aleatorizado; ISAR-DESIRE 3: Randomized Trial of Paclitaxel-Eluting Balloon, Paclitaxel-Eluting Stent and Plain Balloon Angioplasty for Restenosis in “-Limus”-Eluting Coronary Stents; PEPCAD China ISR: A Multicenter, Randomized, Active Controlled Clinical Study to Evaluate the Safety and Efficacy of the Treatment of In-stent Restenosis Lesion by Paclitaxel-eluting PTCA-Balloon Catheter vs Paclitaxel-eluting Stent; PEPCAD DES: Treatment of DES-In-Stent Restenosis With SeQuent Please Paclitaxel Eluting PTCA Catheter; RIBS IV: Restenosis Intrastent of Drug-eluting Stents: Paclitaxel-eluting Balloon vs Everolimus-eluting Stent. A Prospective, Multicenter and Randomized Clinical Trial.
Características principales de los ensayos seleccionados para su inclusión en este estudio
| Ensayo | Periodo de inclusión | Pacientes incluidos (n) | Diseño | Criterios de inclusión principales | Criterios de exclusión principales | Criterio principal de valoración |
|---|---|---|---|---|---|---|
| Habara et al.12 | 2008-2009 | 50 | ECA unicéntrico, a simple ciego, de BFA frente a ABC (relación 1:1) para la reestenosis en SFA | • Edad ≥ 18 años • E C estable • Primera reestenosis en SFA (reestenosis en SLS) • DVR ≥ 2,5 y ≤ 3,5 mm • Longitud de la lesión < 26 mm | • SCA • ERC grave • Implante previo de stent < 6 meses • Reestenosis en SFA que afecta a lesión de ostium, en ACPInp • Lesión en bifurcación • OTC | PLT a los 6 meses |
| Habara et al.14 | 2009-2011 | 210 | ECA multicéntrico, de diseño abierto, de BFA frente a ABC (relación 2:1) para reestenosis en SFA o SMSR | • Edad > 20 años • EC estable o inestable • Reestenosis de lesión única en SMSR o SFA (reestenosis en SLE, SLS, SLZ) o ≤ 2 lesiones reestenóticas en diferentes vasos sanguíneos • DVR ≥ 2,0 y ≤ 4,0 mm • Longitud de la lesión ≤ 22 mm | • FEVI < 30% • IAM < 72 h •E RC • Cualquier ICP < 28 días • ICP con SFA < 6 meses • Cualquier ACV < 6 meses • Intolerancia a fármacos antiagregantes plaquetarios, anticoagulantes, paclitaxel o medios de contraste • Embarazo o posibilidad de embarazo • Enfermedades graves con esperanza de vida < 12 meses • Estenosis de ACPInp > 50% del diámetro • Lesión tortuosa (ángulo > 90°) • Lesiones múltiples en el vaso diana • OTC, lesión intensamente calcificada, reestenosis en SFA que afecta a injerto de bypass o a bifurcación con DVR de rama lateral > 2,0 mm | FVD (muerte cardiaca relacionada con el vaso diana, IM o RVD) |
| ISAR-DESIRE 315 | 2009-2011 | 402 | ECA multicéntrico, de diseño abierto, de BFA frente a SLP frente a ABC (relación 1:1:1) para la reestenosis en SFA | • Edad > 18 años • EC estable o inestable • Reestenosis en SFA > 50% del diámetro (reestenosis de SLB, SLE, SLS, SLZ) | • IAMCEST < 48 h • Shock cardiogénico • ERC grave • Enfermedades graves con una esperanza de vida < 12 meses o que pudieran implicar falta de cumplimiento del protocolo • Contraindicaciones o alergias conocidas al tratamiento antiagregante plaquetario o el placebo, embarazo y posible embarazo • Reestenosis en SFA que afecta a ACPInp o a injerto de bypass | Estenosis del diámetro a los 6-8 meses |
| PEPCAD China ISR16 | 2011-2012 | 220 | ECA unicéntrico, a simple ciego, de BFA frente a SLP (relación 1:1) para la reestenosis en SFA | • Edad ≥ 18 a ≤ 80 años • EC estable o inestable • Reestenosis en SFA de > 50% a ≤ 70% del diámetro (reestenosis de SLE, SLS, SLP) • Clase de RES de Mehran I-III • DVR ≥ 2,5 y ≤ 4,0 mm • Longitud de la lesión ≤ 30 mm | • IAM < 1 semana • Insuficiencia cardiaca en NYHA IV • Valvulopatía cardiaca grave • ACV < 6 meses • ERC grave • Reestenosis en SFA que afecta a bifurcación con DVR > 2,5 mm de rama lateral • Trombo en vaso diana | PLT a los 9 meses |
| PEPCAD DES13 | 2009-2011 | 110 | ECA multicéntrico, a simple ciego, de BFA frente a ABC (relación 2:1) para la reestenosis en SFA | • Reestenosis en SFA (reestenosis de SLE, SLS, SLP) • DVR ≥ 2,5 y ≤ 3,5 mm • Longitud de la lesión < 22 mm | • Intervención quirúrgica prevista en los siguientes 6 meses • Contraindicación para el tratamiento antiagregante plaquetario • Trombo en vaso diana • Reestenosis en SFA que afecta a ACPInp o a injerto de bypass • Lesión en bifurcación • Lesión en ostium • Lesiones múltiples en el vaso diana • OTC | PLT a los 6 meses |
| RIBS IV17 | 2010-2013 | 309 | ECA multicéntrico, de diseño abierto, de BFA frente a SLE (relación 1:1) para la reestenosis en SFA | • EC estable o inestable • Reestenosis en SFA >50% del diámetro • DVR>2,0 mm • Longitud de la lesión ≤ 30 mm | • OTC • Reestenosis en SFA < 1 mes • IAM • Trombo en vaso diana • Enfermedad vascular periférica grave • Enfermedades graves con una esperanza de vida < 12 meses o que pudieran implicar falta de cumplimiento del protocolo • Contraindicaciones para el tratamiento antiagregante plaquetario | DLM a los 6-9 meses |
ABC: angioplastia con balón clásica; ACPInp: arteria coronaria principal izquierda no protegida; ACV: accidente cerebrovascular; BFA: balón farmacoactivo; DLM: diámetro luminal mínimo; DVR: diámetro del vaso de referencia; EC: enfermedad coronaria; ECA: ensayo controlado aleatorizado; ERC: enfermedad renal crónica; FEVI: fracción de eyección del ventrículo izquierdo; FVD: fallo del vaso diana; IAM: infarto agudo de miocardio; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; IM: infarto de miocardio; ISAR-DESIRE 3: Randomized Trial of Paclitaxel-Eluting Balloon, Paclitaxel-Eluting Stent and Plain Balloon Angioplasty for Restenosis in “-Limus”-Eluting Coronary Stents; NYHA: New York Heart Association; OTC: oclusión total crónica; PEPCAD China ISR: A Multicenter, Randomized, Active Controlled Clinical Study to Evaluate the Safety and Efficacy of the Treatment of In-stent Restenosis Lesion by Paclitaxel-eluting PTCA-Balloon Catheter vs Paclitaxel-eluting Stent; PEPCAD DES: Treatment of DES-In-Stent Restenosis With SeQuent Please Paclitaxel Eluting PTCA Catheter; PLT: pérdida luminal tardía; RES: reestenosis en el stent; RIBS IV: Restenosis Intrastent of Drug-eluting Stents: Paclitaxel-eluting Balloon vs Everolimus-eluting Stent. A Prospective, Multicenter and Randomized Clinical Trial; RVD: revascularización del vaso diana; SCA: síndrome coronario agudo; SFA: stent farmacoactivo; SLB: stent liberador de biolimus; SLE: stent liberador de everolimus; SLP: stent liberador de paclitaxel; SLS: stent liberador de sirolimus; SLZ: stent liberador de zotarolimus; SMSR: stent metálico sin recubrimiento.
En los ensayos seleccionados12–17, se asignó a un total de 546 individuos con 588 lesiones al tratamiento con BFA a causa de reestenosis del SFA. En la tabla 3 del material suplementario, se muestran las características principales de los pacientes aleatorizados a angioplastia con BFA en cada uno de los ensayos. De un total de 484 individuos (88,6%) con 518 lesiones tratadas, se dispuso de revisión angiográfica una mediana de 202 [180-275] días tras la intervención índice. En ese momento, se observó reestenosis recurrente en 101 pacientes (20,8%) con 103 lesiones tratadas. El diagrama de flujo del estudio se presenta en la figura del material suplementario.
No se realizó una angiografía de seguimiento a un total de 62 pacientes, que eran de una edad ligeramente mayor (62,2 [58,0-68,0] frente a 59,0 [52,1-67,5] años; p = 0,09), con mayor probabilidad de tener diagnóstico de diabetes (el 58,1 frente al 43,0%; p = 0,02) y similares tasas de infarto de miocardio previo (el 43,5 frente al 46,9%; p = 0,62) que los pacientes con angiografía de seguimiento disponible. De los 62 pacientes, 4 fallecieron antes de la angiografía programada.
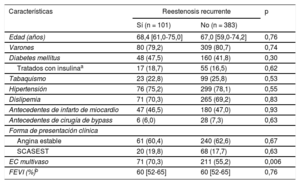
Análisis univariableLas características clínicas iniciales de los pacientes con y sin reestenosis recurrente en la angiografía de seguimiento se muestran en la tabla 2. Las proporciones de pacientes con diabetes mellitus y con antecedentes de infarto de miocardio se aproximaban al 50% y fueron comparables en los 2 grupos. En ambos grupos, la mayor parte de los pacientes referían angina estable en el momento de la intervención índice. La presencia de enfermedad coronaria multivaso fue más probable en los pacientes con estenosis recurrente que en los que no la presentaban.
Características clínicas basales de los pacientes con angiografía de seguimiento disponible tras una angioplastia con balón farmacoactivo por reestenosis en stent farmacoactivo
| Características | Reestenosis recurrente | p | |
|---|---|---|---|
| Sí (n = 101) | No (n = 383) | ||
| Edad (años) | 68,4 [61,0-75,0] | 67,0 [59,0-74,2] | 0,76 |
| Varones | 80 (79,2) | 309 (80,7) | 0,74 |
| Diabetes mellitus | 48 (47,5) | 160 (41,8) | 0,30 |
| Tratados con insulinaa | 17 (18,7) | 55 (16,5) | 0,62 |
| Tabaquismo | 23 (22,8) | 99 (25,8) | 0,53 |
| Hipertensión | 76 (75,2) | 299 (78,1) | 0,55 |
| Dislipemia | 71 (70,3) | 265 (69,2) | 0,83 |
| Antecedentes de infarto de miocardio | 47 (46,5) | 180 (47,0) | 0,93 |
| Antecedentes de cirugía de bypass | 6 (6,0) | 28 (7,3) | 0,63 |
| Forma de presentación clínica | |||
| Angina estable | 61 (60,4) | 240 (62,6) | 0,67 |
| SCASEST | 20 (19,8) | 68 (17,7) | 0,63 |
| EC multivaso | 71 (70,3) | 211 (55,2) | 0,006 |
| FEVI (%)b | 60 [52-65] | 60 [52-65] | 0,76 |
EC: enfermedad coronaria; FEVI: fracción de eyección del ventrículo izquierdo; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
Los valores expresan mediana [intervalo intercuartílico] o n (%) de pacientes.
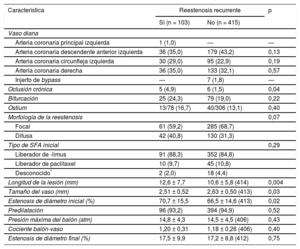
Las características basales angiográficas y de la intervención correspondientes a las lesiones con y sin reestenosis recurrente se muestran en la tabla 3. El tratamiento de las oclusiones crónicas, las lesiones largas, los vasos de pequeño tamaño y el mayor grado de estenosis inicial fueron más probables en los pacientes con estenosis recurrentes que en aquellos sin ella. Hubo una proporción numéricamente superior de reestenosis de patrón difuso en las lesiones con reestenosis recurrentes en la angiografía de seguimiento en comparación con las que no las tenían. Es de destacar que, en ambos grupos, más de 4 de los 5 stents con reestenosis eran liberadores de sirolimus o sus análogos.
Características angiográficas y de la intervención de los pacientes con angiografía de seguimiento disponible tras una angioplastia con balón farmacoactivo por reestenosis en stent farmacoactivo
| Característica | Reestenosis recurrente | p | |
|---|---|---|---|
| Sí (n = 103) | No (n = 415) | ||
| Vaso diana | |||
| Arteria coronaria principal izquierda | 1 (1,0) | — | — |
| Arteria coronaria descendente anterior izquierda | 36 (35,0) | 179 (43,2) | 0,13 |
| Arteria coronaria circunfleja izquierda | 30 (29,0) | 95 (22,9) | 0,19 |
| Arteria coronaria derecha | 36 (35,0) | 133 (32,1) | 0,57 |
| Injerto de bypass | — | 7 (1,8) | — |
| Oclusión crónica | 5 (4,9) | 6 (1,5) | 0,04 |
| Bifurcación | 25 (24,3) | 79 (19,0) | 0,22 |
| Ostium | 13/78 (16,7) | 40/306 (13,1) | 0,40 |
| Morfología de la reestenosis | 0,07 | ||
| Focal | 61 (59,2) | 285 (68,7) | |
| Difusa | 42 (40,8) | 130 (31,3) | |
| Tipo de SFA inicial | 0,29 | ||
| Liberador de -limus | 91 (88,3) | 352 (84,8) | |
| Liberador de paclitaxel | 10 (9,7) | 45 (10,8) | |
| Desconocido* | 2 (2,0) | 18 (4,4) | |
| Longitud de la lesión (mm) | 12,6 ± 7,7 | 10,6 ± 5,8 (414) | 0,004 |
| Tamaño del vaso (mm) | 2,51 ± 0,52 | 2,63 ± 0,50 (413) | 0,03 |
| Estenosis de diámetro inicial (%) | 70,7 ± 15,5 | 66,5 ± 14,6 (413) | 0,02 |
| Predilatación | 96 (93,2) | 394 (94,9) | 0,52 |
| Presión máxima del balón (atm) | 14,8 ± 4,3 | 14,5 ± 4,5 (406) | 0,43 |
| Cociente balón-vaso | 1,20 ± 0,31 | 1,18 ± 0,26 (406) | 0,40 |
| Estenosis de diámetro final (%) | 17,5 ± 9,9 | 17,2 ± 8,8 (412) | 0,75 |
SFA: stent farmacoactivo.
Los valores expresan media ± desviación estándar o n (%) de lesiones. Se indican los denominadores cuando difieren del número total de lesiones.
En la figura 2 se muestra el gráfico de valores de OR para las variables introducidas en el modelo final. La mayor longitud de la lesión (cada 5 mm de aumento, OR = 1,58; IC95%, 1,10-2,26; p = 0,012) y el menor tamaño del vaso (cada 0,5 mm de reducción, OR = 1,42; IC95%, 1,12-1,79; p = 0,003) mostraron asociación independiente con una mayor probabilidad de reestenosis recurrente.
Análisis multivariable de la reestenosis recurrente en pacientes tratados con angioplastia con balón farmacoactivo por reestenosis en un stent farmacoactivo. Gráficos de los valores de odds ratio asociados con la reestenosis recurrente estratificados según el ensayo. Los cuadrados indican la estimación puntual y los extremos izquierdo y derecho de las líneas corresponden al IC95%. DAI: arteria coronaria descendente anterior izquierda; EC: enfermedad coronaria; IC95%: intervalo de confianza del 95%.
En el presente análisis, se ha estudian la incidencia y los predictores de la reestenosis recurrente en la angiografía de seguimiento en 546 individuos tratados con angioplastia con BFA por una reestenosis en SFA en 6 ensayos aleatorizados. El conjunto de datos analizados constituye la población más amplia con angiografías de seguimiento tras una angioplastia con BFA por una reestenosis en SFA que se haya estudiado hasta ahora. Los principales resultados son los siguientes: a) la reestenosis recurrente después de una angioplastia con BFA por reestenosis en SFA se produce en aproximadamente 1 de cada 5 pacientes; b) la mayor longitud de la lesión y el menor tamaño del vaso son predictores de la reestenosis recurrente.
La iteración continua del tratamiento con SFA ha ampliado las indicaciones de las intervenciones percutáneas para poblaciones de pacientes y lesiones de una complejidad creciente1. En consecuencia, dado que las tasas de fallos del stent pueden considerarse una función que depende de la complejidad de la enfermedad20, el número absoluto de pacientes que presentan reestenosis en SFA continúa siendo considerable en cifras absolutas y se prevé que aumente en los próximos años. Dado que la angioplastia con BFA es una de las opciones más eficaces para los pacientes con reestenosis en un SFA5, es importante realizar estudios sobre la reestenosis recurrente en este contexto.
En este estudio se investigó la base de datos más amplia de pacientes aleatorizados en ensayos clínicos controlados a angioplastia con BFA por reestenosis en SFA. Es de destacar que las características basales son comparables con las de los individuos con reestenosis en SFA tratados con un BFA en la práctica clínica habitual21,22. Se observó que la reestenosis angiográfica binaria recurrente se da en casi un 21% de los pacientes. En términos generales, estos resultados son coherentes con los de los ensayos clínicos individuales y respaldan que el BFA es el segundo tratamiento más eficaz para la reestenosis en un SFA después del implante de un nuevo stent liberador de everolimus, el cual se ha asociado con una incidencia de reestenosis recurrente de hasta un 11,3%23.
En este análisis, las lesiones largas fueron un potente predictor de reestenosis recurrente tras angioplastia con BFA por reestenosis en un SFA. Concretamente, se observa un riesgo de recurrencia un 58% superior con cada aumento de 5 mm en la longitud de la lesión. El contacto adecuado de la suficiente concentración del fármaco con el tejido reestenótico subyacente es requisito para la eficacia del tratamiento con BFA4. A este respecto, un mayor desplazamiento de partículas del fármaco de los catéteres con balón al torrente circulatorio durante la aplicación del balón en segmentos reestenóticos largos puede contribuir a que se reduzca la eficacia del BFA en este contexto24. Además, otros factores asociados con una mala evolución, como la infraexpansión del stent, son más frecuentes cuando el implante de stents se hace en segmentos largos25 y es probable que causen un deterioro de la transferencia efectiva del fármaco a la pared del vaso.
Las arterias coronarias de pequeño calibre continúan siendo el factor que muestra una mayor correlación con la reestenosis, independientemente del tipo de tratamiento percutáneo26. Intuitivamente, en un paciente individual, a determinado grado de sobrecrecimiento de neoíntima tras la intervención, la probabilidad de que la estenosis resultante supere el 50% del diámetro está en función del tamaño del vaso y de la estenosis residual tras la intervención. En este análisis se describe un riesgo de reestenosis recurrente un 42% superior por cada 0,5 mm de reducción del diámetro del vaso de referencia. Por un lado, el BFA es una opción de tratamiento atractiva para los pacientes con reestenosis en un SFA en vasos coronarios pequeños, al aplicar un tratamiento antiproliferativo mediante una plataforma que no se basa en un stent, lo cual evita la reducción mecánica de la luz vascular como consecuencia de una capa adicional de metal. Por otro lado, la eficacia antirreestenótica superior de los tratamientos alternativos, es decir, las plataformas contemporáneas de stents de alto rendimiento, como los stents liberadores de everolimus, pueden ser de especial importancia en los pacientes con reestenosis en un SFA en vasos coronarios pequeños26.
Tiene interés señalar que, en nuestro análisis, el tipo de SFA subyacente no fue un predictor independiente de reestenosis recurrente tras la angioplastia con BFA por reestenosis en un SFA. Aunque esta observación se basó en un pequeño número de pacientes, es coherente con los datos presentados en estudios previos27. Los catéteres con BFA comercializados actualmente utilizan solo el derivado taxólico paclitaxel como fármaco antirreestenótico4. Aunque la influencia de la resistencia farmacológica en la eficacia del BFA en pacientes con reestenosis en un SFA tiene interés científico, los stents liberadores de paclitaxel han dejado de utilizarse en la práctica clínica, y los BFA basados en fármacos de tipo-limus se encuentran aún en la fase de desarrollo28. A este respecto, no se ha abordado aún si el continuo desarrollo de nuevos catéteres con BFA (basados en el empleo de paclitaxel y de fármacos -limus), la sinergia de diferentes tecnologías (catéteres con balón de corte/rayado para la predilatación antes de la angioplastia con BFA) y un uso más liberal de las técnicas de imagen intravascular para optimizar la preparación de la lesión permitirán reducir el riesgo de recurrencia tras la angioplastia con BFA por reestenosis en SFA.
LimitacionesEl presente análisis tiene algunas limitaciones. Primero, corresponde únicamente a pacientes con una reestenosis en SFA, y no se puede extrapolar la incidencia y los predictores de la recurrencia tras la angioplastia con BFA observados en este estudio a la reestenosis de stents metálicos sin recubrimiento. Segundo, la tasa de reestenosis recurrente tras la angioplastia con BFA por reestenosis en un SFA en un momento de valoración distinto del de 6-9 meses continúa sin estar bien estudiada y los predictores identificados en este artículo pueden no ser aplicables a los pacientes con reestenosis recurrente en otro momento. Tercero, la validación de la reestenosis se basó en el porcentaje de diámetro del reestrechamiento de la luz en la angiografía de seguimiento. No se evaluó la asociación entre otros factores específicos de la lesión (como la caracterización del tejido reestenótico) y los resultados angiográficos posteriores. Cuarto, debe señalarse que este estudio se basó en un conjunto de pacientes y lesiones bien seleccionados. A este respecto, la tasa de recurrencias observada en el presente análisis debe interpretarse con precaución y no es generalizable a subgrupos de pacientes de mayor riesgo. Quinto, los ensayos originales incluidos en este informe no evaluaron de manera sistemática la carga isquémica de los pacientes con reestenosis recurrentes a los 6 y 9 meses; en este sentido, la importancia clínica de los resultados angiográficos no se puede evaluar en este contexto. Por último, a todos los pacientes incluidos en el presente análisis se los trató mediante angioplastia con BFA utilizando un único catéter con balón. Aunque este aspecto elimina una fuente importante de variabilidad, la evidencia no respalda un efecto de clase para las plataformas de BFA4. A este respecto, los datos angiográficos observados en este análisis no deben extrapolarse a otros dispositivos de BFA.
CONCLUSIONESEn la cohorte más amplia de pacientes con revisión angiográfica tras la angioplastia con BFA por reestenosis en un SFA, la recurrencia tuvo lugar en aproximadamente 1 de cada 5 pacientes. Los predictores independientes de reestenosis recurrente fueron la mayor longitud de la lesión y el menor tamaño del vaso.
- –
La aparición de una reestenosis en segmentos tratados con stents continúa siendo la principal causa de fallos tras el tratamiento con los SFA contemporáneos.
- –
El balón farmacoactivo es una opción terapéutica atractiva, puesto que aporta eficacia antiproliferativa sin necesidad de un stent adicional.
- –
No obstante, el tratamiento de la reestenosis en SFA continúa asociándose con altas tasas de recurrencia.
- –
En este análisis conjunto de los datos de participantes individuales de 6 ensayos controlados y aleatorizados sobre la angioplastia con BFA por reestenosis en SFA, se demuestra que la reestenosis recurrente en la angiografía de seguimiento se da en aproximadamente 1 de cada 5 pacientes.
- –
Los predictores de la reestenosis recurrente son la mayor longitud de la lesión y el menor tamaño del vaso.
- –
El conocimiento de la incidencia y los predictores de la reestenosis recurrente tras una angioplastia con balón farmacoactivo por reestenosis en un SFA puede ser la base para optimizar el tratamiento o individualizar las estrategias de revascularización para subgrupos específicos de pacientes y de lesiones.
A. Kastrati declara solicitudes de patentes relacionadas con tecnologías de stents farmacoactivos. R.A. Byrne declara recibir pagos por conferencias de B. Braun Melsungen AG, Biotronik y Boston Scientific y apoyo científico de Boston Scientific y Heartflow. M. Waliszewski es empleado a tiempo completo del Medical Scientific Affairs Department de B. Braun Melsungen AG.