Desde junio de 2009 se ha implantado en Cataluña el Código Infarto, mediante el cual se plantea a los pacientes con infarto agudo de miocardio con elevación del ST en las primeras 12 h de evolución la realización de angioplastia primaria. El objetivo es describir el impacto de aplicar el Código Infarto a los pacientes atendidos en nuestro centro en cuanto a volumen, tiempos de actuación y perfil clínico en comparación con el periodo previo.
MétodosRegistro prospectivo de pacientes sometidos a angioplastia primaria en nuestro centro. Análisis de características clínicas, tiempos de actuación y mortalidad en el seguimiento de la fase de aplicación del Código Infarto (junio de 2009-mayo de 2010) y comparación con el año previo (junio de 2008-mayo de 2009).
ResultadosEn el periodo del Código Infarto se incluyó a 514 pacientes (241 el año previo). Edad, factores de riesgo, extensión de la enfermedad coronaria, infarto anterior y características del procedimiento fueron similares en los dos grupos. Se observó una disminución del tiempo desde el primer contacto médico a la apertura de la arteria (120 frente a 88 min; p<0,001). Se detectó una tendencia a una menor gravedad de los pacientes en la fase Código Infarto (Killip III, angioplastia de rescate). En el análisis multivariable, la mortalidad a 1 año se relacionó con el infarto anterior, la clase Killip ≥ III, la edad y la enfermedad multivaso.
ConclusionesLa implantación del Código Infarto ha aumentado el número de pacientes tratados mediante angioplastia primaria, con una reducción en los tiempos de actuación y una mejora en el perfil clínico a su llegada.
Palabras clave
La angioplastia primaria (AP) es el tratamiento de primera elección en el infarto agudo de miocardio con elevación del ST (IAMCEST)1, 2, 3. Esta recomendación se basa en asegurar un tiempo entre el primer contacto médico y la apertura de la arteria<120 min, quedando como segunda opción el tratamiento fibrinolítico4. El beneficio de la AP sobre la fibrinolisis reside, además de en la mayor eficacia intrínseca de la AP en restablecer el flujo en la arteria, en la rapidez con que se realiza5, 6. Por ello, el tiempo de actuación desde el momento en que el paciente llega a la atención médica hasta la apertura de la arteria es un factor crucial para determinar la eficacia del procedimiento y los resultados7. En varios registros se ha demostrado que tiempos de actuación cortos se asocian a mejores resultados en cuanto a mortalidad8, 9. Por lo tanto, la realización sistemática de AP tiene que acompañarse de un sistema que garantice diagnóstico rápido y traslado inmediato para realizar la AP. En Europa y España hay varios ejemplos de programas de asistencia en el IAMCEST, fundados en la integración entre un sistema de selección (triage) centralizado y una red de hospitales de referencia que ofrecen tratamiento de reperfusión y hospitales comarcales según el modelo organizativo centro-periferia (hub and spoke)10, 11. La implantación de estos programas ha permitido mayor difusión de la reperfusión en la fase aguda del infarto y un claro beneficio en los resultados clínicos12, 13.
El 1 de junio de 2009 se implantó en Cataluña una red asistencial integrada para realización sistemática de AP, denominada Código Infarto. El objetivo del estudio es detectar las modificaciones que la implantación del Código Infarto ha producido entre los pacientes con IAMCEST tratados con angioplastia en las primeras 12 h del infarto en cuanto a número de pacientes atendidos, tiempos de actuación y perfil clínico a su llegada. Asimismo se describe la evolución a 1 año de seguimiento.
MétodosSe ha llevado a cabo un estudio retrospectivo a partir de un registro prospectivo que incluyó a todos los pacientes consecutivos remitidos a nuestro centro para reperfusión mediante AP o angioplastia de rescate, con diagnóstico de IAMCEST: dolor torácico típico y elevación persistente del segmento ST o bloqueo de rama izquierda de nueva aparición2.
Se diseñó una base de datos única para recoger los datos iniciales y del procedimiento en el laboratorio de hemodinámica y después rellenar la evolución clínica en la unidad coronaria.
El estudio consta de dos periodos de 1 año cada uno: fase PreCódigo (1 de junio de 2008 a 31 de mayo de 2009) y fase Código Infarto (1 de junio de 2009 a 31 de mayo de 2010).
Fase PreCódigoDurante este periodo se realizaba tratamiento de reperfusión percutánea mediante AP a:
• Todos los pacientes que acudían al servicio de urgencias de nuestro hospital.
• Los pacientes trasladados por los servicio de emergencias médicas (SEM) desde el domicilio o desde los centros de atención primaria.
• Los pacientes con contraindicaciones para la trombolisis procedentes desde otros hospitales.
Los pacientes tratados con trombolisis en otros centros, ante la falta de criterios de reperfusión a los 90 min de administrar el tratamiento fibrinolítico, eran trasladados a nuestro centro para angioplastia de rescate. En todos los casos el paciente era valorado directamente por el equipo de guardia de cardiología de nuestro centro, que decidía la indicación de reperfusión y contactaba con la unidad de cardiología intervencionista para la realización del procedimiento. En la fase PreCódigo el área geográfica de procedencia de los pacientes era la misma que en la fase Código Infarto. La diferencia radica en que no había una actuación protocolizada ante un diagnóstico de IAMCEST: no existía una estrategia estandarizada de priorización del traslado ni sistemáticamente un contacto previo entre el SEM y el cardiólogo de guardia.
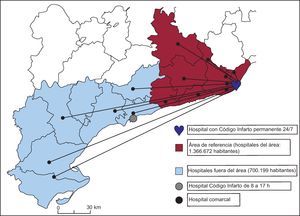
Funcionamiento del Código InfartoSe implantó en Cataluña el 1 de junio de 2009 con el objetivo de ofrecer tratamiento mediante AP a todo paciente diagnosticado de IAMCEST y garantizar un acortamiento de los tiempos entre la demanda de atención y la apertura de la arteria. La comunidad autónoma se dividió en áreas de referencia según criterios de sectorización territorial. El área de referencia de nuestro centro (Figura 1)14 incluye seis comarcas de las provincias de Barcelona y Tarragona14 que integran ocho centros hospitalarios (hospitales del área). En horario extralaboral (lunes a viernes desde las 17.00, sábados y festivos), nuestro centro es referencia también para las otras comarcas de la provincia de Tarragona14, que integran siete hospitales (hospitales fuera del área). Cuando un equipo de atención sanitaria con capacidad para indicar terapia de reperfusión (centro de atención primaria, SEM, hospitales) establece el diagnóstico de IAMCEST, contacta con el SEM: en el momento en que este confirma el diagnóstico y decide el traslado, se considera activado el Código Infarto. El SEM contacta con el equipo de cardiología de guardia (teléfono único de contacto directo) para comunicar la llegada del paciente, y el cardiólogo de guardia avisa a la unidad de cardiología intervencionista mientras el paciente es trasladado de forma prioritaria directamente al laboratorio de hemodinámica. En el momento de la activación, se administra doble antiagregación (ácido acetilsalicílico y clopidogrel 600 mg) y anticoagulación (heparina no fraccionada, 1 mg/kg en bolo intravenoso).
Figura 1. Área de referencia de nuestro centro. Hospitales del área y fuera del área.
Con los pacientes que consultan directamente a urgencias de nuestro centro, el funcionamiento del Código Infarto no difiere respecto al periodo previo: se llama al cardiólogo de guardia, que avisa a la unidad de cardiología intervencionista.
En pacientes que necesitan traslados de otros hospitales para realizar la AP, si el centro de coordinación del SEM considera que el tiempo previsto entre el diagnóstico y la apertura de la arteria supera claramente los 120 min, se recomienda tratamiento fibrinolítico in situ; si este es ineficaz, se traslada al paciente para angioplastia de rescate.
La puesta en marcha del Código Infarto se ha realizado en el nivel extrahospitalario mediante reorganización de los flujos de las ambulancias, sin aumentar los recursos del sistema de transporte. A nivel hospitalario el aumento de recursos se ha concretado con la disponibilidad de dos camas de cuidados intermedios tras intervenciones y el aumento de plantilla de una enfermera y un cardiólogo intervencionista a tiempo parcial.
Dado el aumento de volumen de trabajo supuesto por la implantación del programa, y con la intención de ofrecer una asistencia adecuada a todos los pacientes sin sobrecargar el centro intervencionista, se ha elaborado un protocolo de regreso a los hospitales de referencia que prevé, tras el procedimiento, que los pacientes hemodinámicamente estables y sin complicaciones se trasladen a su hospital de referencia. Los traslados a un hospital con unidad de cuidados intensivos pueden efectuarse pasadas 8 h de la reperfusión; el retorno a un hospital con planta convencional se hace efectivo a partir de las 24 h.
Variables del estudioSe recogieron datos de filiación, procedencia de los pacientes, antecedentes, características clínicas, datos del infarto y del procedimiento.
En cuanto a los tiempos se recogieron los siguientes parámetros: hora del inicio de los síntomas, hora del primer contacto médico (hora en que se realiza el primer electrocardiograma diagnóstico y se indica el tratamiento de reperfusión percutánea)15, hora de llegada al laboratorio de hemodinámica y hora de apertura de la arteria (hora de paso del primer dispositivo).
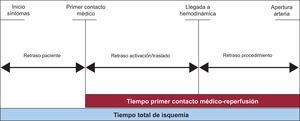
Teniendo en cuenta estos tiempos, se consideraron los siguientes retrasos (Figura 2): retraso del paciente (tiempo desde el inicio de los síntomas hasta el primer contacto médico), retraso activación/traslado (tiempo desde el primer contacto médico hasta la llegada al laboratorio de hemodinámica) y retraso del procedimiento (tiempo desde la llegada al laboratorio de hemodinámica hasta la apertura de la arteria).
Figura 2. Intervalos de tiempo analizados.
Finalmente se calcularon los siguientes intervalos: tiempo primer contacto médico- reperfusión (TPR, tiempo desde el primer contacto médico hasta la apertura de la arteria) y tiempo total de isquemia (tiempo desde el inicio de los síntomas hasta la apertura de la arteria).
El éxito del procedimiento de reperfusión se definió como flujo TIMI (Thrombolysis in Myocardial Infarction) de grado 3 final y estenosis residual < 20%16.
Se ha realizado un seguimiento clínico a 30 días y 1 año recogiendo los datos de mortalidad (total y de causa cardiovascular), reinfarto, nueva revascularización del vaso «responsable» y accidentes cerebrovasculares. Se ha analizado el evento combinado de muerte por todas las causas, reinfarto y nueva revascularización del vaso «responsable» a 30 días y 1 año.
Análisis estadísticoLas variables cuantitativas se muestran como media±desviación estándar y se compararon mediante test de la t de Student; si no siguen distribución normal, se describen como mediana [intervalo intercuartílico] y se compararon mediante la prueba de rangos de Mann-Whitney. Las variables categóricas se compararon mediante el test de la χ2 de Pearson y se describen como valor y porcentaje.
El análisis de supervivencia se realizó mediante el método de riesgos proporcionales de Cox a través de una regresión por pasos. Se incluyeron en el análisis multivariable las variables que resultaron significativas en el univariable (p<0,1) y las variables clínicamente relevantes según estudios previamente publicados. Se comprobó el supuesto de proporcionalidad mediante la introducción en el modelo de las interacciones entre las variables en estudio y el tiempo de supervivencia. Se han construido las curvas de supervivencia a partir del modelo de Cox realizado. Se aceptó un valor de significación estadística de p<0,05 bilateral. El programa utilizado fue SPSS 18.3 (SPSS, Inc., Chicago, Illinois, Estados Unidos).
ResultadosCaracterísticas clínicasEn la fase PreCódigo (1 de junio de 2008-31 de mayo de 2009), se realizó en nuestro centro reperfusión percutánea en las primeras 12 h del infarto a 241 pacientes, mientras que en la fase del Código Infarto (1 de junio de 2009-31 de mayo de 2010) los procedimientos de reperfusión fueron 514, lo que supone un incremento del 112%.
Durante el periodo del Código Infarto se realizaron en nuestro centro 566 procedimientos de cateterismo emergente (indicación de AP o angioplastia de rescate), de los cuales 52 (9,2%) se consideraron falsas alertas, por lo que no se los incluyó en el análisis. Las características clínicas de los pacientes se resumen en la Tabla 1; no se encontraron diferencias significativas entre los dos grupos. Se observó un incremento significativo del porcentaje de AP frente a la angioplastia de rescate. Se detectó un incremento en las tasas de utilización de bivalirudina como anticoagulante en la fase del Código Infarto.
Tabla 1. Características basales, del evento y del procedimiento
| PreCódigo (n=241) | Código Infarto (n=514) | p | |
| Datos demográficos | |||
| Edad | 61,5±12,6 | 61,8±13,4 | 0,75 |
| Mujeres | 44 (18,3) | 103 (20) | 0,6 |
| Antecedentes | |||
| Tabaquismo | 119 (49,4) | 228 (44,4) | 0,2 |
| Dislipemia | 138 (57,3) | 266 (51,8) | 0,16 |
| Hipertensión | 138 (57,3) | 294 (57,2) | 0,99 |
| Diabetes | 57 (23,7) | 137 (26,7) | 0,4 |
| Insuficiencia renal | 11 (4,6) | 31 (6) | 0,4 |
| Vasculopatía periférica | 26 (10,8) | 32 (6,2) | 0,03 |
| IAM previo | 26 (10,8) | 63 (12,3) | 0,6 |
| ICP previo | 18 (7,5) | 39 (7,6) | 0,95 |
| Cirugía coronaria previa | 6 (2,5) | 7 (1,4) | 0,21 |
| Datos del infarto | |||
| IAM anterior | 100 (41,5) | 238 (46,3) | 0,22 |
| IAM inferior | 133 (55) | 252 (49) | 0,12 |
| Killip ≥ III | 24 (10) | 31 (6) | 0,081 |
| Shock cardiogénico | 11 (4,6) | 17 (3,3) | 0,4 |
| IOT | 17 (7,1) | 23 (4,5) | 0,14 |
| Tratamiento | |||
| AAS | 238 (98,7) | 507 (98,6) | 0,5 |
| Clopidogrel | 229 (95) | 488 (94,9) | 0,99 |
| Heparina | 230 (95) | 492 (96) | 0,98 |
| Abcximab | 45 (18,7) | 109 (21,2) | 0,44 |
| Bivalirudina | 31 (12,9) | 125 (24,3) | < 0,001 |
| Datos del procedimiento | |||
| Angioplastia primaria | 195 (80,9) | 486 (94,6) | < 0,001 |
| Angioplastia de rescate | 46 (19,1) | 28 (5,4) | < 0,001 |
| Horario extralaboral | 113 (47) | 286 (64) | < 0,001 |
| BCPIAo | 13 (5,4) | 9 (1,8) | 0,009 |
| Flujo TIMI 0-1 inicial | 177 (73,6) | 396 (77,4) | 0,32 |
| Enfermedad de tres vasos | 43 (17,8) | 97 (18,9) | 0,77 |
| Aspiración de trombo | 167 (69) | 365 (71) | 0,67 |
| Stent intracoronario | 223 (92,5) | 476 (92,6) | 0,97 |
| Flujo TIMI 3 final | 229 (95) | 488 (94,9) | 0,99 |
| Éxito angiográfico | 227 (94,2) | 480 (93,2) | 0,75 |
| Zwolle score | 3,6 [1-4] | 3,2 [1-4] | 0,12 |
AAS: ácido acetilsalicílico; BCPIAo: balón de contrapulsación intraaórtico; IAM: infarto agudo de miocardio; ICP: intervencionismo coronario percutáneo; IOT: intubación orotraqueal; TIMI: Thrombolysis in Myocardial Infarction.
Los resultados se expresan como media±desviación estándar, n (%) o mediana [intervalo intercuartílico].
No se observaron diferencias significativas en cuanto al éxito del procedimiento. Destaca la tendencia a mayor gravedad en la fase PreCódigo. Las variables relativas a hipotensión, shock cardiogénico, clase Killip avanzada e implantación de balón de contrapulsación intraaórtico se presentaron con mayor frecuencia en la fase PreCódigo.
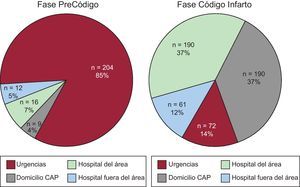
Procedencia de los pacientes y lugar de activaciónDurante la fase del Código Infarto se observó un incremento de los pacientes trasladados por el SEM desde el domicilio o el centro de atención primaria (116 frente a 190) y desde los hospitales del área de referencia (35 frente a 191), mientras que el número de pacientes que acudieron espontáneamente a urgencias de nuestro centro permaneció igual (Tabla 2). En el conjunto, la procedencia de un centro no intervencionista pasó del 24% (n=57) al 49% (n=252). La decisión de activar el sistema de AP en el periodo PreCódigo se tomó casi exclusivamente en nuestro centro a la llegada del paciente. Por contra, tras la implantación del Código Infarto, el 86% de las activaciones procedieron de fuera de nuestro centro (Figura 3). Como consecuencia de esta modificación, el porcentaje de pacientes que entraron directamente al laboratorio de hemodinámica sin pasar por urgencias fue del 11% (n=26) en la fase PreCódigo al 67% (n=327) en la fase Código Infarto. Se observó un incremento significativo de los procedimientos realizados en horario extralaboral (Tabla 1).
Tabla 2. Tiempo primer contacto médico-reperfusión según periodo, procedencia e indicación de reperfusión
| PreCódigo | Código Infarto | p | |
| A. Total de la población | |||
| Domicilio/CAP (n=116/190) | 125 [90-160] | 80 [63-105] | < 0,001 |
| Urgencias (n=68/72) | 82 [60-125] | 70 [50-84) | 0,03 |
| Hospital del área (n=35/191) | 135 [106-200] | 90 [75-110] | < 0,001 |
| Hospital de fuera del área (n=22/61) | 218 [168-300] | 132 [105-155] | < 0,001 |
| B. Sólo angioplastia primaria | |||
| Domicilio/CAP (n=104/189) | 123 [89-160] | 80 [63-105] | < 0,001 |
| Urgencias (n=68/72) | 82 [60-125] | 70 [50-84] | 0,03 |
| Hospital del área (n=16/191) | 130 [105-165] | 90 [75-110] | 0,001 |
| Hospital de fuera del área (n=7/34) | 215 [160-235] | 119 [95-148] | < 0,001 |
CAP: centro de atención primaria.
Tiempos (minutos) como mediana [intervalo intercuartílico].
Figura 3. Lugar de indicación de la reperfusión. Diferencias entre las fases PreCódigo y Código Infarto. CAP: centro de atención primaria.
Tiempos de actuaciónLa Tabla 3 pormenoriza los cambios observados en los tiempos de actuación. Se ha detectado una reducción significativa en el tiempo total de isquemia en 30 min de mediana (reducción del 12,2%). Se ha detectado también una reducción más marcada en el TPR de 32 min de mediana (reducción del 26,7%). En el análisis pormenorizado de los retrasos, se ha producido una reducción en el retraso activación/traslado de 29 min, mientras que el retraso intrahospitalario se ha reducido una de mediana en 3 min. No se han observado cambios significativos en el retraso del paciente.
Tabla 3. Tiempos de actuación
| PreCódigo | Código Infarto | p | |
| A. Población total (n) | 241 | 514 | |
| TPR | 120 [85-165] | 88 [68-114] | < 0,001 |
| Tiempo total de isquemia | 246 [180-390] | 216 [166-330] | 0,001 |
| Retraso del paciente | 110 [75-215] | 115[60-184] | 0,2 |
| Retraso activación/traslado | 85 [53-130] | 56 [40-85] | < 0,001 |
| Retraso intrahospitalario | 30 [25-40] | 27 [20-35] | < 0,001 |
| B. Angioplastia primaria (n) | 195 | 482 | |
| TPR | 115 [80-160] | 85 [66-110] | < 0,001 |
| Tiempo total de isquemia | 225 [170-360] | 210 [165-310] | 0,02 |
| Retraso del paciente | 107 [70-203] | 111[57-175] | 0,3 |
| Retraso activación/traslado | 80 [45-120] | 55 [39-80] | < 0,001 |
| Retraso intrahospitalario | 30 [25-40] | 27 [20-35] | < 0,001 |
TPR: tiempo primer contacto médico-reperfusión.
Tiempos (minutos) como mediana [intervalo intercuartílico].
El porcentaje de pacientes con TPR < 120 min fue significativamente mayor en el grupo Código Infarto (el 81 frente al 51%; p<0,001).
Dado el mayor porcentaje de pacientes tratados con angioplastia de rescate en la fase PreCódigo, se han analizado los tiempos de actuación en el subgrupo de pacientes tratados con AP, en los que se mantienen las mismas diferencias observadas para el total de la población (Tabla 3B).
El análisis según la procedencia permite detectar que la disminución de los tiempos de actuación se ha producido en todos los lugares de activación del Código Infarto (Tabla 2). Este resultado se mantiene cuando se analiza sólo a los pacientes sometidos a AP, y se observa una reducción significativa del TPR incluso en caso de traslado de mayor distancia (hospitales fuera del área).
Resultados clínicosMortalidadLa mortalidad total de los pacientes con IAMCEST tratados mediante angioplastia en las primeras 12 h del infarto fue del 6,5% a 30 días y del 9,8% a 1 año de seguimiento. Las tasas brutas de mortalidad por todas las causas a 30 días y 1 año fueron inferiores en el grupo Código Infarto (Tabla 4A). La Tabla 4B expresa los datos relativos a los pacientes sometidos a AP y muestra resultados parecidos a los de la población total.
Tabla 4. Análisis descriptivo de los resultados clínicos
| PreCódigo | Código Infarto | p | |
| A. Población total | 241 | 514 | |
| Eventos a 30 días | |||
| Mortalidad total | 22 (9,1) | 27 (5,3) | 0,044 |
| Mortalidad cardiaca | 21 (8,7) | 23 (4,5) | 0,02 |
| Reinfarto | 5 (2,1) | 7 (1,4) | 0,54 |
| TVR | 4 (1,7) | 6 (1,2) | 0,74 |
| ACV | 3 (1,2) | 3 (0,6) | 0,39 |
| ECVM | 26 (10,8) | 34 (6,8) | 0,063 |
| Eventos a 1 año | |||
| Mortalidad total | 33 (13,7) | 41 (8) | 0,018 |
| Mortalidad cardiaca | 27 (11,2) | 30 (5,8) | 0,012 |
| Reinfarto | 13 (5,4) | 13 (2,6) | 0,06 |
| TVR | 11 (4,6) | 16 (3,2) | 0,4 |
| ECVM | 45 (18,8) | 57 (11,5) | 0,007 |
| B. Angioplastia primaria | 195 | 486 | |
| Eventos a 30 días | |||
| Mortalidad total | 15 (7,7) | 25 (5,1) | 0,21 |
| Mortalidad cardiaca | 14 (7,2) | 21 (4,3) | 0,13 |
| Reinfarto | 5 (2,6) | 6 (1,3) | 0,31 |
| TVR | 4 (2,1) | 5 (1,1) | 0,46 |
| AVC | 1 (0,5) | 2 (0,4) | 1 |
| ECVM | 19 (9,7) | 31 (6,6) | 0,19 |
| Eventos a 1 año | |||
| Mortalidad total | 26 (13,3) | 37 (7,6) | 0,016 |
| Mortalidad cardiaca | 20 (10,3) | 26 (5,3) | 0,027 |
| Reinfarto | 10 (5,1) | 11 (2,3) | 0,08 |
| TVR | 8 (4,1) | 15 (3,2) | 0,6 |
| ECVM | 34 (17,4) | 52 (10,9) | 0,03 |
ACV: accidente cerebrovascular; ECVM: eventos cardiovasculares mayores (muerte, reinfarto o nueva revascularización); TVR: nueva revascularización del vaso «responsable».
Los resultados expresan n (%).
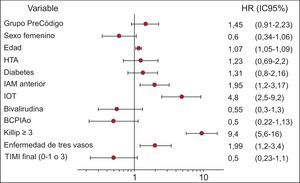
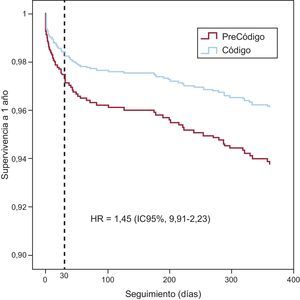
El análisis multivariable (Figura 4) mostró que las variables predictoras de mortalidad a 1 año son la edad, el infarto de localización anterior, la clase Killip ≥ III a la llegada al laboratorio de hemodinámica y la enfermedad multivaso. La variable relativa al periodo del estudio mostró tendencia a menos mortalidad en el grupo Código Infarto, sin diferencias significativas. Las curvas de supervivencia diseñadas a partir del análisis multivariable se muestran en la Figura 5. El análisis multivariable limitado a los pacientes sometidos a AP muestra que las variables predictoras de mortalidad a 1 año son las mismas que para la población general y confirma que la variable relativa al periodo del estudio se asocia con menos mortalidad en el grupo Código Infarto, sin diferencias significativas (hazard ratio=1,67; intervalo de confianza del 95%, 0,98-2,9; p=0,06).
Figura 4. Análisis multivariable de los factores predictivos de mortalidad al año de seguimiento. BCPIAo: balón de contrapulsación intraaórtico; HR: hazard ratio; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; IC95%: intervalo de confianza del 95%; IOT: intubación orotraqueal; TIMI: Thrombolysis in Myocardial Infarction.
Figura 5. Curvas de supervivencia a 1 año. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Reinfarto, revascularización, accidente cerebrovascularLas tasas de reinfarto a 30 días y 1 año no mostraron diferencias significativas entre los dos grupos; se observó tendencia a mayor incidencia de reinfarto al año de seguimiento en el grupo PreCódigo.
Las tasas de revascularización del vaso «responsable» a 30 días y 1 año no mostraron diferencias significativas.
Las tasas de accidentes cerebrovasculares a 30 días fueron bajas en ambos grupos. A pesar de una incidencia doble en el grupo PreCódigo, la diferencia observada no es significativa.
El análisis del evento combinado de muerte, reinfarto y nueva revascularización muestra una diferencia significativa entre los dos grupos al año de seguimiento (Tabla 4); esta diferencia no se mantiene en el análisis multivariable de supervivencia.
DiscusiónLa implantación del Código Infarto ha modificado radicalmente la atención al paciente con IAMCEST en nuestro medio. En línea con estudios previamente publicados, hemos observado un aumento a más del doble de los pacientes que recibieron tratamiento de reperfusión percutánea en la fase aguda del infarto agudo de miocardio y una reducción significativa de la angioplastia de rescate13 en nuestro laboratorio de hemodinámica.
Tiempos de actuaciónEn el presente estudio se demuestra una clara mejora en los tiempos de actuación respecto al periodo previo al Código Infarto en los pacientes tratados con angioplastia en las primeras 12 h. Actualmente, la gran mayoría de los pacientes tienen TPR que cumplen las recomendaciones de las guías europeas2. Entre las modificaciones aportadas por el nuevo protocolo queremos enfatizar la eficacia de la activación extrahospitalaria de la AP que, junto con el traslado directo al laboratorio de hemodinámica, se ha demostrado que influye significativamente en la reducción de los tiempos de actuación17. Hay que subrayar que en nuestro estudio nos referimos al tiempo del primer contacto médico como el momento en que se indica el tratamiento de reperfusión, ya sea en nuestro centro, en la atención extrahospitalaria o en otro centro sin capacidad para la AP. Esta puntualización es importante, ya que en algunas publicaciones recientes sobre los tiempos de actuación en Estados Unidos6, 18 se excluyó a los pacientes trasladados de otros centros (hasta un tercio del total) y se calculó el retraso a partir de la llegada del paciente al hospital con AP. Medir los tiempos a partir de la indicación terapéutica parece una estrategia más correcta, ya que permite valorar en su conjunto el funcionamiento del sistema de salud15. Nuestros resultados son comparables a los publicados en esta Revista por Rodríguez-Leor et al19, que obtuvieron tiempos totales de isquemia y TPR muy parecidos. En nuestra serie, respecto a dicho estudio, los pacientes trasladados desde otros centros, a pesar de un área de referencia de mayores dimensión y población, mostraron tiempos de actuación más cortos, que se ajustan a los recomendados por las guías. Es especialmente en este grupo de pacientes en el que la implantación del Código Infarto ha permitido la mayor reducción del TPR respecto al periodo anterior.
En cuanto a los pacientes procedentes de centros fuera del área de referencia, a pesar de una reducción de los tiempos respecto a la fase PreCódigo, el TPR sigue presentando valores por encima de los recomendados por las guías; es necesario un esfuerzo ulterior para optimizar la estrategia de traslado y ajustarse a las recomendaciones con el objetivo de mantener el beneficio clínico de la AP y garantizar una asistencia homogénea a toda la población.
No obstante, teniendo en cuenta que hay traslados de hasta 200 km, los tiempos obtenidos no se diferencian de otros registros del «mundo real» que han evaluado escenarios similares8, 10, 20.
Eventos clínicosLos resultados de mortalidad son comparables a los obtenidos por otros programas de atención al IAMCEST de ámbito nacional21 y además se ajustan a los datos publicados en ensayos clínicos y registros internacionales9, 22, 23, 24. Destaca la tendencia a la mejora de la situación clínica al ingreso, con menor incidencia de insuficiencia cardiaca grave entre los pacientes del grupo Código Infarto. Esta diferencia en variables clínicas fundamentales para marcar el pronóstico tiene varias explicaciones. En primer lugar se puede justificar, en parte, por la reducción del porcentaje de pacientes sometidos a angioplastia de rescate, un subgrupo con peor perfil de gravedad y tendencia a evolucionar peor25, 26. En segundo lugar, la disminución de los tiempos de actuación ha contribuido a mejorar el perfil de gravedad a la llegada al laboratorio de hemodinámica. Finalmente, no podemos descartar de nuestro estudio la presencia de un sesgo de selección en el periodo PreCódigo que haya influido en los resultados clínicos.
Respecto a otras series publicadas, no hemos encontrado diferencias en los factores predictores de mortalidad en nuestra población6, 21, 27. Sería necesario incluir a mayor número de pacientes para determinar un impacto significativo en la mortalidad con la aplicación del Código Infarto. Sin embargo, la reducción observada en los tiempos de actuación y la situación clínica inicial más favorable a la llegada a la sala de hemodinámica tienen una repercusión indudable en la tendencia observada.
Las diferencias en mortalidad y eventos clínicos observadas en los dos grupos se mantienen en el subgrupo de pacientes sometidos a AP, dato que subraya la importancia de la reducción de los retrasos tras la instauración del Código Infarto.
Un aspecto reseñable es que, debido a características de nuestra área geográfica, la población que asiste nuestro hospital tiene poca movilización intersectorial, con lo que el programa de Código Infarto puede servir para identificar la incidencia real del infarto de miocardio susceptible de reperfusión por población en nuestro medio.
LimitacionesSe trata de un estudio unicéntrico y observacional y, aunque la recogida de las variables se ha realizado de forma prospectiva, algunas diferencias pueden no haber sido detectadas y condicionar los resultados encontrados. Como ya se ha comentado, además, si bien se ha recogido a todos los pacientes remitidos a nuestro hospital durante el periodo de estudio, lo que otorga buena representación del funcionamiento de la AP en el «mundo real», no se puede descartar un sesgo de selección en cuanto al periodo PreCódigo. En efecto, desconocemos la incidencia real y las características de los infartos tratados mediante fibrinolisis eficaz o no tratados con ninguna terapia de reperfusión en ese periodo. A la luz de esta consideración, la interpretación de los resultados clínicos tiene que ser cuidadosa, aunque la implantación del Código Infarto representa la mayor diferencia entre los dos periodos y probablemente sea el principal factor de las mejoras observadas en la evolución de nuestros pacientes.
ConclusionesSe ha demostrado que la implantación del Código Infarto mejora los tiempos de actuación en la atención a los pacientes con IAMCEST tratados en nuestro centro con AP, lo que resulta en una red asistencial eficaz, incluso en caso de traslados largos. El buen funcionamiento de este protocolo se confirma por los resultados a corto y medio plazo, con mejora del perfil clínico de los pacientes a la llegada al laboratorio de hemodinámica y tasas bajas de mortalidad en el seguimiento.
FinanciaciónEste trabajo ha sido subvencionado en parte por una beca no condicionada de Boston Scientific (P.D.D.), una beca de la Sección de Hemodinámica y Cardiología Intervencionista de la Sociedad Española de Cardiología para formación en investigación post-residencia, 2011 (S.H.) y un programa IDIBELL de formación post residencia en investigación (J.G.L). También se ha desarrollado en parte por la iniciativa Stent for Life de la Sociedad Española de Cardiología y la Sociedad Europea de Cardiología.
Conflicto de interesesNinguno.
Recibido 9 Febrero 2012
Aceptado 11 Junio 2012
Autor para correspondencia: Unidad de Hemodinámica y Cardiología Intervencionista, Servicio de Cardiología, Área de Enfermedades del Corazón, Hospital Universitario de Bellvitge, Feixa Llarga s/n, 08007 L’Hospitalet de Llobregat, Barcelona, España. 26587jgh@comb.cat