Las guías de fibrilación auricular (FA) de la Sociedad Europea de Cardiología incluyen en la estratificación del riesgo tromboembólico nuevos factores «moduladores» que recalifican a un porcentaje de pacientes anteriormente catalogados de riesgo «bajo» o «moderado» a categorías superiores. El objetivo de nuestro estudio es analizar el impacto de la escala CHA2DS2-VASc y las nuevas recomendaciones de anticoagulación oral (ACO) en una muestra contemporánea de pacientes con FA reclutados en consultas externas de cardiología y atención primaria.
MétodosEstudio epidemiológico observacional, transversal y multicéntrico diseñado por la sección de hipertensión arterial con el objetivo de conocer la prevalencia y el control de la hipertensión en la práctica clínica habitual. Cada médico debía incluir a los primeros 6 pacientes de cada día durante 5 días.
ResultadosSe reclutó a 25.137 pacientes, de los que 1.544 tenían el antecedente de FA. De estos, el 77,3% tenía una puntuación CHADS2 ≥ 2. Se recalificó según la escala CHA2DS2-VASc a la población restante con CHADS2 < 2. El 14,4% tenía ≥ 75 años (CHA2DS2-VASc = 2). De los menores de 75 años, el 42,3% tenía un CHA2DS2-VASc = 2; el 23,7%, CHA2DS2-VASc = 3 y el 1,1%, CHA2DS2-VASc = 4. Esto supone que el 85,1% de los pacientes con CHADS2 < 2 tendrán, en ausencia de contraindicaciones, indicación de ACO.
ConclusionesLas nuevas indicaciones supondrán un incremento significativo en el número de pacientes con indicación de ACO, a expensas de los previamente categorizados como con riesgo «bajo-moderado». Por lo tanto, será indispensable identificarlos con vistas a disminuir el riesgo tromboembólico sin dejar de prestar atención al perfil de riesgo hemorrágico.
Palabras clave
La identificación de factores de riesgo de complicaciones tromboembólicas en pacientes con fibrilación auricular (FA) no valvular supone uno de los grandes retos en el manejo de estos pacientes y ha llevado en la última década a la publicación de varios algoritmos de estratificación de riesgo con el objetivo de categorizar a los pacientes en función de su riesgo embólico1, 2, 3, 4, 5. La más aceptada es la escala CHADS2, acrónimo de varios factores de riesgo establecidos3: insuficiencia cardiaca (IC), hipertensión arterial (HTA), edad ≥ 75 años, diabetes mellitus (DM) y accidente cerebrovascular (ACV), que asignan un punto a cada uno de ellos excepto al antecedente de ACV, que suma dos. Sin embargo, esta escala posee ciertas limitaciones, especialmente en pacientes con riesgo «bajo-moderado», pues muchos de ellos se beneficiarían del tratamiento con anticoagulación oral (ACO), y además no considera otros marcadores de riesgo6.
Las guías de la Sociedad Europea de Cardiología de 20107 enfatizan otros factores «moduladores» no recogidos previamente, como la enfermedad vascular y el sexo femenino, y recodifica la edad en tres categorías (< 65 años, entre 65 y 74 años, y ≥ 75 años). La nueva escala, denominada CHA2DS2-VASc, recalifica a un porcentaje considerable de pacientes considerados anteriormente como en riesgo «bajo» o «moderado» a categorías superiores, lo que sentaría la indicación de ACO, aunque la magnitud real de estas recomendaciones no ha sido cuantificada. El objetivo de nuestro estudio es analizar el impacto de la clasificación de los pacientes con FA según la escala CHA2DS2-VASc, en comparación con la escala CHADS2, y las nuevas recomendaciones de ACO en una muestra contemporánea de pacientes con FA reclutados en consultas externas de cardiología y atención primaria. Además, se buscó hacer un análisis comparativo con los resultados del registro de similar diseño CARDIOTENS 19998.
MétodosDiseño del estudioEstudio epidemiológico observacional, transversal y multicéntrico diseñado por la Sección de Hipertensión Arterial de la Sociedad Española de Cardiología (SEC), y avalado por la Agencia de Investigación de la SEC, con el objetivo de conocer la prevalencia y el control de la HTA en la práctica clínica habitual. Los pacientes fueron reclutados en consultas externas de atención primaria y cardiología. Los criterios de inclusión fueron: edad ≥ 18 años, posibilidad de registrar toda la historia clínica y diagnósticos previos de enfermedad cardiovascular y que el paciente, o su representante legal, otorgase su consentimiento para participar en el estudio de forma escrita (consentimiento informado firmado). Los criterios de exclusión fueron adicción o consumo de drogas ilegales (cocaína, cannabis, psicotrópicos) y denegación del consentimiento. Se seleccionó a 885 médicos, el 89,1% de atención primaria y el 10,9% de cardiología. Cada uno de los médicos participantes debía incluir a los primeros 6 pacientes de cada día, durante 5 días, que cumpliesen los criterios de inclusión del estudio. Se reclutó a un total de 25.137 pacientes: 15.102 (60,1%) tenían algún factor de riesgo o enfermedad cardiovascular y 1.544 (el 6,14% del total; intervalo de confianza del 95%, 6,13-6,15), diagnóstico de FA. Se elaboró un cuestionario específico para el estudio, en papel, para cada paciente. Al igual que en el registro CARDIOTENS de 19998, en la primera hoja se recogía información relativa a datos sociodemográficos, presencia de enfermedad cardiovascular, factores de riesgo cardiovascular y antecedentes personales del paciente. En caso de que se contestase positivamente a alguno de los apartados de presencia de enfermedad cardiovascular diagnosticada (cardiopatía isquémica, angina o infarto, IC o ACV) o presencia de factores de riesgo (dislipemia, HTA, DM o consumo de tabaco), se continuaba recogiendo datos, en una segunda hoja que contenía información adicional más detallada sobre el tratamiento, características del electrocardiograma, ecocardiograma y datos de laboratorio. Los datos del electrocardiograma y/o analíticos debían ser de los 6 meses previos. Los valores de presión arterial y frecuencia cardiaca se recogieron en el momento de la consulta.
Definición de variablesLa escala CHADS2 se calculó otorgando 1 punto por la presencia de cada uno de los siguientes: IC, HTA, edad > 65 años o DM, y 2 puntos al antecedente de ACV previo, por lo que 6 fue la máxima puntuación. La escala CHA2DS2-VASc otorga 1 punto a la presencia de IC (o disfunción ventricular izquierda), HTA, DM, enfermedad vascular periférica (que incluye infarto de miocardio, placa aórticas complejas y enfermedad arterial periférica), edad entre 65 y 74 y sexo femenino, y 2 puntos a la edad ≥ 75 años y el ACV previo7.
Se consideró HTA en caso de obtenerse dos mediciones consecutivas de presión arterial ≥ 140/90mmHg o se siguiese tratamiento antihipertensivo específico. Para el control de la HTA, se consideraron los objetivos de control de las guías de la reevaluación de 2009 (< 140/90mmHg). Para el antecedente de DM, se aceptó la constatación en la historia clínica de un diagnóstico previo, seguir tratamiento farmacológico específico o el registro consecutivo de dos glucemias en ayunas > 126mg/dl. Para el antecedente de FA, se requirió que figurase en algún informe médico o hubiese algún registro electrocardiográfico en la historia de los pacientes. Se codificó como antecedente de cardiopatía isquémica a todos los pacientes con historia previa de infarto agudo de miocardio, angina estable o inestable, revascularización coronaria percutánea o quirúrgica o test de inducción de isquemia positivo (ergometría, gammagrafía, ecocardiograma de estrés, etc.). La IC se registró para los pacientes que hubieran tenido al menos un ingreso hospitalario con ese diagnóstico en el informe médico de alta, además de los pacientes con signos y síntomas de IC que tuvieran una prueba de imagen compatible (radiografía de tórax o ecocardiograma). Se recogió como antecedente de ACV los casos en que figuraba en la historia clínica o algún informe médico el diagnóstico de ACV isquémico, hemorrágico o transitorio. Los antecedentes de claudicación de la marcha, revascularización de extremidades inferiores, amputación o diagnóstico establecido se codificaron como enfermedad arterial periférica. Para el análisis de la categoría de pacientes con ECV, se analizó conjuntamente a los que tenían cardiopatía isquémica, IC, arteriopatía periférica o ACV.
Análisis estadísticoLos datos fueron procesados mediante el paquete estadístico SPSS 15.0 (SPSS Inc.; Chicago, Illinois, Estados Unidos). Todas las variables siguieron una distribución normal y se presentan como media±desviación estándar; las comparaciones de proporciones se analizaron mediante pruebas de la t de Student y test de la χ2 para valorar las diferencias estadísticas entre el tratamiento médico de los pacientes con y sin FA. La comparación de la utilización de ACO entre el registro CARDIOTENS 1999 y CARDIOTENS 2009 se realizó mediante el contraste con la t de Student, usando para el cálculo de la varianza las estimaciones de los porcentajes de cada uno de los registros. Se atribuyó significación estadística a los valores de p≤0,05.
ResultadosDe los 25.137 pacientes reclutados en el estudio, 1.544 (el 6,14% del total y el 10,22% de los pacientes con factores de riesgo o ECV) tenían el antecedente de FA (paroxística, persistente o permanente). Como se muestra en la Tabla 1, los pacientes con FA presentaron mayor media de edad, prevalencia de factores de riesgo y ECV. En lo referente al tratamiento médico, los pacientes con FA recibían más ACO, antiagregantes, bloqueadores beta, antihipertensivos, nitratos, antagonistas del calcio, diuréticos y estatinas (Tabla 2).
Tabla 1. Características basales de los pacientes con y sin fibrilación auricular
| Total | Sin FA | Con FA | p | |
| Total (n) | 25.137 | 23.593 (93,5%) | 1.544 (6,5%) | |
| Edad (años) a | 61±15,51 | 52±15,4 | 73±10,8 | < 0,01 |
| Frecuencia cardiaca (lat/min) | 73±10,84 | 73±10,42 | 74±13,45 | 0,11 |
| PAS (mmHg) | 135,6±15,48 | 135,51±15,2 | 135,85±16,59 | 0,44 |
| PAD (mmHg) | 78,7±11 | 78,74±11,31 | 78,33±12,86 | 0,19 |
| IMC a | 28,35±4,82 | 28,29±4,82 | 28,81±4,91 | < 0,01 |
| Perímetro abdominal (cm) a | 96,42±14,27 | 96,24±14,13 | 97,26±14,62 | < 0,01 |
| Glucosa (mg/dl) a | 110,9±36,67 | 110,16±35,8 | 115,77±40,71 | < 0,01 |
| Colesterol total (mg/dl) a | 204±44,62 | 204,82±44,62 | 197,69±43,48 | < 0,01 |
| cLDL (mg/dl) a | 123,33±37,25 | 123,8±37,32 | 119,7±35,89 | < 0,01 |
| cHDL (mg/dl) a | 52,73±15,83 | 53,08±15,79 | 50,32±15,5 | < 0,01 |
| Triglicéridos (mg/dl) | 142,13±69,97 | 141,67±69,6 | 144,06±72,4 | 0,23 |
| Ácido úrico (mg/dl) a | 5,44±1,58 | 5,38±1,55 | 5,91±1,68 | < 0,01 |
| Creatinina (mg/dl) a | 0,72±0,78 | 0,7±0,74 | 0,83±0,71 | < 0,01 |
| Glucohemoglobina (%) | 6,25±1,43 | 6,28±1,41 | 6,31±1,44 | 0,3 |
cHDL: colesterol de las lipoproteínas de alta densidad; cLDL: colesterol de las lipoproteínas de baja densidad; FA: fibrilación auricular; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
La primera columna representa el número de pacientes en los que se pudo registrar dicha variable. Los valores expresan media±desviación estándar.
a Variables en las que hubo diferencia estadísticamente significativa.
Tabla 2. Tratamiento de los pacientes en función de la presencia o ausencia de fibrilación auricular
| Total | Sin FA | Con FA | p | |
| Pacientes | 25.137 | 23.596 | 1.544 | |
| ACO | 1.372 (5,5) | 404 (1,7) | 968 (62,7) | < 0,01 |
| Ácido acetilsalicílico | 4.055 (16,1) | 3.579 (15,2) | 476 (30,8) | < 0,01 |
| Clopidogrel | 1.175 (4,7) | 995 (4,2) | 180 (11,7) | < 0,01 |
| Bloqueadores beta | 2.937 (11,7) | 2.297 (9,7) | 640 (41,5) | < 0,01 |
| IECA | 4.736 (18,8) | 4.108 (17,4) | 628 (40,7) | < 0,01 |
| ARA II | 3.615 (14,4) | 3.076 (13) | 539 (34,9) | < 0,01 |
| Diuréticos | 509 (2) | 424 (1,8) | 85 (5,5) | < 0,01 |
| ACa | 3.615 (14,4) | 3.076 (13) | 539 (34,9) | < 0,01 |
| Nitratos | 1.281 (5,1) | 1.014 (4,3) | 267 (17,3) | < 0,01 |
| Estatinas | 6.509 (25,9) | 5.695 (24,1) | 814 (52,7) | < 0,01 |
ACa: antagonistas del calcio; ACO: anticoagulantes orales; ARA: antagonista del receptor AT1 de la angiotensina II; FA: fibrilación auricular; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los datos expresan n (%).
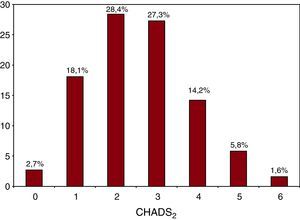
Del total de pacientes con FA, 1.193 (77,3%) presentaron un perfil de riesgo «moderado-alto» (puntuación CHADS2 ≥ 2); las puntuaciones de 2 y 3 fueron las más frecuentes (el 28,4 y el 27,3% respectivamente); tenían 1 punto 299 pacientes (18,1%) y únicamente 41 (2,7%), riesgo bajo (CHADS2=0) (Figura 1). De los pacientes con una puntuación CHADS2 ≥ 2, destaca que el 35,5% no estaba en tratamiento anticoagulante (n=148) y de estos, el 70,9% eran mayores de 65 años, el 56% eran mayores de 74 años y el 53,5% eran mujeres. En este subgrupo de pacientes con alto riesgo sin ACO, la terapia alternativa escogida preferentemente fue la antiagregación con ácido acetilsalicílico o clopidogrel (67,4%), el 8,9% estaba en doble terapia y un 23,7% no seguía ninguna. Por último, se observó mayor tendencia a no anticoagular a pacientes con CHADS2 ≥ 2 en centros de atención primaria que en consultas de cardiología (el 64,5 frente al 35,5%; p=0,08).
Figura 1. Porcentaje de pacientes en cada grupo según la escala CHADS2.
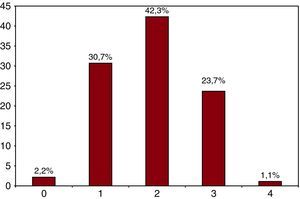
Respecto a la población con riesgo «bajo-moderado» según la escala CHADS2 (es decir, puntuación 0 o 1), se observó que el 41,7% de ellos no tomaba ACO, frente al 58,3% que sí los tomaba, y que se trataba preferentemente de pacientes mayores de 75 años (el 63,4 frente al 36,6% en el grupo de ≥ 75 años y el 56,8% frente al 43,2% en el grupo de menos de 75 años). El 14,4% de este grupo tenía una edad≥75 años (por lo tanto, CHA2DS2-VASc=2) y el 40% de ellos estaba en el grupo de entre 65 y 74 años. De este último grupo (pacientes menores de 75 años, con CHADS2<2), el 67,1% presentaba 2 o más factores de riesgo (el 42,3% CHA2DS2-VASc=2, el 23,7% CHA2DS2-VASc=3 y el 1,1% CHA2DS2-VASc=4). El 30,7% presentaba un factor de riesgo (CHA2DS2-VASc=1) y únicamente el 2,2% no presentaba ningún factor de riesgo (CHA2DS2-VASc=0) (Figura 2).
Figura 2. Porcentaje de factores de riesgo en pacientes menores de 75 años con puntuación CHADS2<2.
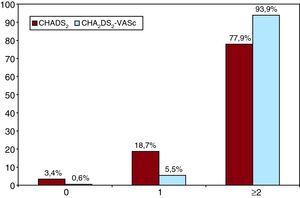
Por lo tanto, dentro de la categoría de riesgo «bajo o moderado», con la introducción de las nuevas escalas de riesgo, el porcentaje de pacientes con indicación de anticoagulación (en ausencia de contraindicaciones) supondría el 81,5% (el 67,1% de los menores de 75 años y el 14,4% correspondiente a los que presentan como único factor de riesgo la edad ≥ 75 años). Si a esto se añade la población en «alto riesgo» (77,3%), resultaría que el 93,8% de los pacientes con FA tendrán indicación de ACO (Figura 3). Por ende, queda un 1,8% de pacientes en que sería posible escoger entre esta terapia o la antiagregación.
Figura 3. Resultado final tras la categorización de los pacientes según la escala CHA2DS2-VASc comparándola con la escala CHADS2.
DiscusiónLos resultados de este análisis del estudio CARDIOTENS 2009 reflejan la elevada prevalencia de FA en los pacientes atendidos en las consultas médicas, con el consiguiente incremento de pacientes candidatos al tratamiento con ACO según las nuevas recomendaciones y estratificación del riesgo embólico. La media de edad, la prevalencia de factores de riesgo y la FA son similares a las de los registros nacionales e internacionales previos, por lo que nuestros resultados podrían ser representativos de la actividad clínica cotidiana. Además, es la primera vez que se lleva a cabo un análisis sobre el impacto de los nuevos criterios de anticoagulación en pacientes con FA en una amplia cohorte contemporánea de pacientes diagnósticas de FA en España.
Respecto al registro CARDIOTENS 1999, se observa un incremento en el número de pacientes bajo tratamiento con ACO9, pasando del 33% (intervalo de confianza del 95%, 32-34) al 62,7% (intervalo de confianza del 95%, 59,9-65,5) en 2009, lo que supone un incremento del 90% en la última década (p<0,01). Además, destaca que la gran mayoría de la población de estudio presenta un perfil de riesgo «moderado-alto» de eventos tromboembólicos (el 77,3% tiene un CHADS2 ≥ 2). A pesar de ello, hay un alto porcentaje de pacientes en alto riego sin anticoagulación, concretamente el 35%, que además son mayormente individuos con más riesgo, como los pacientes añosos y las mujeres. Esta infrautilización de los ACO, no obstante, es menor que la comunicada en otros registros10 y puede explicarse en parte por la presencia de contraindicaciones, pero también por la falta de indicación médica o de cumplimiento del paciente, debido a la necesidad de monitorización estrecha y/o miedo a sangrado. Por otra parte, dentro de este subgrupo de pacientes con riesgo de eventos tromboembólicos sin ACO, la estrategia preferida es monoterapia con ácido acetilsalicílico, a pesar de haberse demostrado que es inferior en la reducción de eventos tromboembólicos cuando se compara con ACO, tanto en monoterapia11 como en combinación con clopidogrel12, sin estar exenta de tasas significativas de hemorragia. Tal vez con las nuevas alternativas anticoagulantes de más cómodo manejo obviemos parte de estos problemas y se incremente su uso en los pacientes con esa indicación. Se deduce también de este registro el alto porcentaje de pacientes que con las nuevas recomendaciones tendrán indicación de ACO (> 90%) si extrapolamos los datos a la población general.
Este incremento en el porcentaje de pacientes con indicación para ACO es obviamente a expensas de los previamente categorizados como en riesgo «bajo-moderado», estrategia que previsiblemente conllevará una disminución en el riesgo de accidentes tromboembólicos, pero de forma colateral traerá un incremento de los eventos hemorrágicos en términos absolutos. Por lo tanto, será crucial, ahora más que antes, la identificación de esta población de riesgo para tratar de minimizar en la medida de lo posible sus riesgos potenciales, especialmente en sujetos añosos13. Las nuevas guías inciden en este punto aportando escalas de riesgo hemorrágico que habrá que tener en cuenta a la hora de la valorar la estrategia terapéutica. Las actuales recomendaciones, siguen dejando a elección del criterio médico la prescripción de ACO frente a antiagregantes en un porcentaje de pacientes, concretamente en aquellos con una puntuación CHA2DS2-VASc de 1 (aunque muestran su preferencia por la ACO). De cualquier forma, se tratará de un porcentaje mucho menor (el 1,8% en este registro), ya que muchos de ellos tendrán, en ausencia de contraindicaciones, indicación clara de anticoagulación.
Resulta paradójico el hecho de que, a pesar de que en la inmensa mayoría de los registros se ha demostrado reiteradamente la infrautilización del tratamiento anticoagulante10, parece que en cada edición de las guías de manejo de los pacientes con FA se amplían las indicaciones de la anticoagulación. Esto no ha estado exento de las críticas de quienes consideran que, por una parte, se trata de recomendaciones demasiado taxativas, a pesar de no haberse demostrado beneficios en ensayos clínicos aleatorizados para estos escenarios tan concretos14 y, segundo, que se hayan introducido sin tener datos concluyentes de su superioridad en lo que a impacto pronóstico se refiere respecto a la escala previa CHADS2. Además, si bien es cierto que alguno de los marcadores son fáciles de definir, como la edad o el sexo, la enfermedad vascular representa un criterio más difuso y difícil de aplicar a la población general, a la par que heterogéneo.
Para finalizar, aunque parece que estas guías ampliarán las indicaciones de ACO, es preciso matizar que en pacientes con FA y cardiopatía isquémica (concomitancia que se da en un 20-30% de los pacientes)15, se trata de minimizar o evitar en lo posible combinarlos con antiagregantes acortando la duración de la triple terapia tras la implantación de un stent: 1 mes en caso de no ser farmacoactivo y de 3 a 6 meses si es farmacoactivo o ha habido un síndrome coronario agudo. En los pacientes con riesgo hemorrágico HAS-BLED ≥ 3, se recomienda el uso de stents no farmacoactivos, con posterior asociación de ácido acetilsalicílico, clopidogrel y ACO durante 2-4 semanas y 4 semanas con esta terapia en caso de un síndrome coronario agudo7. Por lo tanto, es de esperar que, en este grupo en concreto, nos encontremos con menores tasas de sangrado que las actuales.
LimitacionesNuestro estudio presenta algunas limitaciones que merecen consideración. En primer lugar, al tratarse de un estudio transversal, no puede establecerse una cronografía de cada enfermedad y esto puede ser especialmente limitante en el caso de la FA, que puede variar en función de la estrategia del médico (control del ritmo o la frecuencia) y la propia evolución de la enfermedad y las complicaciones del tratamiento (embolias, hemorragias, ingresos hospitalarios, cirugías, etc.). Por otra parte, el registro CARDIOTENS no tiene un diseño poblacional que incluyera una muestra aleatoria y representativa de la población, sólo trata de reflejar a los pacientes atendidos en consultas, por lo que las conclusiones del estudio sólo pueden limitarse a este contexto. Otra limitación es que no se pueda calcular el riesgo hemorrágico en la cohorte analizada, por no disponerse de las todas las variables requeridas para el cálculo de la escala de riesgo hemorrágico HAS-BLED7. Por último, hubo una pequeña proporción de pacientes cuyo riesgo tromboembólico no se pudo calcular por haber valores perdidos; sin embargo, este porcentaje fue pequeño (1,9%), por lo que no creemos que ello pudiese interferir en las conclusiones del estudio.
ConclusionesLas nuevas indicaciones de manejo anticoagulante supondrán un incremento significativo en el número de pacientes con esa indicación, a expensas de los previamente categorizados como en riesgo «bajo-moderado». Por lo tanto, será indispensable identificarlos con vistas a disminuir el riesgo tromboembólico sin dejar de prestar atención al perfil de riesgo hemorrágico para compensar en la medida de lo posible el efecto colateral.
FinanciaciónEl estudio CARDIOTENS cuenta con una beca no condicionada de Laboratorios Recordati España.
Conflicto de interesesNinguno.
Recibido 11 Diciembre 2010
Aceptado 7 Marzo 2011
Autor para correspondencia: Heart Rhythm Management Centre, University Hospital Brussels-UZ Brussels, Laarbeeklaan 101, BE-1090 Bruselas, Bélgica. mrodrigu@uzbrussel.be