Uno de los objetivos de la prevención secundaria es conseguir la estabilización de la placa. En este estudio se investigaron las consecuencias clínicas y los factores predictivos del cambio en el tipo de placa (CTP) mediante ecografía intracoronaria seriada en pacientes con diabetes mellitus tipo 2 y enfermedad coronaria conocida.
MétodosSe estudiaron 237 segmentos (45 pacientes) de los ensayos DIABETES I, II y III. La ecografía intracoronaria se realizó con retirada motorizada (0,5mm/s) tras la intervención inicial y en un seguimiento angiográfico llevado a cabo a los 9 meses en el mismo segmento coronario. Se incluyeron las lesiones leves no tratadas (estenosis angiográfica < 25%) con grosor de la placa ≥ 0,5 mm y longitud ≥ 5 mm evaluadas mediante ecografía intracoronaria. Dado que puede haber diferentes tipos de placas en distintos lugares de una determinada lesión coronaria, cada lesión evaluada se dividió en tres segmentos para los análisis seriados cuantitativos y cualitativos. Se aplicó un ajuste estadístico por múltiples segmentos por lesión por paciente (método de ecuaciones de estimación generalizada). Se definió como CTP cualquier cambio cualitativo del tipo de placa observado en el seguimiento. En el seguimiento realizado a 1 año, se registraron los eventos adversos cardiacos mayores (muerte, infarto de miocardio y revascularización del vaso diana).
ResultadosSe observó un CTP en 48 lesiones (20,2%) y su aparición fue más frecuente (52,1%) en las placas mixtas. Los factores predictivos independientes del CTP fueron las cifras de glucohemoglobina (odds ratio [OR]=1,2; intervalo de confianza [IC] del 95%, 1,01-1,5; p=0,04); los inhibidores de la glucoproteína IIb/IIIa (OR=0,3; IC del 95%, 0,1-0,7; p=0,004) y la administración de estatinas (OR=0,3; IC del 95%, 0,1-0,8; p=0,02). En el seguimiento realizado a 1 año, el CTP se asoció a un aumento de la tasa de eventos adversos cardiacos mayores (CTP, 20,8% frente a ausencia de CTP, 13,8%; p=0,008; hazard ratio=1,9; IC del 95%, 1,3-1,9; p=0,01).
ConclusionesLos cambios cualitativos en las estenosis leves documentados mediante ecografía intracoronaria en los pacientes con diabetes mellitus tipo 2 se asocian a una prevención secundaria subóptima y pueden tener consecuencias clínicas.
Palabras clave
La ecografía intravascular (EIC) permite caracterizar la composición de la placa según su ecogenicidad1. De hecho, se ha demostrado que la EIC predice las características histológicas de las placas ateroscleróticas en el 96% de los pacientes estudiados en autopsias2. Se han descrito cuatro tipos básicos de componentes que corresponden a diferentes señales ecogénicas: depósitos de lípidos (hipoecogénicos), tejido fibromuscular (ecos blandos), tejido fibroso (ecos brillantes) y depósitos de calcio (ecos brillantes con sombra por detrás de la lesión)3. Se obtuvieron resultados similares en muestras histológicas extraídas en una aterectomía coronaria direccional, que mostraron que las placas con mayor fracción de tejido fibroso denso, elástico o calcificado son predominantemente ecogénicas, mientras que las placas blandas ecotransparentes tienen una mayor fracción de músculo liso y elementos trombóticos o necróticos4.
La evaluación de la morfología de la placa mediante EIC, con independencia de la gravedad de la estenosis subyacente, ha llevado a un mejor conocimiento de la fisiopatología de la enfermedad coronaria y de sus consecuencias clínicas en los estudios transversales5, 6. Así, las placas con mayor porcentaje de área lipídica y una cápsula fibrosa fina son más propensas a la rotura que las placas fibrosas7. A este respecto, las placas vulnerables que pueden conducir a episodios coronarios agudos se observan con mayor frecuencia en los pacientes con diabetes mellitus tipo 2 (DM2) que en los no diabéticos8. Para alcanzar la estabilización de la placa mediante la reducción de la cantidad de lípidos presentes en ella, se ha recomendado el tratamiento con estatinas para la prevención secundaria9.
Hasta la fecha, no se han evaluado prospectivamente las repercusiones clínicas del cambio en el tipo de placa (CTP) en los pacientes con DM2 mediante un examen seriado con EIC. Por lo tanto, planteamos la hipótesis de que la detección de los cambios dinámicos de la placa podría identificar a pacientes con riesgo de sufrir posteriores episodios coronarios. En consecuencia, diseñamos este estudio de EIC para evaluar las consecuencias clínicas y los factores predictivos del CTP en pacientes con DM2 y enfermedad coronaria conocida.
MétodosPoblación en estudioSe incluyeron en este estudio pacientes con DM2 que participaban en los ensayos DIABETES (DIABETes and sirolimus Eluting Stent) I, II y III10, 11, 12 en los que se llevó a cabo una evaluación mediante EIC. El diagrama de flujo del estudio y los criterios de inclusión y exclusión se han descrito ya con anterioridad13. De forma resumida, se seleccionaron para el estudio las lesiones leves no tratadas (estenosis angiográfica < 25% mediante evaluación visual), con grosor de la placa ≥ 0,5 mm y longitud ≥ 5 mm según la evaluación de EIC. Los segmentos coronarios elegibles para los análisis seriados debían estar situados al menos a 10 mm, distal o proximal al segmento tratado anteriormente con un stent y no debían haberse visto afectados por una lesión causada por el balón durante la intervención inicial. Excluimos del análisis las lesiones con artefactos relacionados con la EIC, como la distorsión rotacional no uniforme, el artefacto de ring down, las lesiones con circunferencia incompleta y la retirada del catéter de EIC que no incluía la lesión en el seguimiento, así como las lesiones que fueron tratadas antes de los 9 meses de seguimiento. Se excluyó también a los pacientes en los que se hinchó el balón múltiples veces durante procedimientos complejos habiendo dudas acerca de la ubicación del balón hinchado. Los protocolos del estudio fueron aprobados por los comités éticos médicos de los centros participantes y todos los pacientes dieron su consentimiento informado por escrito.
Imágenes y análisis de la ecografía intracoronariaSe realizaron análisis cualitativos y cuantitativos de las retiradas del catéter motorizadas (0,5mm/s) tras la intervención inicial y en el seguimiento angiográfico a los 9 meses, en el mismo segmento coronario. En todos los casos, el sistema de EIC utilizado fue la consola ClearView™ (CVIS, Sunnyvale, California) y el catéter Atlantis-Pro 40MHz ™ (CVIS, Sunnyvale, California, Estados Unidos). Se analizaron de manera seriada las placas angiográficamente no significativas que no estaban relacionadas con el lugar del tratamiento. La placa individual se definió como un ateroma continuo con grosor de la placa más la capa media > 0,5mm y longitud ≥ 5 mm y sin ramificaciones en ella. Se exigió que hubiera un segmento intermedio no afectado de al menos 5 mm para diferenciar las placas. Se utilizaron como referencia segmentos adyacentes sin ramas laterales significativas que cumplieran los criterios de normalidad y tuvieran una longitud > 2,5 mm.
Además, dado que puede haber diferentes tipos de placas dentro de una determinada lesión coronaria, cada lesión estudiada se dividió en tres segmentos para los análisis cuantitativos y cualitativos14. Este análisis seriado de la EIC fue realizado por un laboratorio central independiente (University of Florida Health Science Center at Shands Jacksonville, Florida, Estados Unidos), que no conocía los datos clínicos ni de laboratorio. Para los análisis se siguió una metodología descrita con anterioridad15. A partir de las imágenes digitalizadas, se midió el área de la luz, la placa y la membrana elástica externa (MEE) a intervalos de 0,5 mm en cada segmento coronario. Se calcularon los valores medios del área de la luz, la placa y la MEE en la situación basal y en el seguimiento realizado a los 9 meses. Se registró la distancia de la placa al stent implantado previo y la distancia de la placa a cualquier rama lateral, con objeto de garantizar que los análisis correspondieran al mismo segmento coronario en el seguimiento. Se efectuó un análisis cuantitativo de EIC tridimensional con el empleo de un sistema de análisis de EIC dedicado (QIVA, Pie Medical Imaging, Maastricht, Países Bajos). Este sistema permite delimitar de forma semiautomática la luz y el vaso, así como realizar un análisis cuantitativo de sus dimensiones en una proyección longitudinal y transversal. La localización de las áreas transversales mínima y máxima (luz, placa y MEE) se definió automáticamente con un algoritmo informatizado. Las mediciones se hicieron a lo largo de toda la placa y todas las referencias relacionadas. Los volúmenes se determinaron con la suma de las áreas transversales medidas en la región en la que se realizaba la retirada del catéter, basándose en la regla de Simpson. Para los cortes transversales calcificados, se interpoló el contorno de la MEE basado en los cortes sin calcificación. Además, los segmentos fueron clasificados cualitativamente en cuatro categorías morfológicas por dos observadores experimentados: placas blandas, fibrosas, mixtas y calcificadas. La variabilidad intraobservador se evaluó mediante el análisis de una serie de 40 segmentos con al menos 3 meses de separación. El porcentaje de coincidencia es > 95% (κ=0,946 para el tipo de placa basal y κ=0,965 para el tipo de placa en el seguimiento); en los casos de desacuerdo entre los dos observadores se solicitó la opinión de un tercero.
DefinicionesEl tipo de placa se definió de la siguiente manera16: tejido blando cuando al menos un 80% del área estaba formado por un material que mostraba una reflectividad ecogénica inferior a la de la adventicia, con un arco de calcio < 10°; placa fibrosa cuando la reflectividad ecogénica de al menos un 80% del material era brillante o más brillante que la adventicia, sin sombra acústica; placa calcificada difusa cuando contenía un material más brillante que la adventicia, con sombra acústica > 90°, y mixta cuando la placa no satisfacía el criterio del 80%. El CTP se definió como cualquier cambio cualitativo en el tipo de placa entre la intervención inicial y el seguimiento realizado a los 9 meses. Los cambios vasculares seriados se clasificaron como CTP o no CTP.
Los cambios vasculares seriados cuantitativos se clasificaron como una reducción o un aumento de tamaño del vaso. La reducción de tamaño del vaso se definió como el cociente entre el cambio del área del vaso respecto al cambio del área del ateroma < 013, 17.
Los eventos cardiacos adversos mayores (MACE) se definieron como muerte cardiaca, infarto de miocardio (IM) y revascularización del vaso diana (RVD), y su adjudicación se realizó a los 12 meses de seguimiento.
Análisis estadísticoEl análisis estadístico se realizó con las versiones de los programas SPSS 12.0 y SAS 9.1. Los datos cuantitativos se presentan en forma de media±desviación estándar y los cualitativos, como porcentajes. Con objeto de tener en cuenta la variabilidad intraindividual (evaluaciones repetidas), todas las comparaciones (univariables y multivariables) se ajustaron mediante un modelo de ecuaciones de estimación generalizada, con estratificación por paciente, lesión y segmento18. Para evaluar la asociación entre el CTP y los datos clínicos, de laboratorio y cuantitativos de EIC, se utilizó un modelo de regresión logística multivariable. Las variables con un valor de probabilidad < 0,1 en el análisis univariable o clínicamente relevantes fueron incluidas en los análisis: cifras de glucohemoglobina, lipoproteínas de baja densidad (LDL) y triglicéridos, edad, tabaquismo, hipercolesterolemia, angina estable y DM, área media basal del vaso, área media basal de la placa, tipo basal de placa y uso de estatinas, inhibidores de la enzima de conversión de la angiotensina (IECA) e inhibidores de la glucoproteína (GP) IIb/IIIa. Se consideró estadísticamente significativo un valor de p bilateral < 0,05.
ResultadosCaracterísticas basales y resultados de la ecografía intracoronariaSe efectuaron análisis seriados de EIC de 237 segmentos ateroscleróticos de 45 pacientes en la situación basal y de los mismos segmentos en el seguimiento realizado a los 9 meses. Las características basales de los pacientes incluidos se han descrito en una publicación anterior13 (Tabla 1).
Tabla 1. Características clínicas basales (n=45)
| Edad (años) | 67,4±9,1 |
| Mujeres | 19 (22,2) |
| DMID | 13 (28,9) |
| Hiperlipemia | 29 (64,4) |
| Hipertensión | 30 (66,7) |
| Tabaquismo | 26 (57,8) |
| IM previo | 19 (42,2) |
| Revascularización previa | 8 (17,8) |
| Angina estable | 11 (24,4) |
| Enfermedad multivaso | 30 (66,7) |
| FEVI (%) | 66,6±14,1 |
| Estatinas | 37 (82,2) |
| Inhibidores de la GPIIb/IIIa | 26 (57,8) |
| Glucohemoglobina | 7,2±1,4 |
DMID: diabetes mellitus insulinodependiente; FEVI: fracción de eyección ventricular izquierda; GPIIb/IIIa: glucoproteína IIb/IIIa; IM: infarto de miocardio.
Los datos se presentan en forma de media±desviación estándar o n (%).
La media de longitud de las lesiones fue de 10,3 mm. El tipo de placa observado con mayor frecuencia fue el mixto (39,2%), seguido del calcificado (31,3%), el fibroso (16,5%) y el blando (13,1%). Se produjo un CTP en 48 lesiones (20,2%) (Figura 1). El tipo de placa que se modificó con más frecuencia durante el seguimiento fue el mixto (52,1%), seguido del fibroso (22,9%). El CTP se produjo con menor frecuencia en las placas blandas y calcificadas (el 12,5% en ambos tipos). En la Tabla 2 se presentan los resultados cuantitativos de la EIC. Los valores del cambio de las dimensiones vasculares fueron comparables en el grupo con CTP y el grupo sin CTP: área del vaso (1,3±3,5 frente a 1,1±3,6; p=0,66), área de la placa (0,6±2,1 frente a 0,4±2,1; p=0,86) y área de la luz (0,7±2,5 frente a 0,6±2,5; p=0,7).
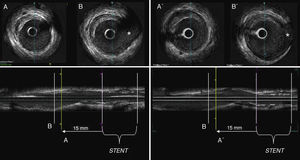
Figura 1. Ejemplo de una exploración de ecografía intracoronaria en un paciente incluido en el estudio, que muestra un cambio en el tipo de placa, que pasa de fibrosa a blanda. En el panel izquierdo se muestra la exploración basal en la que se aprecia una placa fibrosa situada proximalmente al stent (15 mm) y proximal a un punto de referencia: B (asterisco: rama lateral). En el panel derecho se muestra la exploración de seguimiento en la que se aprecia una lesión blanda (B) situada en la misma posición. B’ corresponde al punto de referencia en el seguimiento.
Tabla 2. Mediciones cuantitativas de ecografía intracoronaria
| Cambio en el tipo de placa (n=48) | Ausencia de cambio en el tipo de placa (n=189) | p | |
| Basal | |||
| Área de MEE (mm2) | 19,3±3,5 | 20,5±5,1 | 0,07 |
| Área de placa (mm2) | 9,3±3,1 | 10,3±3,4 | 0,07 |
| Área de luz (mm2) | 10±2,7 | 10,1±3,8 | 0,78 |
| Seguimiento | |||
| Área de MEE (mm2) | 20,6±4,4 | 21,5±5 | 0,15 |
| Área de placa (mm2) | 9,9±3,3 | 10,8±3,5 | 0,22 |
| Área de luz (mm2) | 10,7±3,4 | 10,8±3,9 | 0,91 |
| Reducción de tamaño del vaso | 16 (33,3) | 72 (38,1) | 0,7 |
MEE: membrana elástica externa.
Los datos se expresan en forma de media±desviación estándar o n (%). Todas las estadísticas se calcularon con el método de ecuaciones de estimación generalizada, estratificando según pacientes, vaso y segmento.
El análisis clínico de los grupos con y sin CTP se muestra en la Tabla 3. El grupo con CTP tenía una edad significativamente mayor y mayor prevalencia de DM insulinodependiente, así como menor prevalencia de hiperlipemia, tabaquismo y uso de estatinas, IECA e inhibidores de la GPIIb/IIIa. Se observaron cifras de colesterol unido a LDL inferiores y tendencia a valores más altos de glucohemoglobina basal en el grupo de CTP. No hubo relación alguna entre los cambios vasculares cuantitativos y el CTP ni entre el tipo de placa basal y el CTP. En los análisis multivariables, los factores asociados de manera independiente al CTP fueron los valores de glucohemoglobina (p=0,04), el uso de inhibidores de la GPIIb/IIIa (p=0,004) y el uso de estatinas (p=0,02) (Tabla 4).
Tabla 3. Análisis univariable estratificado entre las lesiones con cambio en el tipo de placa y las lesiones que no presentaron cambio en el seguimiento
| Cambio en el tipo de placa (n=48) | Sin cambio en el tipo de placa (n=189) | p | |
| Edad (años) | 69,4±7 | 66,5±9,7 | 0,024 |
| Varones | 43 (75,4) | 146 (81,1) | 0,35 |
| DMID | 18 (31,6) | 35 (18,5) | 0,028 |
| Hiperlipemia | 23 (47,9) | 136 (72) | 0,002 |
| Hipertensión | 33 (68,8) | 126 (66,7) | 0,78 |
| Tabaquismo | 23 (47,9) | 136 (72) | 0,007 |
| IM previo | 17 (35,4) | 79 (41,8) | 0,42 |
| Revascularización previa | 17 (35,4) | 79 (41,8) | 0,42 |
| Angina estable | 18 (37,5) | 45 (23,8) | 0,057 |
| Enfermedad multivaso | 35 (72,9) | 133 (70,4) | 0,72 |
| FEVI (%) | 63,8±16,9 | 66±16,6 | 0,4 |
| Estatina | 32 (66,7) | 172 (91) | < 0,001 |
| IECA | 23 (47,9) | 121 (64) | 0,04 |
| Inhibidores de la GPIIb/IIIa | 21 (43,8) | 111(58,7) | 0,06 |
| Colesterol total (mg/dl) | 175,9±52,8 | 166,1±29,5 | 0,15 |
| Triglicéridos (mg/dl) | 124,7±48,9 | 141,3±61,6 | 0,09 |
| cHDL (mg/dl) | 41,9±9,3 | 42,54±12,6 | 0,74 |
| cLDL (mg/dl) | 108,5±45 | 195±32,3 | 0,03 |
| Apolipoproteína A (mg/dl) | 118,4±27,3 | 119,1±24,4 | 0,88 |
| Apolipoproteína B (mg/dl) | 98,3±32,7 | 93,6±21,6 | 0,38 |
| Glucohemoglobina (%) | 7,8±1,2 | 7,4±1,4 | 0,059 |
| PCRhs | 0,7±0,7 | 1,1±1,5 | 0,23 |
cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; DMID: diabetes mellitus insulinodependiente; FEVI: fracción de eyección ventricular izquierda; GPIIb/IIIa: glucoproteína IIb/IIIa; IECA: inhibidores de la enzima de conversión de la angiotensina; IM: infarto de miocardio; PCRhs: proteína C reactiva de alta sensibilidad.
Los datos se presentan en forma de media±desviación estándar o n (%). Todas las estadísticas se calcularon con el método de ecuaciones de estimación generalizada, estratificando por pacientes, vaso y segmento.
Tabla 4. Análisis multivariables estratificados para los predictores del cambio en el tipo de placa
| OR | IC del 95% | p | |
| Glucohemoglobina | 1,25 | 1,01-1,56 | 0,04 |
| Triglicéridos | 0,99 | 0,98-1 | 0,08 |
| Hipercolesterolemia | 0,55 | 0,25-1,19 | 0,12 |
| Tabaquismo | 0,59 | 0,28-1,27 | 0,18 |
| Área del vaso basal | 0,93 | 0,86-1,01 | 0,08 |
| Estatina | 0,35 | 0,14-0,88 | 0,02 |
| Inhibidores de la GPIIb/IIIa | 0,34 | 0,16-0,72 | 0,004 |
GPIIb/IIIa: glucoproteína IIb/IIIa; IC: intervalo de confianza; OR: odds ratio.
Todas las estadísticas se calcularon con el método de ecuaciones de estimación generalizada, con estratificación por pacientes, vaso y segmento.
En el seguimiento clínico realizado a 1 año, hubo un aumento significativo del total de MACE en el grupo de CTP (13 [27,1%] frente a 29 [15,3%]; p<0,001) debido principalmente a un aumento significativo de la necesidad de RVD (10 [20,8%] frente a 26 [13,8%]; p=0,008). En el grupo de CTP, la RVD se debió a la progresión de la aterosclerosis en otros segmentos coronarios en 6 casos y fue necesaria una revascularización de la lesión diana a causa de restenosis en 4 casos. En el grupo sin CTP, la RVD se debió a la progresión de la aterosclerosis en otros segmentos coronarios en 20 casos, mientras que en 6 casos se realizó una revascularización de la lesión diana. Tan solo en 1 caso estuvo relacionada la arteria causal de un IM con placas leves previas analizadas y confirmadas por EIC. No se produjo ninguna muerte cardiaca en ninguno de los dos grupos. Además, hubo tendencia a mayor frecuencia de IM en el grupo de CTP (3 [6,3%] frente a 3 [1,6%]; p=0,08).
El CTP también fue un factor independiente asociado a los MACE a 1 año (hazard ratio =1,9; intervalo de confianza del 95%, 1,3-9,9; p=0,01) con ajuste para la edad, el tipo de DM y la enfermedad multivaso. En la Tabla 5 se indica el sentido de los cambios de la placa y los eventos clínicos tras 1 año de seguimiento en el grupo de CTP.
Tabla 5. Sentido de los cambios de la placa y eventos clínicos en el seguimiento a 1 año
| Tipo de placa | Tipo de placa en el seguimiento | Número de eventos a 1 año en el grupo de CTP (n=13) |
| Blanda (n=6) | Mixta (n=6) | Eventos n=3 (n=2 RVD; n=1 RLD) |
| Mixta (n=25) | Blanda (n=17) | Eventos n=3 (n=1 RVD; n=1 IM; n=1 RLD) |
| Fibrosa (n=4) | - | |
| Calcificada (n=4) | Eventos n=2 (n=1 RVD; n=1 RVD) | |
| Fibrosa (n=11) | Mixta (n=10) | Eventos n=4 (n=1 RVD; n=1 RLD; n=2 IM) |
| Calcificada (n=1) | - | |
| Calcificada (n=6) | Mixta (n=6) | Eventos n=1 RLD |
CTP: cambio en el tipo de placa; IM: infarto de miocardio; RLD: revascularización de lesión diana; RVD: revascularización de vaso diana.
Eventos exclusivos.
Los principales resultados del presente estudio son los siguientes: a) un 20% de las placas estudiadas presentaron cambios cualitativos en el seguimiento realizado a los 9 meses; b) el mal control de la glucemia presentó una asociación positiva con este cambio, mientras que el empleo de estatinas e inhibidores de la GPIIb/IIIa previno su aparición, y c) por último, el CTP parecía estar relacionado con los resultados clínicos a 1 año.
Se ha propuesto que es el tipo de placa, más que la gravedad de la estenosis subyacente, lo que desempeña un papel en la propensión a la vulnerabilidad y, por lo tanto, al desarrollo de un síndrome coronario agudo5, 6, 19, 20. Los estudios de anatomía patológica han puesto de manifiesto que las placas ricas en lípidos son más propensas a la rotura que las placas fibrosas21. Los estudios de EIC describieron que las placas con contenido de zonas ecolucentes tienen mayor tendencia a la inestabilidad. Además, el tipo de placa determinado con la EIC se asocia a los eventos clínicos. Nakamura et al22 pusieron de relieve que las placas blandas son más propensas al remodelado positivo y a síndrome coronario agudo y constituyen un factor predictivo de la reestenosis intrastent23.
Este es el primer estudio que muestra que el CTP en los pacientes con DM2 y enfermedad coronaria conocida tiene repercusiones clínicas. El cambio que se produce en una placa aterosclerótica no parece ser un fenómeno aislado limitado a un único segmento coronario, sino más bien una «pancoronaritis», según lo señalado por estudios recientes de EIC y angioscopia24, 25, 26. En este sentido, los pacientes con síndrome coronario agudo examinados mediante EIC presentaron roturas de placas en localizaciones distintas de las de la lesión causal, incluso en arterias diferentes. Esto indica que los factores sistémicos, además de los locales, probablemente influyeran en todo el árbol coronario y causaran una desestabilización difusa de las placas coronarias. Esta conclusión está respaldada por estudios previos que ponen de manifiesto una activación amplia de los neutrófilos en todo el árbol coronario, con independencia de la lesión causal, en los pacientes con angina inestable27. Cabe plantear la hipótesis de que el CTP en las lesiones leves alejadas de un segmento coronario tratado con anterioridad pueda ser un reflejo de un proceso que afecte a todo el vaso.
Los pacientes con DM2 tienen una enfermedad aterosclerótica más agresiva y mayor riesgo de complicaciones trombóticas28. La hiperglucemia desempeña un papel importante en la fisiopatología de la enfermedad vascular en la DM que comporta anomalías de las funciones endotelial y plaquetaria. La hiperglucemia induce una disfunción endotelial a través de múltiples mecanismos. Aumenta el estrés oxidativo, lo que da lugar a inflamación de la adventicia y neovascularización de los vasa vasorum, procesos ambos que se asocian a la inestabilidad de la placa29. Además, el mal control de la glucemia es un factor importante en la activación de las plaquetas, que son clave en la aterogénesis, la progresión de la placa y las complicaciones trombóticas30. En el presente estudio, los valores más elevados de glucohemoglobina condujeron al CTP, lo cual resalta el importante papel del control metabólico para mejorar los resultados obtenidos en los pacientes con DM2.
La administración de estatinas se ha asociado a regresión de la placa y estabilización de la placa como consecuencia de la reducción del contenido lipídico9. En el presente estudio, el uso de estatinas fue un factor preventivo para la aparición del CTP y, por lo tanto, se asoció a un mejor resultado. Una posible explicación es que nuestros pacientes recibían un tratamiento crónico con estatinas (el 61,8 simvastatina y el 38,2% atorvastatina: 20-40mg) y las concentraciones de LDL se mantuvieron estables: solamente en 2 pacientes se aumentó la dosis debido a un control lipídico insuficiente. Además, las placas con mayor contenido de lípidos, como las placas blandas, son infrecuentes en nuestra población, y esto puede ser otra explicación de nuestros resultados. Las propiedades antiinflamatorias de las estatinas también pueden ser importantes, al prevenir todo CTP31.
La administración de inhibidores de la GPIIb/IIIa tiene dos efectos principales: el efecto antitrombótico debido a la inhibición del receptor de la integrina de la GPIIb/IIIa, que causa una inhibición potente de la agregación plaquetaria y de la formación de trombos, y el efecto antiinflamatorio debido a la inhibición de la interacción entre plaquetas y leucocitos. En los pacientes con angina inestable, IM o angioplastia coronaria transluminal percutánea (ACTP), se ha descrito una respuesta inflamatoria sistémica con aumento de proteína C reactiva de alta sensibilidad, interleucina 6 y factor de necrosis tumoral32. De igual modo, el grado de activación de células inflamatorias después de una intervención percutánea se ha asociado a aumento de la tasa de eventos en el seguimiento tanto a corto como a largo plazo33. En cambio, la administración de inhibidores de la GPIIb/IIIa durante una intervención coronaria percutánea se asoció a supresión del aumento observado en los marcadores de la inflamación en el periodo periintervención. Otras propiedades de los inhibidores de la GPIIb/IIIa son la reducción de sCD40L y de agregados de leucocitos-plaquetas circulantes34, fenómenos ambos que desempeñan un papel importante en el desarrollo y la progresión de la aterosclerosis. En nuestro estudio, los inhibidores de la GPIIb/IIIa se administraron según el protocolo, independientemente de la complejidad de la intervención de ACTP, y evitaron la aparición de un CTP. En resumen, nosotros proponemos que el CTP refleja un cambio en el vaso y/o la activación de la placa que puede estar relacionado con los eventos clínicos. En consecuencia, los factores asociados a la inestabilidad de la placa y la progresión de esta, como los valores más altos de glucohemoglobina, pueden explicar la asociación con el CTP.
Limitaciones del estudioSe trata de un estudio observacional, en el que la principal limitación radica en el posible sesgo de selección, por dos razones: solamente se incluyeron arterias aptas para una exploración de EIC y se excluyó a los pacientes en los que se había hinchado múltiples veces un balón durante operaciones complejas cuando quedaban dudas acerca de la ubicación exacta del balón hinchado. En el presente estudio solamente se evaluaron las lesiones leves; en consecuencia, los resultados obtenidos en este estudio no pueden extrapolarse a las lesiones más graves. El tipo de placa no se asoció al CTP. Esta observación puede estar relacionada con el pequeño tamaño muestral. De igual modo, solamente 6 placas blandas y 6 placas calcificadas presentaron un cambio en el examen de seguimiento respecto a la situación basal; por lo tanto, dado el pequeño tamaño muestral, no podemos evaluar las implicaciones de los diferentes sentidos del cambio de la placa. Probablemente el sentido del CTP no tenga las mismas consecuencias clínicas y esto constituye una limitación de este estudio. Es posible que sean necesarios nuevos estudios con mayor número de pacientes o un seguimiento más largo para determinar las consecuencias clínicas de un sentido específico del cambio. Sin embargo, pudimos demostrar un CTP en un porcentaje bastante elevado de placas, así como una relación entre este cambio y los resultados clínicos. Estos resultados respaldan el paradigma del proceso de aterosclerosis acelerada que se produce en la población con DM2.
La EIC estándar basada en la escala de grises tiene limitaciones en lo que respecta a la caracterización del tejido. La sensibilidad, la especificidad y la reproducibilidad de la caracterización de la placa son bajas con la evaluación basal de la imagen de escala de grises, sobre todo para las placas ricas en lípidos. Por este motivo, el presente estudio no evalúa el cambio de la composición de la placa. Este estudio pretende evaluar las consecuencias clínicas del CTP estudiado mediante la EIC basada en la escala de grises, con todas las limitaciones que tiene esa técnica, incluido el hecho de que la calidad de imagen de la EIC puede reducirse por diversos artefactos y depende de la posición del transductor dentro de la arteria coronaria. Además, la posición excéntrica, no coaxial, del catéter, comporta una distorsión geométrica y puede afectar a la ecogenicidad de la pared del vaso. Por otra parte, las imágenes obtenidas in vivo pueden sufrir cambios durante el ciclo cardiaco. A pesar de estas limitaciones, la EIC basada en la escala de grises se ha utilizado para caracterizar la composición de la placa en ensayos multicéntricos amplios9, 22, 23, 35.
ConclusionesLos cambios cualitativos en la estenosis leve documentados mediante EIC en los pacientes con DM2 se asocian a una prevención secundaria subóptima y pueden tener consecuencias clínicas. El papel de las nuevas tecnologías, como la tecnología de EIC Virtual Histology™ o la combinación de tomografía de coherencia óptica y EIC, en este contexto está aún por determinar.
Conflicto de interesesNinguno.
Recibido 2 Septiembre 2010
Aceptado 21 Enero 2011
Autor para correspondencia: Servicio de Cardiología Intervencionista, Hospital Clínico San Carlos, Plaza Cristo Rey s/n, 28040 Madrid, España. manelsabate1@telefonica.net