La tomografía computarizada presenta dificultades para determinar qué lesiones coronarias condicionan repercusión en el miocardio, y es necesario realizar pruebas de inducción de isquemia. El objetivo del estudio es analizar la seguridad diagnóstica de la tomografía computarizada de doble fuente para valorar perfusión y viabilidad miocárdica en sospecha de cardiopatía isquémica, en comparación con la resonancia magnética.
MétodosEstudio prospectivo de 56 pacientes consecutivos, 39 varones (69,6%), de 23-81 (media, 63±10) años de edad. Se realizó tomografía computarizada (con el protocolo: 1, perfusión de estrés con adenosina; 2, coronariografía y 3, realce tardío) y resonancia magnética con perfusión de estrés y realce tardío en menos de 30 días. Dos observadores en consenso analizaron la perfusión y el realce tardío.
ResultadosSe analizaron 952 segmentos miocárdicos y 168 territorios vasculares. En un análisis por segmentos, sensibilidad, especificidad, valores predictivos positivo y negativo de la tomografía en comparación con la resonancia para detectar defectos de perfusión fueron del 76, el 99, el 89 y el 98%, y para realce tardío, el 64, el 99, el 82 y el 99%. Por territorios vasculares, el 78, el 97, el 86 y el 95% (defectos de perfusión) y el 72, el 99, el 93 y el 97% (realce tardío). La dosis media de radiación fue 8,2±2 mSv.
ConclusionesLa tomografía computarizada de doble fuente permite analizar defectos de perfusión y viabilidad miocárdica de manera precisa y valorar conjuntamente la anatomía coronaria.
Palabras clave
La coronariografía por tomografía computarizada (TC) es una técnica útil para valorar las arterias coronarias de pacientes sin enfermedad coronaria conocida. Su alto valor predictivo negativo excluye con seguridad enfermedad coronaria en pacientes cuya prueba es normal1. Sin embargo, de haberla, es difícil predecir qué estenosis darán como resultado un deterioro del flujo miocárdico2, especialmente cuando existen importantes calcificaciones o son de gravedad intermedia. La cuantificación de la estenosis no indica de manera certera la isquemia miocárdica. El papel del diagnóstico por imagen en la isquemia miocárdica no es completo si no se verifica la limitación funcional causada por la estenosis coronaria3.
El estado hemodinámico de la enfermedad coronaria se puede valorar con las imágenes de perfusión miocárdica (IPM) durante el estrés inducido por el ejercicio o fármacos4. Las técnicas para detectar defectos de perfusión miocárdica en la práctica clínica habitual son la tomografía computarizada por emisión monofotónica (single photon emission computed tomography [SPECT]) y la resonancia magnética (RM), que tiene el valor añadido de obtener imágenes de realce tardío, que ayudan a diagnosticar la necrosis miocárdica5–7.
Estudios recientes de IPM con TC han demostrado que se puede representar el miocardio isquémico y que los resultados coinciden con los de la SPECT y la angiografía coronaria convencional8–10. La TC de doble fuente (TCDF), con dos tubos de rayos X y sus correspondientes paneles de detectores, presenta ventajas importantes: realizar adquisiciones con alto pitch y baja dosis de radiación11 y la adquisición con TC de doble energía (TCDE), que consiste en que cada tubo de rayos X funciona con energías diferentes. Con esta técnica se puede generar mapas de color que permiten la evaluación del estado de la perfusión miocárdica mediante el análisis del volumen de yodo que hay en el miocardio.
Estudios recientes de IPM con TCDE indican una elevada precisión para detectar isquemia miocárdica12. Además, la combinación de la IPM con TCDE incrementa el valor diagnóstico de la TC-coronariografía para detectar estenosis coronarias significativas13. Por otro lado, la adquisición de alto pitch ha mostrado buena precisión en la valoración de la viabilidad miocárdica con baja dosis de radiación en comparación con la RM, aunque conlleva más «ruido» en la imagen14. La obtención del análisis de la anatomía coronaria, la repercusión funcional de las lesiones y la necrosis-viabilidad miocárdica combinados en una única prueba podría ser el deseado «one-stop shop» de las exploraciones complementarias en enfermedad coronaria.
El objetivo de este trabajo fue evaluar la precisión diagnóstica de la TCDF para valorar la perfusión y la viabilidad miocárdica en pacientes con sospecha clínica de cardiopatía isquemica, en comparación con la RM.
MÉTODOSPoblación de estudioSe realizó un estudio prospectivo que incluyó a los pacientes que acudieron a la consulta de cardiología por sospecha clínica de isquemia e indicación de prueba de estrés. A todos se les propuso realizar una TCDF y una RM cardiaca con un intervalo entre pruebas < 30 días. Se excluyó a los pacientes con asma, alergia al contraste yodado o el gadolinio, ritmo cardiaco irregular, marcapasos, insuficiencia renal con filtrado glomerular < 60 ml/min, miocardiopatía hipertrófica, miocardiopatía dilatada con fracción de eyección del ventrículo izquierdo < 30% o insuficiencia cardiaca en grado funcional III o IV.
El protocolo del estudio fue aprobado por el comité de ética institucional y todos los pacientes dieron su consentimiento informado por escrito antes de la inclusión.
Estudios de imagenProtocolo de tomografía computarizada cardiacaSe instruyó a los pacientes para que no tomasen café, té ni bloqueadores beta orales en las 24 h previas a la exploración. Se tomaron en el brazo derecho dos accesos venosos (18-G para administración del contraste, 20-G para infusión de adenosina). Se midió la frecuencia cardiaca y la presión arterial.
Todas las exploraciones se realizaron en un equipo 128-TCDF (Flash Definition®, Siemens; Forcheim, Alemania) con el siguiente protocolo:
Tomografía computarizada de doble energía con estrés para valorar la perfusión miocárdicaUna vez realizado el topograma y planificado el estudio desde la bifurcación traqueal hasta el diafragma en dirección craneocaudal, se administró adenosina mediante una bomba de perfusión (Alaris System, Cardinal Health; Ohio, Estados Unidos) a una velocidad constante a dosis de 140 μg/kg/min; 3 min después, se administró contraste yodado: 60 ml de iopromida (Ultravist 370, Bayer Schering Pharma; Berlín, Alemania), seguido de 60 ml de suero salino, a 4 ml/s, utilizando una inyectora (Stellant Dual, Medrad; Pennsylvania, Estados Unidos). Se realizó una adquisición retrospectiva sincronizada con el electrocardiograma con técnica de energía dual y modulación de la dosis, con las siguientes características técnicas: tiempo de rotación, 330ms; pitch adaptativo a la frecuencia cardiaca, 0,2-0,43; colimación, 0,6 mm; resolución temporal, 165 ms. Un tubo funcionando con 165 mAs/rot a 100 kV y el otro con 140 mAs/rot a 140 kV. La modulación de dosis se realizó con técnica MinDose utilizando toda la corriente del tubo entre el 60 y el 75% del ciclo cardiaco y reduciéndola al 4% fuera de esa ventana temporal.
Para conseguir un adecuado realce, se utilizó bolus tracking colocando una región de interés en el arco aórtico con un umbral de disparo a 160 UH. Se añadió un retraso de 10 s para garantizar la adecuada perfusión del miocardio.
La infusión de adenosina se finalizó al terminar la adquisición. se vigiló cuidadosamente la presión arterial, el electrocardiograma y los síntomas clínicos.
Para la reconstrucción de las imágenes, se usó un algoritmo de reconstrucción monosegmentario que utiliza datos de una rotación completa de ambos detectores. Los datos fueron reconstruidos en diástole entre el 60 y el 75% del intervalo R-R, con grosor de corte de 3 mm, incremento de reconstrucción de 1,5 mm y filtro de reconstrucción D30f.
Tomografía computarizada-coronariografía para valorar la anatomía coronariaTranscurridos 5 min, se realizó TC-coronariografía. Si no existía contraindicación y la frecuencia cardiaca era > 65 lpm, se administraba bloqueador beta (5-15 mg de metoprolol intravenoso). En caso de que la frecuencia cardiaca fuera estable y < 65 lpm, se realizó adquisición prospectiva con técnica de alto pitch. En caso de que no fuera posible, se realizaba adquisición helicoidal electrocardiograma-retrospectivo. A todos se administró 0,5-1mg de nitroglicerina sublingual.
Los parámetros técnicos para la adquisición prospectiva con alto pitch fueron: colimación, 0,6 mm (128×0,6 mm); tiempo de rotación, 280 ms; corriente efectiva, 370 mAs con técnica de modulación CARE DOSE, 100 o 120 Kv según el peso fuera < 80 o > 80 kg respectivamente; pitch, 3,4 y resolución temporal, 75 ms. La adquisición se realizó en sentido caudocraneal comenzando al 60% del intervalo R-R.
En la adquisición retrospectiva, los parámetros técnicos fueron: colimación, 0,6 mm (128×0,6 mm); tiempo de rotación tubo, 280 ms, 100 o 120 Kv según el peso fuera < 80 o > 80 kg respectivamente; corriente efectiva, 370 mAs; pitch adaptativo a frecuencia cardiaca, 0,2-0,43; modulación de dosis MinDose utilizando la máxima corriente del tubo entre el 60 y el 75% del ciclo cardiaco y reduciéndola al 4% fuera de esa ventana temporal.
El realce vascular se consiguió administrando 60 ml de iopromida (Ultravist 370, Bayer Schering Pharma), seguidos de 60 ml de suero salino, a flujo constante de 6 ml/s. Se utilizó bolus tracking colocando una región de interés en aorta ascendente con un umbral de disparo de 100 UH.
En todos los casos la reconstrucción de las imágenes se realizó con grosor de corte de 0,6 mm, incremento de reconstrucción de 0,4 mm y filtro de reconstrucción de B26f. Cuando la adquisición fue retrospectiva, la reconstrucción se obtuvo en la fase del ciclo cardiaco donde mejor se valoraban las arterias coronarias.
Se consideró estenosis significativa cuando en el análisis cuantitativo fue > 50%.
Las imágenes del miocardio de esta serie se evaluaron como perfusión en reposo.
Tomografía computarizada para valorar la viabilidad miocárdicaSiete minutos después, se realizó una adquisición prospectiva con técnica de alto pitch, con las mismas características que la TC-coronariografía, a excepción de que se utilizó baja dosis de radiación con 80 kV y 300 mAs/rot. No se administró contraste intravenoso ni ningún otro fármaco.
La reconstrucción de las imágenes se realizaron con grosor de corte de 0,6 mm, incremento de reconstrucción de 0,4 mm y filtro de reconstrucción B26f.
Protocolo resonancia magnética cardiacaSe realizaron con una RM de 1,5 T (Achieva, Philips Medical Systems; Eindohven, Países Bajos), utilizando antena de superficie de cinco elementos específica para estudios cardiacos (SENSE Cardiac, Philips Medical Systems), con el siguiente protocolo:
Perfusión de primer paso en estrésSe administró adenosina intravenosa mediante bomba de perfusión (Alaris System, Cardinal Health) a dosis de 140 μg/kg/min. La presión arterial, frecuencia cardiaca y saturación de oxígeno se monitorizaron a intervalos de 1 min. A los 3 min, se inyectó un bolo de contraste intravenoso de 0,05 mmol/kg de gadobutrol (Bayer Schering Pharma) a 4 ml/s más 40 ml de suero salino a 4 ml/s, mediante vena antecubital en el brazo contrario a la infusión de adenosina. Se realizó la perfusión de primer paso utilizando una secuencia turbo-eco de gradiente (TEG) potenciada en T1 (tiempo de repetición, 2,2 ms; tiempo de eco, 1,04 ms; ángulo, 50°; grosor de corte, 10 mm) en el eje corto incluyendo base, tercio medio y ápex del ventrículo izquierdo. Las imágenes se adquirieron en la telediástole para maximizar la señal intravascular.
Perfusión de primer paso en reposoAproximadamente 5 min después de realizar la perfusión de estrés, se administró nuevamente contraste y se realizó la perfusión basal con la misma técnica.
Viabilidad miocárdicaTras una espera de 10 min, se adquirieron las imágenes de realce tardío. Antes de adquirir las imágenes de viabilidad, se calculaba el valor del tiempo óptimo de inversión, que mejor anulaba la señal del miocardio, con una secuencia ecoplanar-TEG (tiempo de repetición, 40 ms; tiempo de eco, 5 ms; ángulo, 15°; grosor de corte, 10 mm). La secuencia del realce tardío fue una TEG tridimensional potenciada en T1 y con preparación tisular (tiempo de repetición, 3,9-4,3 ms; tiempo de eco, 1,2-1,3 ms; ángulo, 15°; grosor de corte, 10 mm). Todas se adquirieron en apnea y en los ejes corto y largo del ventrículo izquierdo y en plano de cuatro cámaras.
Posprocesado de las imágenes e interpretaciónLas reconstrucciones de la TC y la RM fueron interpretadas independientemente por dos observadores (con 10 y 8 años de experiencia en imagen cardiaca) para cada uno de los 17 segmentos miocárdicos de la clasificación de la American Heart Association, sin que conociesen los resultados de otras pruebas. Posteriormente analizaron las imágenes en consenso para resolver cualquier discrepancia que hubiese.
Para valorar las IPM de la TCDE, se generaron mapas de yodo en el eje corto cardiaco, con grosor de corte de 5 mm, mediante el software de posprocesado Syngo Multimodality Workplace (Syngo Dual Energy, Siemens). Los defectos de perfusión se definieron como áreas contiguas y circunscritas con disminución o ausencia de yodo en relación con el miocardio normal del ventrículo izquierdo15.
Para evaluar la viabilidad miocárdica en la TC, se realizaron reconstrucciones multiplanares en una estación de trabajo Leonardo (Siemens) en los ejes corto y largo y en el plano de cuatro cámaras, con grosor de corte de 10 mm.
La comparación entre TC y RM en cuanto al análisis de perfusión y viabilidad miocárdica se hizo tomando la RM como patrón de referencia.
Dosis de radiaciónLa dosis de radiación efectiva para el estudio de TC se calculó multiplicando el producto dosis-longitud por el factor de conversión para el tórax (k=0,014 mSv / mGy×cm) según la fórmula: dosis efectiva estimada (mSv) = producto dosis-longitud (mGy-cm)×0,014 (factor de conversión en tórax; mSv / mGy×cm)16.
Análisis estadísticoEn el análisis estadístico descriptivo, las variables cuantitativas se expresan como media ± desviación estándar y las variables cualitativas, como frecuencias o porcentajes.
Con la RM cardiaca como estándar de referencia, la precisión diagnóstica de la TC para valorar defectos de perfusión miocárdicos y realce tardío se expresó en términos de sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo.
Las variables cualitativas se evaluaron mediante el test de la χ2.
RESULTADOSPoblación de estudioEl protocolo se completó en 56 de los 68 pacientes remitidos, y se excluyó a 12 pacientes porque no dieron su consentimiento para realizar la RM.
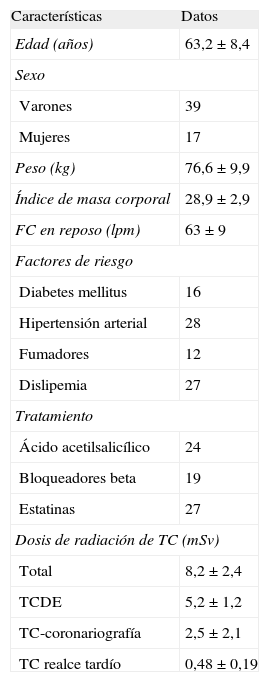
Las características clínicas de los pacientes y las dosis de radiación se resumen en la tabla 1. La indicación de las pruebas fue dolor torácico en 51 pacientes y alteraciones del electrocardiograma en 5. Un paciente se había sometido a cirugía de revascularización coronaria y 6, a implante de stents coronarios. El promedio de tiempo entre la TC y la RM cardiaca fue de 10,8±5,1 días.
Características clínicas de los pacientes
| Características | Datos |
| Edad (años) | 63,2±8,4 |
| Sexo | |
| Varones | 39 |
| Mujeres | 17 |
| Peso (kg) | 76,6±9,9 |
| Índice de masa corporal | 28,9±2,9 |
| FC en reposo (lpm) | 63±9 |
| Factores de riesgo | |
| Diabetes mellitus | 16 |
| Hipertensión arterial | 28 |
| Fumadores | 12 |
| Dislipemia | 27 |
| Tratamiento | |
| Ácido acetilsalicílico | 24 |
| Bloqueadores beta | 19 |
| Estatinas | 27 |
| Dosis de radiación de TC (mSv) | |
| Total | 8,2±2,4 |
| TCDE | 5,2±1,2 |
| TC-coronariografía | 2,5±2,1 |
| TC realce tardío | 0,48±0,19 |
FC: frecuencia cardiaca; TC: tomografía computarizada; TCDE: tomografía computarizada de doble energía.
Tras la administración de adenosina, la frecuencia cardiaca aumentó de 63,7±9,3 lpm en reposo a 75,5±13,8 lpm. No hubo complicaciones mayores que impidiesen terminar el estudio, aunque 9 pacientes presentaron bloqueos auriculoventriculares 2:1; 3, malestar torácico y 4, cefalea. Todas estas complicaciones cedieron tras suspender la adenosina. La dosis efectiva estimada fue de 5,2±1,2 mSv. Se encontraron defectos de perfusión en 17 de 56 pacientes (30,3%), 29 de 168 territorios arteriales (17,2%) y 55 de 952 segmentos miocárdicos estudiados (5,7%).
Tomografía computarizada-coronariografíaA 44 pacientes se les realizó adquisición prospectiva con alto pitch (frecuencia cardiaca, 57±6 lpm) y a 12, adquisición retrospectiva (frecuencia cardiaca, 73±5 lpm). La dosis efectiva estimada fue de 2,5±2,1 mSv. En un análisis por paciente, 27 tenían coronarias normales o estenosis < 50%; 15, estenosis significativa (11 monovaso, 2 bivaso y 2 trivaso) y 14, al menos una de las arterias no valorable por artefacto o calcificación grave. En un análisis por arteria, la descendente anterior fue normal o sin estenosis significativas en 37 casos, con estenosis significativa en 5 e imposible de valorar en 14; la coronaria derecha, en 34, 8 y 14 y la circunfleja, en 37, 8 y 11 respectivamente.
Tomografía computarizada para viabilidad miocárdicaSe observó hiperrealce en 10 de 56 pacientes (17,8%), 14 de 168 territorios arteriales (8,3%) y 28 de 952 segmentos miocárdicos estudiados (2,9%). La dosis efectiva estimada fue de 0,48±0,19 mSv.
Resonancia magnética cardiacaEn los 56 pacientes se obtuvieron imágenes de buena calidad para valorar los defectos de perfusión y el realce tardío. Se encontraron defectos de perfusión en 21 (37,5%) pacientes, 33 (19,6%) territorios arteriales y 68 (7,1%) segmentos miocárdicos. Se observó hiperrealce tardío en 12 (21,4%) pacientes, 18 (10,7%) territorios arteriales y 37 (3,8%) segmentos miocárdicos.
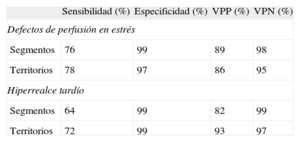
Comparación entre imágenes de perfusión miocárdicas con tomografía computarizada cardiaca y resonancia magnética cardiacaEn la tabla 2 se muestran los valores de sensibilidad, especificidad y valores predictivos negativo y positivo de la TC cardiaca para los defectos de perfusión e hiperrealce tardío.
Resultados del estudio con la tomografía computarizada de doble fuente en la valoración de defectos de perfusión e hiperrealce tardío
| Sensibilidad (%) | Especificidad (%) | VPP (%) | VPN (%) | |
| Defectos de perfusión en estrés | ||||
| Segmentos | 76 | 99 | 89 | 98 |
| Territorios | 78 | 97 | 86 | 95 |
| Hiperrealce tardío | ||||
| Segmentos | 64 | 99 | 82 | 99 |
| Territorios | 72 | 99 | 93 | 97 |
VPN: valor predictivo negativo; VPP: valor predictivo positivo.
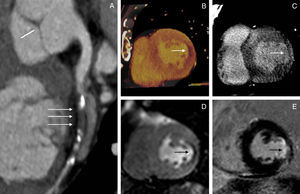
De los 62 segmentos miocárdicos con defectos de perfusión en TCDE, 55 se detectaron en la perfusión de primer paso en la RM (fig. 1); sin embargo, 7 no fueron coincidentes; 15 segmentos con alteración de la perfusión en RM no fueron coincidentes con la perfusión en TCDE.
Caso concordante entre tomografía computarizada y resonancia magnética. Varón de 67 años con estenosis significativa en arteria circunfleja (A), defecto de perfusión en cara lateral del ventrículo izquierdo en tomografía computarizada (B) y resonancia magnética (D). Realce tardío evidenciado con ambas técnicas (C y E).
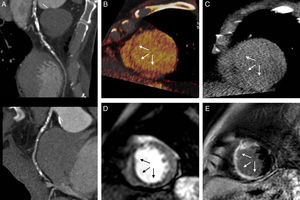
En 28 segmentos se encontró hiperrealce tardío en TC, de los cuales 23 coincidieron con la RM. Hubo 13 hiperrealces en RM que no se vieron en TC (fig. 2).
Falso negativo en la tomografía computarizada de viabilidad con coronarias patológicas. Varón de 72 años con lesiones en descendente anterior (A) y defecto de perfusión en el septo en tomografía computarizada (B) y resonancia magnética (D). Realce tardío en resonancia magnética (E), que no se aprecia en tomografía computarizada (C).
Se encontraron 21 arterias coronarias con estenosis > 50% y 107 sin estenosis. La tabla 3 detalla la relación entre los hallazgos en la TC-coronariografía y la presencia de defecto de perfusión. De los 14 pacientes con al menos una de las arterias coronarias no valorable, se observó defecto de perfusión por TC en el territorio correspondiente en 3 pacientes.
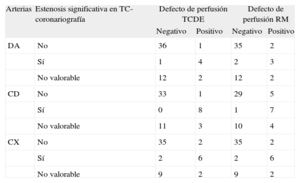
Relación de la estenosis en la tomografía computarizada-coronariografía con los defectos de perfusión tanto en la tomografía computarizada de doble energía como en la resonancia magnética
| Arterias | Estenosis significativa en TC-coronariografía | Defecto de perfusión TCDE | Defecto de perfusión RM | ||
| Negativo | Positivo | Negativo | Positivo | ||
| DA | No | 36 | 1 | 35 | 2 |
| Sí | 1 | 4 | 2 | 3 | |
| No valorable | 12 | 2 | 12 | 2 | |
| CD | No | 33 | 1 | 29 | 5 |
| Sí | 0 | 8 | 1 | 7 | |
| No valorable | 11 | 3 | 10 | 4 | |
| CX | No | 35 | 2 | 35 | 2 |
| Sí | 2 | 6 | 2 | 6 | |
| No valorable | 9 | 2 | 9 | 2 | |
CD: arteria coronaria derecha; CX: arteria circunfleja; DA: arteria descendente anterior; TC: tomografía computarizada; TCDE: tomografía computarizada con doble energía en estrés; RM: resonancia magnética en estrés.
El presente estudio indica que la TCDF es una técnica diagnóstica factible y con aceptables resultados diagnósticos para la valoración de la perfusión miocárdica en comparación con la RM. El estudio con TC posibilita además una imagen de las arterias coronarias que ayuda a la estratificación pronóstica de la aterosclerosis.
La TC-coronariografía es una técnica excelente para la valoración de la enfermedad coronaria; sin embargo, no proporciona información de la perfusión miocárdica, ya que el flujo coronario se mantiene hasta que la estenosis no supera el 80% de la luz17. Por lo tanto, en muchas ocasiones en que se diagnostica enfermedad coronaria, solo se puede valorar la repercusión en la perfusión miocárdica mediante pruebas de estrés.
El desarrollo tecnológico de los equipos de TC ha hecho posible que se pueda realizar estudios de perfusión con buena calidad y dosis de radiación adecuada. Blankstein et al18 han comunicado que los estudios de IPM con TCDF en estrés tienen una sensibilidad del 93% y una especificidad del 74% para detectar estenosis coronarias en comparación con la SPECT. Rocha-Filho et al19 publicaron que la adición de las IPM incrementa la precisión diagnóstica en el estudio de TC-coronariografía, lo que ofrece la oportunidad para la evaluación simultánea de la anatomía y la perfusión en un solo examen.
Recientemente Bettencourt et al20 han demostrado las altas sensibilidad y especificidad de las IPM tanto por TC como por RM para la detección de las estenosis coronarias significativas en un estudio en el que el patrón de referencia fue la fracción del flujo de reserva, y han puesto de manifiesto que un protocolo de TC que integre anatomía y perfusión puede ser tan eficaz como la perfusión-RM para detectar lesiones coronarias significativas.
Otra forma más novedosa de valorar las IPM es la TCDE, mediante la cual se puede generar un mapa de yodo analizando la distribución de este en el miocardio, basándose en las características específicas de absorción de rayos X por el yodo con niveles de alta y baja energía21. Ko et al12,13 publicaron que la TCDE es segura para valorar los defectos de perfusión miocárdicos en comparación con la RM. Además demostraron que los estudios de perfusión con mapa de yodo incrementan la seguridad diagnóstica de la TC-coronariografía en pacientes con enfermedad coronaria conocida.
La TC también puede valorar el realce tardío, ya que el yodo es un contraste extracelular que persiste cuando hay necrosis miocárdica. La TCDF con técnica de alto pitch se ha demostrado de buena precisión en la valoración del realce tardío con baja dosis de radiación, aunque conlleva más «ruido» de la imagen14.
En nuestro trabajo se realizó un novedoso protocolo, con una TCDF de segunda generación, valorando la perfusión miocárdica con energía dual y mapa de yodo, las arterias coronarias y el realce tardío con técnica de alto pitch. A diferencia de otros estudios, se incluyó a sujetos con sospecha clínica de enfermedad coronaria en la consulta del cardiólogo, sin prueba de imagen alguna que documentara con anterioridad la existencia de enfermedad coronaria. De hecho, la prevalencia de enfermedad coronaria en nuestra población es relativamente baja. Los valores de nuestro estudio para valorar la IPM con mapa de yodo en comparación con la RM son parecidos a los de Ko et al12, que hacen una comparación similar pero en sujetos con enfermedad coronaria conocida. Sin embargo, la sensibilidad para detetectar el hiperrealce tardío fue tan solo del 64%, probablemente influido por el bajo kilovoltaje utilizado, que hace que las imágenes presenten mucho «ruido».
También se estudió la anatomía de las arterias coronarias, y se observó una excelente correlación entre la estenosis de la arteria coronaria con los defectos de perfusión tanto en TCDE como en RM. En nuestro estudio, 3 pacientes con coronarias no valorables mostraron alteraciones de la perfusión en la TC, y se les cambió el manejo y se los remitió a realización de coronariografía.
LimitacionesSon varias las limitaciones que tiene nuestro estudio. En primer lugar, se trata de un estudio realizado en un único centro. Por lo tanto, se necesita de estudios prospectivos, aleatorizados y multicéntricos para valorar el uso de este protocolo en el estudio de la cardiopatía isquémica.
La IPM con mapa de yodo es una técnica introducida recientemente y no está documentado cómo se debe realizarla para obtener una imagen óptima (velocidad y cantidad de contraste administrado, tiempo de inicio de la adquisición, características técnicas, etc.). Además, en ocasiones se observan artefactos de endurecimiento del haz que pueden dar lugar a falsos positivos. Se necesita un aprendizaje de la técnica que ayude a protocolizar mejor la adquisición y mejore la interpretación de imágenes.
Otro problema es que la perfusión de mapa de yodo no es dinámica, solo se valora la distribución del yodo en un instante y puede que este no sea el momento óptimo en que haya más diferencia de atenuación entre el miocardio mal perfundido y el normal. La imagen estática, además, carece de datos cuantitativos de perfusión como flujo arterial y volumen sanguíneo.
Solo utilizamos la RM como patrón de referencia, sin estudios invasivos como la coronariografía para valorar las estenosis coronarias y el flujo de reserva coronario.
Por último, la dosis de radiación en nuestro protocolo sigue siendo considerablemente alta (8,2±2,4 mSv), aunque es menor que en los estudios de perfusión con SPECT (12,3±4,3 mSv)22.
Implicaciones para la práctica clínicaA pesar de todas estas limitaciones, en ausencia de contraindicaciones la TCDF es una técnica diagnóstica que ofrece aceptables resultados en la valoración de la isquemia miocárdica. Esto puede ayudar a valorar la repercusión funcional, con la misma prueba, en los casos de estenosis coronaria difícil de cuantificar porque, por ejemplo, hay mucho calcio. Esto permitiría identificar de manera más precisa a pacientes subsidiarios de coronariografía por alteraciones en la IPM.
CONCLUSIONESLa TCDF es una técnica prometedora para valorar los defectos de perfusión y la viabilidad miocárdica que permite valorar conjuntamente la anatomía coronaria con una aceptable dosis de radiación. Se necesitan estudios multicéntricos más amplios que permitan conocer su verdadero valor.
CONFLICTO DE INTERESESNinguno.