El implante de marcapasos endocárdico definitivo en población pediátrica es un reto y supone menos del 1% del total de pacientes que merecen colocación1. La ausencia de dispositivos diseñados para niños ha limitado su aplicación generalizada. Anteriormente, los implantes de marcapasos en menores se realizaban con abordaje epicárdico porque el tamaño de los generadores y los cables intravenosos se consideraba poco apropiado y peligroso. Sin embargo, la colocación de marcapasos endocárdico en edad pediátrica se utiliza cada vez con mayor frecuencia por las ventajas que ofrece, como los umbrales de captura más bajos y la menor posibilidad de fractura de los electrodos2.
Se presenta nuestra experiencia en pacientes con peso < 10 kg a los que se implantó un marcapasos endocárdico definitivo (25 pacientes), desde enero de 2006 a marzo de 2015. Las medianas de edad y peso fueron 17 (intervalo, 6-40) meses y 7 (4,4-10,0) kg respectivamente. El motivo del implante fue el bloqueo auriculoventricular (BAV) completo posquirúrgico en 22 pacientes (88%) (tabla). Salvo en un caso, el BAV era consecuencia del cierre de un defecto interventricular. La mediana de tiempo entre la cirugía y el implante del marcapasos fue 23 (9-40) días. El acceso vascular fue mediante punción de la vena subclavia derecha (n = 15) o izquierda (n = 10). Se utilizaron introductores de calibre 7 Fr para avanzar los electrodos auriculares o ventriculares (52 cm de longitud y 2 mm de diámetro), todos bipolares y de fijación activa. Los cables auriculares en casos de colocación bicameral se dejaron con un asa redundante en la aurícula derecha (aproximadamente de 4-6 cm) (figura). En la tabla se muestran los modelos de generador utilizados, los sitios anatómicos de fijación de los cables y la modalidad de estimulación y los parámetros eléctricos basales en el momento del implante y en el seguimiento. El generador se colocó en una bolsa subpectoral. La colocación del marcapasos se realizó sin incidentes en prácticamente todos los pacientes; 1 presentó taquicardia supraventricular durante la fijación del cable auricular, sin repercusión; 1 niño sufrió la disfunción del cable auricular el segundo día del procedimiento (por desplazamiento del cable) y requirió recambio. Se dio seguimiento a 22 pacientes (88%), con una mediana de 48 (1–102) meses. Dos niños necesitaron recambio del generador por agotamiento de la batería. No hubo evidencia de trombosis venosa en el momento de recambiar el sistema. La exteriorización de los electrodos se presentó en 3 casos (12%), secundaria a infección en el sitio del implante a los 8, 25 y 27 meses de colocado el marcapasos, todos sin antecedente de hematoma en el sitio del implante. Una vez resuelto el proceso infeccioso, 2 niños necesitaron extracción y reimplante por vía quirúrgica (epicárdico) y otro, la recolocación por vía percutánea en posición contralateral. Todos los pacientes, incluidos los que sufrieron exteriorización del marcapasos, se encontraban en buen estado clínico.
Características clínicas y eléctricas del implante de marcapasos endocárdico definitivo en niños pequeños
| Paciente | Cardiopatía congénita | Generador | Sitio de implante | Modalidad | Parámetros eléctricos al implante | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aurícula | Ventrículo | Aurícula | Ventrículo | Frecuencia cardiaca máx/mín (lpm) | ||||||||
| Sensibilidad (mV) | Umbral captura (mV) | Impedancia (Ω) | Sensibilidad (mV) | Umbral de captura (mV) | Impedancia (Ω) | |||||||
| 1 | CIA + CIV | St. JudeMicrony II | ------ | Ápex | VVIR | ------- | ------- | ------- | NA | NA | NA | 185/90 |
| 2 | CoAo + PCA + CIV | Guidant InsigniaI Entra | Pared posterior | Ápex | DDDR | NA | NA | 464 | NA | NA | 512 | 150/80 |
| 3 | Doble discordancia + CIV | Vitatron | Pared posterior | Ápex de VI | DDD | NA | 0,2 | 450 | NA | 0,4 | 598 | 170/90 |
| 4 | Canal AV | St. JudeMicrony II | ----- | TSVD | VVIR | ------- | ------- | ------ | NA | NA | 415 | 185/90 |
| 5 | CIV + PCA | Guidant InsigniaI Entra | Orejuela | TSVD | DDDR | NA | NA | 610 | NA | NA | 530 | 180/80 |
| 6 | CATVP supracardiaca a VCS | Guidant InsigniaI Entra | Pared posterior | Ápex | DDD | 3,5 | 0,4 | 420 | 3,5 | 0,4 | 430 | 180/90 |
| 7 | Dextrocardia, situs inversus, DVSVD | Guidant InsigniaI Entra | Pared posterior | Ápex | DDD | 0,75 | 0,6 | 447 | 8,6 | 0,9 | 464 | 150/90 |
| 8 | Corazón estructuralmente sano | Guidant InsigniaI Entra | Pared posterior | Ápex | DDDR | 1,5 | 530 | 8,0 | 490 | 185/90 | ||
| 9 | TGA + CIV + rodete subpulmonar | Guidant InsigniaI Entra | Pared lateral | Ápex | DDDR | 2,0 | 1,0 | 400 | 10 | 1,25 | 700 | 185/110 |
| 10 | CIV + PCA | Medtronic | Orejuela | TSVD | DDDR | 0,19 | 2,4 | 866 | 15 | 2,1 | 952 | 180/80 |
| 11 | CIV + PCA | Boston ScientificAltrua | Orejuela | TSVD | DDD | 1,0 | 0,75 | 470 | 6,0 | 0,5 | 440 | 185/70 |
| 12 | Corazón estructuralmente sano + parálisis de aurícula derecha | Boston ScientifcAltrua | Pared posterior | TSVD | DDDR | NA | NA | 420 | 8,5 | NA | 480 | 185/90 |
| 13 | CIV + PCA | Boston ScientificAltrua | Orejuela | TSVD | DDDR | 2,0 | 1,6 | 610 | 15 | 1,2 | 530 | 180/70 |
| 14 | CIV + PCA | Boston ScientificAltrua | Pared posterior | TSVD | DDDR | 3,6 | 1,5 | 636 | 20,7 | 0,9 | 870 | 185/100 |
| 15 | Yuxtaposición de orejuelas | Medtronic | Septo interauricular | Ápex | DDD | 1,0 | 0,6 | 764 | 6,8 | 1,1 | 697 | 185/100 |
| 16 | CIV + PCA | Boston ScientificAltrua | Orejuela | TSVD | DDDR | 1,5 | 0,9 | 430 | 2,5 | 0,5 | 480 | 180/80 |
| 17 | Canal AV | Boston ScientificAltrua | Pared lateral | TSVD | DDDR | 1,2 | 0,5 | 780 | 7,0 | 0,8 | 640 | 185/100 |
| 18 | CIA + CIV | Boston ScientificAltrua | Pared posterior | TSVD | DDDR | 1,2 | 0,4 | 560 | 6,0 | 0,7 | 538 | 185/70 |
| 19 | CIV | Boston ScientificAltrua | Techo | Ápex | DDDR | 0,75 | 0,8 | 413 | 2,5 | 0,4 | 445 | 180/80 |
| 20 | CIV + PCA | Boston ScientificAltrua | Pared lateral | Ápex | DDDR | 0,75 | 1,2 | 534 | 2,5 | 1,2 | 568 | 180/80 |
| 21 | CATVP intracardiaca a seno coronario + CIV | Boston ScientificAltrua | Orejuela | TSVD | DDDR | 0,5 | 0,9 | 474 | 2,5 | 0,5 | 540 | 185/90 |
| 22 | DVSVD | Boston ScientificAltrua | Techo | TSVD | DDDR | 0,8 | 1,3 | 568 | 3,0 | 1,4 | 620 | 185/70 |
| 23 | CoAo + CIV | Boston ScientificIngenio MRI | Orejuela | TSVD | DDDR | 1,0 | 1,5 | 610 | 6,5 | 0,7 | 740 | 185/100 |
| 24 | CIV | Boston ScientificIngenio MRI | Orejuela | TSVD | DDDR | 0,75 | 0,6 | 468 | 2,5 | 0,8 | 534 | 185/90 |
| 25 | CIA + DVSVD | Boston ScientificIngenio MRI | Orejuela | TSVD | DDDR | 0,75 | 0,4 | 788 | 2,5 | 0,4 | 753 | 185/110 |
| Paciente | Parámetros eléctricos al seguimiento | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Aurícula | Ventrículo | % estimulación | Intervalo AV | |||||||
| Sensibilidad (mV) | Umbral captura (mV) | Impedancia (Ω) | Sensibilidad (mV) | Umbral de captura (mV) | Impedancia (Ω) | Auricular | Ventricular | AVs | AVp | |
| 1 | ----- | ----- | ----- | NA | NA | NA | SS | SS | SS | SS |
| 2 | NA | NA | NA | NA | NA | NA | SS | SS | SS | SS |
| 3 | 1,75 | 2,5 | 650 | NA | 0,75 | 450 | 29 | 99 | ND | ND |
| 4 | ----- | ----- | ----- | NA | NA | NA | ----- | ND | ----- | ----- |
| 5 | 1,2 | 3,25 | 310 | 8,6 | 5,0 | 380 | 6 | 100 | ND | ND |
| 6 | NA | NA | NA | NA | NA | NA | SS | SS | SS | SS |
| 7 | 2,0 | 0,1 | 470 | NA | 2,5 | 500 | 57 | 100 | ND | ND |
| 8 | 4,2 | 1,75 | 470 | NA | 1,5 | 520 | 0 | 100 | 150 | 80 |
| 9 | NA | NA | NA | NA | NA | NA | 13 | 98 | ND | ND |
| 10 | 4,0 | 1,75 | 460 | 7,7 | 5,1 | 383 | 21 | 100 | 80 | 140 |
| 11 | 2,0 | 0,05 | 370 | NA | 0,05 | 410 | 0 | 100 | ND | ND |
| 12 | 2,5 | 1,16 | 490 | 4,4 | 4,1 | 490 | 100 | 73 | ND | ND |
| 13 | 0,75 | 0,75 | 460 | NA | 2,5 | 420 | 1 | 99 | ND | ND |
| 14 | NA | 2,0 | 410 | NA | 1,75 | 520 | 97 | 100 | ND | 150 |
| 15 | 1,4 | 1,25 | 522 | NA | 1,25 | 470 | 1 | 100 | 120 | 150 |
| 16 | 2,4 | 1,24 | 610 | NA | 1,25 | 480 | 4 | 100 | ND | ND |
| 17 | 2,2 | 1,75 | 420 | NA | 1,5 | 420 | 19 | 100 | ND | ND |
| 18 | 0,5 | 1,5 | 420 | NA | 1,5 | 420 | 14 | 100 | ND | ND |
| 19 | NA | 2,0 | 380 | NA | 1,75 | 410 | 2 | 100 | ND | ND |
| 20 | 1,0 | 1,25 | 530 | NA | 1,75 | 430 | 40 | 100 | ND | ND |
| 21 | 0,32 | 8,75 | 560 | 6,5 | 1,5 | 440 | 14 | 92 | ND | ND |
| 22 | 2,4 | 1,25 | 410 | NA | 1,25 | 460 | 57 | 100 | ND | ND |
| 23 | 1,9 | 1,25 | 400 | NA | 1,5 | 460 | 11 | 100 | ND | ND |
| 24 | 0,9 | 6,25 | NA | 12 | 2,0 | NA | 7 | 2 | ND | ND |
| 25 | NA | NA | NA | NA | NA | NA | 56 | 100 | 80 | 160 |
AV: auriculoventricular; AVp: intervalo AV estimulado; AVs: intervalo AV sensado; CATVP: conexión anómala total de venas pulmonares; CIA: comunicación interauricular; CIV: comunicación interventricular; CoAo: coartación de aorta; DVSVD: doble vía de salida del ventrículo derecho; lpm: latidos por minuto; NA: no aplicable; ND: no disponible; PCA: persistencia de conducto arterioso; SS: sin seguimiento; TGA: transposición de grandes arterias; TSVD: tracto de salida de ventrículo derecho; VI: ventrículo izquierdo.
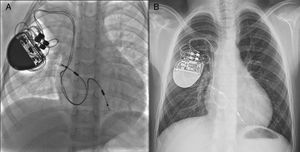
Paciente de 2 años y 9 kg de peso con bloqueo auriculoventricular congénito. Obsérvese la disposición de los electrodos tanto en la aurícula como en el ápex del ventrículo derecho (A). El mismo paciente a la edad de 8 años y con 25 kg (B). Obsérvese el mínimo desplazamiento de los electrodos a pesar de un crecimiento somático significativo.
Se debe tener en cuenta algunas consideraciones cuando se decide colocar un marcapasos endocárdico en niños pequeños. El crecimiento puede causar desplazamiento de los cables, lo que puede afectar a la estimulación del dispositivo, lo cual a su vez obligaría a implantar nuevos cables en un periodo relativamente corto. Para evitarlo, es deseable introducir una mayor longitud del cable en la aurícula. Gheissari et al.3 calcularon que un asa del electrodo auricular derecho de 8cm permite un crecimiento de 6 a 12 años sin necesidad de reintervención; cada año se necesitan aproximadamente 10 mm del cable para compensar el crecimiento del niño. Otros señalan que, al dejar un asa tan redundante, hay riesgo de desplazamiento hacia el tracto de salida del ventrículo derecho que puede generar insuficiencia pulmonar4. En nuestra experiencia, es conveniente dejar un asa de aproximadamente 4-6 cm, y hasta el momento no se ha producido problema alguno, aunque reconocemos que se debe contar con un mayor número de pacientes y un seguimiento más largo. Otro aspecto importante es la delgada capa de tejido subcutáneo de los niños pequeños. El tamaño de la fuente del marcapasos tiende a ejercer tensión contra el tejido y puede ocasionar lesiones a ese nivel. Según esto, hay riesgo de exteriorización e infección del sistema de estimulación, como han señalado estudios similares al nuestro5. Al respecto, el implante subpectoral del generador se ha asociado con menos riesgo de infección6. Se prefiere este abordaje no solo por razones estéticas, sino porque el músculo pectoral provee mayor protección en estos pacientes.
Para concluir, si bien los pacientes merecen vigilancia estrecha toda la vida por el riesgo de exteriorización de los electrodos o trombosis venosa, consideramos que el implante de marcapasos endocárdico en pacientes pediátricos de menos de 10 kg es una opción razonablemente efectiva y segura en centros con experiencia.