La angina estable es un cuadro clínico de gran importancia, dado que es una de las presentaciones iniciales de la cardiopatía isquémica y probablemente su frecuencia sea mayor en la atención primaria y el ámbito de urgencias. Tiene un pronóstico desfavorable y el diagnóstico se basa en los datos clínicos, la probabilidad pretest y la selección de pruebas diagnósticas acordes con esa probabilidad. Entrar en el proceso diagnóstico del dolor torácico sin una orientación previa conlleva un exceso de pruebas no concluyentes y potencialmente peligrosas para el paciente. Con una metodología adecuada, es posible estratificar eficazmente a los pacientes detectando a los que tengan lesiones coronarias significativas en los que se pueda plantear una opción terapéutica basada en los conocimientos actuales.
Palabras clave
La angina es una de las manifestaciones de la cardiopatía isquémica, junto con el síndrome coronario agudo (SCA) y la muerte súbita. La angina se define como un dolor torácico opresivo, o sus variantes clínicas, secundario a isquemia en el miocardio. Esta isquemia se produce porque la demanda de oxígeno del músculo cardiaco supera la oferta que la arteria coronaria correspondiente consigue hacer llegar. La causa más frecuente de angina es la estenosis de una arteria coronaria por ateromatosis. Si la estenosis es fija (placa ateromatosa estable), el umbral de isquemia es siempre similar y aparece con niveles de ejercicio predecibles, lo que constituye el cuadro clínico denominado angina estable. Se denomina angina inestable a todas las variantes de la angina que no siguen una aparición del dolor para un umbral fijo y aparecen en reposo, con un umbral de ejercicio variable o cada vez más reducido, y a la angina de inicio reciente y, por lo tanto, de evolución impredecible.
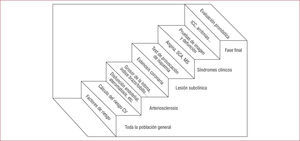
En ocasiones, especialmente en la literatura anglosajona, se habla indistintamente de angina estable y de cardiopatía isquémica crónica estable, pero debe quedar muy claro que no son conceptos intercambiables. Mientras que la angina estable es un cuadro clínico muy bien definido, en el que el paciente describe una clínica específica secundaria a un episodio transitorio de isquemia miocárdica—que puede producirse con coronarias normales—, la cardiopatía isquémica crónica implica que el paciente tenga un diagnóstico establecido e inequívoco de un antecedente de isquemia coronaria, pero que pueda estar activo o totalmente asintomático y que quizá no haya isquemia residual. El concepto de cardiopatía isquémica crónica es más amplio que el de angina estable e incluye a los pacientes con antecedentes de infarto o de revascularización coronaria, independientemente de su estado clínico actual. En el esquema clásico ilustrado en la figura 1, el paciente con angina estable está en el cuarto escalón, el que corresponde a manifestaciones clínicas, mientras que el paciente con cardiopatía isquémica crónica puede estar en el segundo escalón si hay evidencia de enfermedad arteriosclerótica coronaria, en el tercero si se demuestra isquemia miocárdica o en el cuarto si tiene clínica de angina o de SCA; precisamente, el trabajo del cardiólogo será identificar en qué estadio se encuentra, dado que los niveles de riesgo cardiovascular son diferentes.
Esquema de las formas evolutivas de la cardiopatía isquémica. La base, mucho más amplia, contiene toda la población, y en cada escalón hay menos individuos en una fase más avanzada que en el escalón previo. En la cara vertical de cada escalón hay un ejemplo de los elementos que lo forman, mientras que en la faceta horizontal hay un ejemplo de qué herramientas clínicas aplicar en ese escalón concreto. CV: cardiovascular; ICC: insuficiencia cardiaca; MS: muerte súbita; SCA: síndrome coronario agudo.
En las páginas siguientes se describe básicamente el estado actual del diagnóstico de la angina estable y la estratificación del riesgo de estos pacientes. El término cardiopatía isquémica crónica se reserva para los pacientes con antecedentes de enfermedad coronaria (angina, infarto o muerte súbita recuperada de etiología isquémica), independientemente de que el paciente tenga clínica de angina.
Aunque existen causas de angina sin lesiones coronarias subyacentes y en todos los libros hay listas exhaustivas de posibles etiologías, la enfermedad causal más frecuente es la ateromatosis coronaria, y este artículo se dedica exclusivamente a esta etiología.
Diagnóstico de la angina estableAnte un paciente que consulta por un dolor torácico crónico y estable, el médico debe responder a dos preguntas básicas: ¿qué probabilidad tiene este paciente de que se trate de una angina de pecho? y ¿cuál es la mejor forma de confirmar o descartar el diagnóstico?
El diagnóstico de la angina es clínico y se caracteriza por una molestia en la zona retroesternal que puede variar desde cierta pesadez a un dolor intenso, sin que haya una relación directa entre el grado de malestar y el grado de isquemia subyacente. De forma típica, la angina aparece con el ejercicio o en circunstancias que aumentan el trabajo cardiaco, como el estrés emocional, el frío intenso o una comida copiosa, dura unos pocos minutos y cede con el reposo o tras la toma de nitroglicerina. Estos tres criterios (localización retroesternal, su relación con el ejercicio y la desaparición con el reposo o la nitroglicerina), los describieron Diamond et al1 en 1979 y posteriormente se tradujeron a los términos de angina típica si tiene las tres características, angina atípica si tiene dos y dolor torácico no anginoso si sólo tiene una o ninguna. Esta clasificación no es puramente semántica, ya que, en combinación con la edad y el sexo del paciente y de acuerdo con los resultados del estudio CASS y otros posteriores, permite determinar la probabilidad de que haya una enfermedad coronaria subyacente2. Estas cifras, denominadas probabilidad pretest de enfermedad coronaria, se describen en la tabla 1, están disponibles en los portales de las principales sociedades cardiovasculares y se han incorporado a calculadoras electrónicas para ordenadores o dispositivos móviles3.
Probabilidad pretest (%) de enfermedad coronaria significativa en función del tipo de angina, la edad y el sexo.
| Edad | Angina típica | Angina atípica | Dolor no anginoso | |||
| Varones | Mujeres | Varones | Mujeres | Varones | Mujeres | |
| < 40 años | 76 | 26 | 34 | 12 | 4 | 2 |
| 40–49 años | 87 | 55 | 51 | 22 | 13 | 3 |
| 50–59 años | 93 | 73 | 65 | 31 | 20 | 7 |
| > 60 años | 94 | 86 | 72 | 51 | 27 | 14 |
Los pacientes con factores de riesgo coronario conocidos como hipertensión, diabetes mellitus, hipercolesterolemia, tabaquismo o antecedentes familiares de cardiopatía isquémica precoz, tienen mayor riesgo de sufrir enfermedad isquémica subyacente, por lo que la presencia de estos factores en un paciente con dolor torácico hace más probable que este sea de origen coronario; sin embargo, y a diferencia de lo que ocurre con el cálculo de sufrir una muerte coronaria o un infarto de miocardio, estos factores no se han introducido en los algoritmos diagnósticos más utilizados, y hasta la fecha no hay indicadores similares a las tablas de riesgo de Frammingham o el EuroSCORE.
Un factor muy importante en el diagnóstico de la angina de pecho es el ámbito donde se realiza. Normalmente los cardiólogos no son los primeros en ver a los pacientes con dolor anginoso, sino que estos acuden al médico de familia o a los servicios de urgencias, sea directamente o referidos por el médico de atención primaria. Esto ha generado en los últimos años un esfuerzo muy importante para diagnosticar correctamente a estos pacientes y ha impulsado la creación de dispositivos específicos como las unidades de dolor torácico, sean estructurales o funcionales. Estas unidades se desarrollaron sobre todo para diagnosticar episodios de isquemia coronaria con riesgo vital para el paciente (riesgo de sufrir un SCA), acortar el tiempo de estancia en el área de urgencias y, al mismo tiempo, orientar en los procesos diagnósticos y terapéuticos más adecuados. Indirectamente, han desplazado el diagnóstico de la angina hacia una vertiente mucho menos clínica, donde predominan las pruebas complementarias como las determinaciones de las enzimas de necrosis, los electrocardiogramas (ECG) seriados, las pruebas de esfuerzo de provocación de isquemia en sus diferentes variedades e incluso las técnicas de visualización del árbol coronario por métodos no invasivos o por angiografía. Evidentemente, realizar pruebas en pacientes con bajo riesgo de un SCA se asocia con un aumento de falsos positivos, pruebas innecesarias para completar el estudio y un incremento de costes.
Para graduar la gravedad de la angina estable, la clasificación más utilizada es la de la Sociedad Canadiense de Cardiología, que describe cuatro niveles de angina en función de la intensidad de ejercicio que se puede realizar antes de que se presente el dolor anginoso (tabla 2). Esta clasificación se ha impuesto por la facilidad de uso y por la buena asociación con el pronóstico de la angina, que empeora a medida que la clase funcional aumenta4. La gravedad de la angina difiere según el ámbito donde se controle al paciente y suele ser más importante en las áreas cardiológicas. En el registro AVANCE5, que incluyó a 2.024 pacientes con angina estable en consultas externas de cardiología, un 49% declaraba estar sintomático y un 14% tenía una clase funcional III o IV de la citada clasificación.
Clasificación de la intensidad de la angina de pecho según la Sociedad Canadiense de Cardiología.
| Clase I | La actividad diaria no ocasiona angina. Sólo con ejercicio intenso |
| Clase II | Moderada limitación de la actividad diaria. Permite caminar más de 200m o subir más de un piso a velocidad normal |
| Clase III | Marcada limitación de la actividad diaria. La angina aparece al caminar menos de 200m o al subir un piso a velocidad normal |
| Clase IV | Incapacidad para llevar a cabo cualquier actividad física sin molestias. Angina de reposo |
Dado que la angina de pecho es un síntoma, el diagnóstico se completa con alguna prueba que objetive la presencia de isquemia o la falta de perfusión de un territorio determinado. Se debe subrayar en este punto que no es lo mismo realizar el diagnóstico de un dolor torácico como posible angina de pecho que el diagnóstico de arteriosclerosis coronaria. De nuevo nos remitiremos a la figura 1 y, si bien la mayoría de los pacientes con infarto previo tienen una afección ateromatosa vascular en su etiología, la detección de evidencia de arteriosclerosis—sea por historia clínica cardiológica o de otro territorio vascular o por datos de la exploración física, como encontrar unos pulsos periféricos débiles—no nos garantiza que el dolor torácico que estamos investigando sea una angina de pecho.
Se debe realizar un ECG a todos los pacientes con dolor torácico, pero sabiendo que en ausencia de isquemia el 50% de los pacientes con enfermedad coronaria significativa tienen un ECG normal6. El ECG nos informa de un infarto de miocardio previo y, en los casos de un ECG muy alterado por hipertrofia ventricular o por trastorno de conducción interventricular, también nos puede orientar de la baja rentabilidad de una prueba de esfuerzo convencional en el proceso diagnóstico de ese paciente. Un ECG basal característico de isquemia, con ondas T simétricas e invertidas en el territorio de una arteria coronaria, es infrecuente pero al mismo tiempo indicativo de una estenosis epicárdica relevante, capaz de ocasionar isquemia en reposo, lo que obliga al médico a una actitud agresiva en el proceso diagnóstico. La detección de un bloqueo avanzado de la rama izquierda del haz de His se puede asociar a enfermedad coronaria multivaso y en ocasiones a una disfunción ventricular izquierda, por lo que también indica que no hay que entretenerse en el proceso diagnóstico.
En ocasiones, es posible obtener un trazado del ECG durante una de las crisis de angina, especialmente si el paciente está ingresado o en el área de urgencias. La detección de cambios en la repolarización durante la crisis de angina es altamente sensible y específica para el diagnóstico de enfermedad coronaria subyacente, normalmente no se necesitan pruebas adicionales de confirmación y permite pasar a la fase de estratificación del riesgo y evaluación terapéutica.
La prueba de esfuerzo convencional, habitualmente en cinta continua, tiene un papel importante en el diagnóstico de la angina de esfuerzo, especialmente en los pacientes que pueden realizar un esfuerzo reglado y un ECG basal normal. Su especificidad y su sensibilidad no son muy elevadas (entre el 70 y el 80%, dependiendo de la experiencia de los exploradores y de su habilidad para conseguir una prueba máxima limitada por síntomas) y caen estrepitosamente si el ECG de base está alterado por trastornos de la conducción ventricular, depresión del ST por hipertrofia ventricular y también (aunque las causas no son claras) si el paciente ya fue revascularizado antes. De todas formas, la prueba de esfuerzo convencional es una técnica barata y que aporta información adicional sobre la capacidad funcional del paciente, la frecuencia cardiaca a la que aparecen la isquemia o la respuesta tensional, que pueden ser importantes en la estratificación y el pronóstico.
A este respecto, vale la pena destacar la puntuación de la prueba de esfuerzo según la Universidad de Duke (Duke Treadmill Score)7, obtenida según la siguiente fórmula: Puntuación = Tiempo de ejercicio [en min] – (5 × máxima desviación del ST durante el esfuerzo [en mm]) – (4 × angina clínica durante la prueba [0, sin angina; 1, angina; 2, angina que obliga a suspender la prueba]). Una puntuación superior a 4 puntos se correlaciona con un riesgo bajo y una supervivencia a los 5 años del 97%. Una puntuación entre 4 y −10 se considera un riesgo moderado y con una supervivencia a los 5 años del 91%. Obtener una puntuación de −11 o inferior se considera un riesgo alto y se ha descrito una supervivencia a los 5 años de sólo el 72%.
En los casos con ECG basal alterado, podemos recurrir a las técnicas de imagen (ecocardiografía, angiografía isotópica o resonancia magnética) y cuando el paciente es incapaz de realizar un esfuerzo físico, se puede utilizar fármacos para aumentar el trabajo miocárdico y revelar una isquemia subyacente (dobutamina o adenosina). Todas las variantes técnicas no invasivas son posibles, y en general la sensibilidad de estas pruebas está entre el 85 y el 90%, con una especificidad un poco menor (entre el 80 y el 85%). Acostumbran ser técnicas con una curva de aprendizaje importante y con unos costes no despreciables, por lo que deberían ser excluyentes entre sí, y su elección depende mucho del paciente y sobre todo de la disponibilidad y la experiencia de los gabinetes donde se realicen las pruebas. En la tabla 3 se resumen las principales pruebas no invasivas con las sensibilidades y especificidades descritas8–10.
Sensibilidad y especificidad de las pruebas no invasivas utilizadas para el diagnóstico de isquemia.
| Prueba | Sensibilidad, % | Especificidad, % |
| SPECT con ejercicio8 | 86 | 78 |
| SPECT con adenosina8 | 87 | 76 |
| Ecocardiografía en ejercicio9 | 85 | 80 |
| Ecocardiografía con dobutamina9 | 83 | 85 |
| CRM con adenosina10 | 83 | 86 |
| CRM con dobutamina10 | 91 | 83 |
CRM: cardiorresonancia magnética; SPECT: tomografía computarizada por emisión monofotónica.
Un capítulo aparte merece la tomografía computarizada multidetectores (TCMD). Esta técnica, de creciente implantación, aporta dos datos diferentes. Por un lado, el estudio del calcio coronario, mensurable de forma estandarizada mediante el índice de calcificación (ICa) según la puntuación de Agaston, nos indica el grado de calcificación de las coronarias y se ha correlacionado con la presencia de lesiones significativas y eventos cardiacos11. El ICa se ha utilizado como elemento de estratificación pero, como veremos luego, su utilidad en el diagnóstico de angina de pecho está en discusión y no hay una correlación exacta entre el grado de calcificación y la gravedad de las estenosis.
El segundo aporte de la TCMD es la facilidad para visualizar la anatomía de las arterias coronarias en una auténtica coronariografía no invasiva. Aunque la presencia de lesiones coronarias, incluso significativas, no es sinónimo de isquemia y, por lo tanto, no sirve para el diagnóstico de angina, la demostración de un árbol coronario sin lesiones significativas descarta una angina por ateromatosis coronaria y además mejora inmediatamente el pronóstico vital del paciente. Este valor predictivo negativo elevado es una herramienta muy valiosa en la escala diagnóstica y pronóstica, pero dado que la presencia de lesiones coronarias asintomáticas no es infrecuente, puede llevar no ya a diagnósticos inexactos, sino, lo que es peor, a tratamientos innecesarios sobre lesiones coronarias que no se ha demostrado que produzcan isquemia miocárdica. Por ello, la TCMD se debe reservar para pacientes con bajo riesgo pretest de lesiones coronarias y en los que el hallazgo de un árbol coronario normal finaliza completamente el proceso diagnóstico de la angina. Se han descrito muy buenos resultados en la evaluación preoperatoria de la cirugía cardiaca no coronaria en pacientes sin antecedentes de cardiopatía isquémica, en quienes se puede ahorrar más de un 80% de las coronariografías sistemáticas12.
Estratificación del paciente con angina estableComo se discute en otros artículos de esta monografía, el enfoque terapéutico de la angina estable ha cambiado en los últimos años y después de la publicación del estudio COURAGE13, que no demostró superioridad en la evolución entre el tratamiento conservador y el invasivo, el primer paso actualmente es obtener un «tratamiento médico óptimo» (TMO). Por esta razón, el problema de la estratificación del riesgo en los pacientes con angina estable y función ventricular normal ha perdido cierto interés si se consigue que el paciente esté asintomático y con TMO. De todas formas, el concepto de que la angina estable es una entidad benigna, tal y como han señalado algunos trabajos14,15, probablemente no sea extrapolable a todos los pacientes con angina, dado que los enfermos reclutados en esos trabajos provienen especialmente de áreas cardiológicas, con un alto porcentaje de revascularización y tasas de TMO muy altas. En los escasos estudios poblacionales, como el finlandés publicado en 200616, se demostró una incidencia de angina del 2% anual y un riesgo relativo de mortalidad o eventos cardiovasculares mayores que varía entre 2,1 y 5,1 a los 10 años, en función del sexo y la edad de los pacientes. En el estudio Whitehall17, realizado en funcionarios londinenses, la presencia de angina doblaba el riesgo por mortalidad coronaria, y si la angina se asociaba al antecedente de un infarto de miocardio, la mortalidad era 6 veces mayor. En la literatura médica hay demanda de nuevos estudios poblacionales sobre la prevalencia y el pronóstico de la angina estable18.
Por otro lado, los buenos resultados de las técnicas de revascularización en los pacientes con angina inestable y SCA han llevado en algunos ámbitos a indicar demasiado fácilmente una coronariografía a un paciente con dolor torácico indicativo de angina. Patel et al19 publicaron en 2010 el hallazgo de que sólo un 38% de las lesiones coronarias eran significativas, en una serie de más de 400.000 coronariografías indicadas por sospecha de enfermedad coronaria en pacientes sin antecedentes de enfermedad isquémica cardiaca conocida. En la discusión de los hallazgos, así como en la correspondencia posterior, se puso de manifiesto un claro sesgo causado por la facilidad de indicar pruebas con bajas sensibilidad y especificidad en pacientes con bajo riesgo (generalmente un test de esfuerzo), lo que origina un número importante de falsos positivos. Una vez que una prueba diagnóstica etiqueta al paciente de isquemia miocárdica, es muy difícil descartar este diagnóstico sin una coronariografía.
Entre estas dos orientaciones extremas, TMO como objetivo último e independiente de la anatomía coronaria y coronariografía fácil e indiscriminada, parece deseable identificar a los pacientes con elevado riesgo anatómico, es decir, afección del tronco común de la coronaria izquierda > 50% o enfermedad de las tres arterias principales con lesiones > 70%. Con algunas consideraciones adicionales, un modelo correcto de manejo del paciente con dolor torácico compatible con angina es el que describe en sus guías el National Institute for Health and Clinical Excellence (NICE), del Servicio Nacional de Salud del Reino Unido, de acceso libre en internet20.
En ellas, y siguiendo la determinación del riesgo pretest descrito en la tabla 1, se considera que a un paciente con una probabilidad pretest > 90% se le debe diagnosticar de angina, y la prueba que se debe realizar es una coronariografía para determinar la anatomía y evaluar el beneficio de las diferentes opciones terapéuticas. Si, por el contrario, el riesgo pretest es < 10%, se debe orientar como con un dolor no anginoso e investigar otras causas y, desde luego, no realizar pruebas diagnósticas con sensibilidad y especificidad reducidas que llevan a un alto número de falsos positivos.
Si el paciente tiene una probabilidad pretest entre el 61 y el 90%, la coronariografía invasiva es adecuada como primera línea diagnóstica, siempre y cuando el paciente sea candidato y esté dispuesto a la revascularización si se detectan lesiones que así lo indiquen. Si la probabilidad pretest de enfermedad coronaria está entre el 30 y el 60%, se debe practicar una prueba funcional diagnóstica, que puede ir desde la ergometría convencional a pruebas que incluyan imagen y estrés farmacológico, dependiendo de la disponibilidad local, la capacidad de ejercicio y las alteraciones del ECG basal. Un planteamiento correcto de cada caso ha de permitir un diagnóstico completo con una o dos pruebas por paciente como máximo; lo que no se justifica es la práctica de todas las disponibles en nuestro arsenal diagnóstico. Sea cual sea la prueba seleccionada, se ha de poder clasificar al paciente con una probabilidad de lesiones coronarias > 60%, en cuyo caso se indica coronariografía invasiva, o situarlo con una probabilidad < 11%, lo cual desvía el diagnóstico hacia causas de dolor torácico no coronario.
En las guías NICE, para los pacientes con una probabilidad pretest de enfermedad coronaria entre el 11 y el 29% se aconseja la práctica de una TCMD con determinación del ICa. En los pacientes con un ICa = 0, se descarta la enfermedad coronaria subyacente, pero este enfoque ha sido criticado en los últimos años, dado que el ICa no tiene la sensibilidad y, sobre todo, la especificidad tan elevada observadas inicialmente y se ha publicado21 que hasta el 19% de los pacientes sin calcificación coronaria (lo que habría descartado el origen isquémico del dolor torácico según NICE) tienen lesiones obstructivas (> 50%) en las arterias epicárdicas.
En los pacientes con dolor torácico y antecedente de enfermedad coronaria, como infarto de miocardio o revascularización, se aconseja practicar una prueba funcional para detectar isquemia. De nuevo, se escogerá la prueba más adecuada dependiendo de la disponibilidad local, la capacidad de ejercicio y las alteraciones del ECG basal.
La práctica de una ecocardiografía u otras técnicas de imagen para obtener la fracción de eyección del ventrículo izquierdo no está justificada en el paciente con angina estable en ausencia de infarto previo o de bloqueo de la rama izquierda del haz de His, pero tiene una importancia pronóstica esencial si se da cualquiera de estas dos circunstancias22.
Un aspecto adicional y que ha despertado bastante interés es el uso de biomarcadores en el diagnóstico y la estratificación de los pacientes con angina estable. Sería muy importante tener una determinación analítica que permitiera diagnosticar o descartar una enfermedad subyacente en los pacientes con dolor torácico. Los resultados hasta la fecha han sido pobres. Se han probado diferentes biomarcadores, como la gamma glutamil tranferasa, la troponina T, la interleucina 6 y, sobre todo, la proteína C reactiva. De manera general, la elevación de estos biomarcadores se asocia a peor pronóstico en forma de mayor incidencia de eventos cardiovasculares, pero no se ha conseguido demostrar que incrementen el valor predictivo obtenido con los datos clínicos y las pruebas de imagen. En un estudio reciente23, sólo la fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP) ha mostrado capacidad diagnóstica, dado que el hallazgo de cifras normales (por debajo del umbral de 25ng/l) tuvo una capacidad predictiva > 95% de que un estudio de perfusión miocárdica fuera negativo.
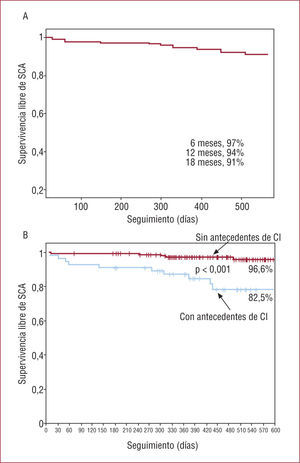
Aunque las unidades de dolor torácico creadas alrededor de los servicios de urgencias de los hospitales han permitido diagnosticar y estratificar rápidamente a los pacientes con dolor torácico, no se han diseñado para el seguimiento de estos enfermos, sino específicamente para obtener altas rápidas o procesos diagnósticos acelerados. En una serie de 204 pacientes consecutivos atendidos por dolor torácico en el servicio de urgencias de nuestro hospital y cuyas pruebas de esfuerzo convencional negativas permitieron el alta precoz, 15 (7,4%) sufrieron un episodio coronario que precisó atención médica durante un seguimiento de 1 año (entre 6 y 18 meses). Esta incidencia de alrededor del 0,5% mensual se mantuvo constante durante el periodo de estudio. La única variable del episodio de dolor torácico que se relacionó con la posibilidad de sufrir un evento isquémico a pesar de una ergometría negativa fue la presencia de enfermedad coronaria conocida previamente (infarto de miocardio, angina o revascularización), lo que indica que se trata de la evolución natural de la enfermedad aterosclerosa subyacente (fig. 2). Ni los datos de la prueba ergométrica realizada ni las analíticas practicadas, que incluían cifras de troponina, tuvieron carácter predictivo.
Se puede concluir que, en el campo del diagnóstico y el tratamiento de la angina estable, se necesitan más estudios de incidencia poblacionales y hay que abordar al paciente con dolor torácico de una forma muy sistematizada para conseguir eficientemente el diagnóstico de angina. La asociación de grados elevados de severidad de la angina y la presencia de factores de riesgo cardiovascular o antecedentes comprobados de cardiopatía isquémica aconseja ser más agresivos en las fases diagnósticas para detectar a los pacientes con más riesgo y optimizar precozmente la terapéutica adecuada.
Conflicto de interesesNinguno.