En los últimos años se han intensificado los esfuerzos de la investigación clínica para determinar los efectos de las diversas estrategias antihipertensivas, más allá de meramente reducir y controlar la presión arterial. De hecho, el bloqueo dual del sistema renina-angiotensina-aldosterona (SRAA) interfiriendo simultáneamente con inhibidores de la enzima de conversión de la angiotensina, antagonistas de los receptores de la angiotensina II o inhibidores directos de la renina (aliskiren) ha centrado tales estrategias en pacientes con elevado riesgo cardiometabólico1.
La posibilidad de que el bloqueo dual del SRAA pueda mejorar los resultados obtenidos con cada uno de los fármacos por separado es una hipótesis atractiva. Sin embargo, ya en el estudio ONTARGET (The ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial) se observó que el bloqueo dual con antagonistas de los receptores de la angiotensina II (telmisartán) y enzima de conversión de la angiotensina (ramipril) no ofrecía ningún beneficio adicional (respecto a la monoterapia) en la reducción de la morbimortalidad cardiovascular de los pacientes con riesgo cardiovascular elevado, y si más efectos adversos2.
Más recientemente, el estudio ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) se interrumpió prematuramente debido a que la terapia dual tampoco mostró beneficio clínico en los pacientes diabéticos que recibían aliskiren además del tratamiento con enzima de conversión de la angiotensina o antagonistas de los receptores de la angiotensina II, mientras que sí se produjeron mayores complicaciones renales, hiperpotasemia, hipotensión e ictus, entre otros3.
En este trabajo se evalúan los riesgos del bloqueo dual del SRAA en pacientes con diabetes mellitus a través de un metaanálisis de ensayos clínicos aleatorizados y controlados. Para ello, se realizó una revisión en PubMed hasta noviembre de 2012. También se consultaron las webs de la Agencia Española de Medicamentos y Productos Sanitarios (www.aemps.gob.es), la European Medicines Agency (www.ema.europa.eu) y la Food and Drug Administration de Estados Unidos (www.fda.gov). Los términos de búsqueda (en inglés) fueron: renin inhibitor, aliskiren, angiotensin receptor block*, losartan, irbesartan, valsartan, olmesartan, candesartan, eprosartan, telmisartan, angiotensin-converting enzyme inhibit*, captopril, enalapril, lisinopril, perindopril, ramipril, fosinopril, trandolapril, temocapril, imidapril combinados con diabetes, diabetic* y randomized controlled trial [publication type]. Se incluyeron estudios en pacientes diabéticos que emplearan la combinación (doble) de bloqueadores del SRAA en el grupo intervención y la compararan con algún bloqueador del SRAA en monoterapia, y que presentaran datos sobre hiperpotasemia, hipotensión, daño renal y/o mortalidad por cualquier causa. Se utilizaron las definiciones propuestas en cada uno de los estudios identificados.
Se calcularon los riesgos relativos combinados junto con el intervalo de confianza del 95%. Para ello se emplearon modelos de efectos fijos y de efectos aleatorios. Se evaluó el grado de heterogeneidad en cada estudio y entre estudios mediante los estadísticos Q de Cochran y el índice I2. Todos los análisis se realizaron con STATA 12® (StataCorp LP; Collage Station, Texas, Estados Unidos).
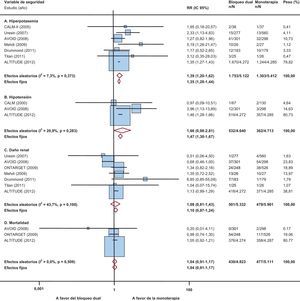
En total, se seleccionaron 9 estudios con 11.543 pacientes diabéticos (tabla) (referencias bibliográficas en el material adicional). Los resultados del metaanálisis permitieron observar que los pacientes diabéticos tratados mediante bloqueo dual del SRAA presentaban mayor riesgo (respecto a la monoterapia) de hiperpotasemia, hipotensión y daño renal, sin producirse una reducción en la mortalidad total. No se observó heterogeneidad significativa. En el caso de la hipotensión y el daño renal, el incremento de riesgo resultó de significación estadística (o próximo a ella) tan sólo en uno de lo modelos (fig.). En general, y salvo el caso del daño renal, la eliminación del estudio más influyente (ALTITUDE) no alteró el sentido de los resultados de los análisis (material adicional).
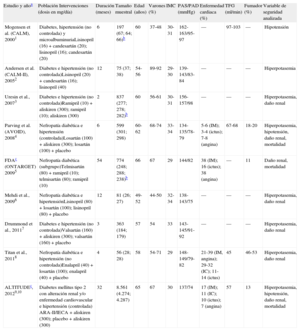
Estudios seleccionados y características basales de los pacientes diabéticos
| Estudio y añoa | Población Intervenciones (dosis en mg/día) | Duración (meses) | Tamaño muestral | Edad (años) | Varones (%) | IMC | PAS/PAD (mmHg) | Enfermedad cardiaca (%) | TFG (ml/min) | Fumador (%) | Variable de seguridad analizada |
| Mogensen et al. (CALM), 20001 | Diabetes, hipertensión (no controlada) y microalbuminuriaLisinopril (16) + candesartán (20); lisinopril (16); candesartán (20) | 6 | 197 (67; 64; 66)b | 60 | 37-48 | 30-31 | 162-163/95-97 | — | 97-103 | — | Hipotensión |
| Andersen et al. (CALM-II), 20052 | Diabetes e hipertensión (no controlada)Lisinopril (20) + candesartán (16); lisinopril (40) | 12 | 75 (37; 38) | 54-56 | 89-92 | 29-30 | 139-143/83-84 | — | — | — | Hiperpotasemia |
| Uresin et al., 20073 | Diabetes e hipertensión (no controlada)Ramipril (10) + aliskiren (300); ramipril (10); aliskiren (300) | 2 | 837 (277; 278; 282)b | 60 | 56-61 | 30-31 | 156-157/98 | — | — | — | Hiperpotasemia, daño renal |
| Parving et al. (AVOID), 20084 | Nefropatía diabética e hipertensión (controlada)Losartán (100) + aliskiren (300); losartán (100) + placebo | 6 | 599 (301; 298) | 60-62 | 68-74 | 33-34 | 134-135/78-79 | 5-6 (IM); 3-4 (ictus); 7-8 (angina) | 67-68 | 18-20 | Hiperpotasemia, hipotensión, daño renal, mortalidad |
| FDAc (ONTARGET) 20095 | Nefropatía diabética (subgrupo)Telmisartán (80) + ramipril (10); telmisartán (80); ramipril (10) | 54 | 774 (248; 288; 238)b | 66 | 67 | 29 | 144/82 | 38 (IM); 16 (ictus); 38 (angina) | — | 11 | Daño renal, mortalidad |
| Mehdi et al., 20096 | Nefropatía diabética e hipertensiónLisinopril (80) + losartán (100); lisinopril (80) + placebo | 12 | 81 (26; 27) | 49-52 | 44-50 | 32-34 | 138-143/75 | — | — | — | Hiperpotasemia, daño renal |
| Drummond et al., 20117 | Diabetes e hipertensión (no controlada)Valsartán (160) + aliskiren (300); valsartán (160) + placebo | 3 | 363 (184; 179) | 57 | 54 | 33 | 143-145/91-92 | — | — | — | Hiperpotasemia, daño renal |
| Titan et al., 20118 | Nefropatía diabética e hipertensión (no controlada)Enalapril (40) + losartán (100); enalapril (40) + placebo | 4 | 56 (28; 28) | 58 | 54-71 | 29 | 148-149/79-82 | 21-39 (IM, angina); 29-32 (IC); 11-14 (ictus) | 45 | 46-53 | Hiperpotasemia, daño renal |
| ALTITUDEc, 20129,10 | Diabetes mellitus tipo 2 con alteración renal y/o enfermedad cardiovascular e hipertensión (controlada) ARA-II/IECA + aliskiren (300); placebo + aliskiren (300) | 32 | 8.561 (4.274; 4.287) | 65 | 67 | 30 | 137/74 | 17 (IM); 11 (IC); 10 (ictus); 7 (angina) | 57 | 13 | Hiperpotasemia, hipotensión, daño renal, mortalidad |
ALTITUDE: Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints; ARA-II: antagonistas de los receptores de la angiotensina II; AVOID: Air Verses Oxygen In myocarDial infarction study; CALM: Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria, and non-insulin dependent diabetes: the candesartan and lisinopril microalbuminuria study; DBP, diastolic blood pressure; FDA: Food and Drug Administration; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; IM: infarto de miocardio; IMC: índice de masa corporal; ONTARGET: ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial; PAD: presión arterial diastólica; PAS: presión arterial sistólica; TFG: tasa de filtración glomerular estimada (media).
Riesgos del bloqueo dual del sistema renina-angiotensina-aldosterona en pacientes diabéticos. ALTITUDE: Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints; AVOID: Air Verses Oxygen In myocarDial infarction study; CALM: Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria, and non-insulin dependent diabetes: the candesartan and lisinopril microalbuminuria study; IC95%: intervalo de confianza del 95%; ONTARGET: ONgoing Telmisartan Alone and in combination with Ramipril Global Endpoint Trial; RR: riesgo relativo.
Las enfermedades cardiovasculares y renales son las principales causas de morbimortalidad en los pacientes diabéticos. Algunas guías clínicas4 incluyen entre sus recomendaciones el uso de los tratamientos antihipertensivos más agresivos (como el bloqueo dual del SRAA) para alcanzar objetivos terapéuticos de presión arterial por debajo de 130/80 mmHg, aun habiendo controversia sobre su beneficio clínico adicional. Pese a que existen diferencias de carácter metodológico y entre las poblaciones estudiadas, los resultados del estudio ALTITUDE han confirmado las previsiones del estudio ONTARGET, en el que ya se había demostrado que la combinación de bloqueadores del SRAA tiene un balance beneficio-riesgo negativo principalmente por la mayor ocurrencia de efectos adversos graves. De hecho, en la información técnica de los productos ya se desaconseja el uso concomitante de enzima de conversión de la angiotensina y antagonistas de los receptores de la angiotensina II en pacientes hipertensos controlados, y en los casos individualmente definidos se debe seguir estrechamente la función renal y las concentraciones sanguíneas de potasio5. Recientemente, y como consecuencia de los resultados del estudio ALTITUDE, se ha contraindicado el bloqueo intenso o dual del SRAA conjuntamente con aliskiren e enzima de conversión de la angiotensina/antagonistas de los receptores de la angiotensina II en pacientes diabéticos o con insuficiencia renal moderada-grave3.
Los resultados obtenidos en este trabajo coinciden los de estudios previos realizados en poblaciones más heterogéneas6. Sin embargo, nuestros análisis presentan limitaciones por la variable calidad de la información empleada, el reducido número de estudios identificados en población diabética —en algunos casos, con un tamaño muestral escaso—, lo cual impidió diferenciar entre tratamientos más allá de la combinación en dos amplios grupos (bloqueo dual de SRAA frente a monoterapia).