En cardiología, es esencial disponer de tecnología adecuada, actualizada y en buenas condiciones de funcionamiento. En España, el marco económico ha impactado fuertemente en los programas de renovación de tecnología y la obsolescencia es un problema creciente. El actual informe trata de dar respuesta al momento y las condiciones que deben concurrir para plantear la actualización, el reemplazo o la adopción de nuevas tecnologías en el ámbito de la cardiología.
Palabras clave
Pocas especialidades como la cardiología emplean tanta tecnología para el diagnóstico y el tratamiento de sus pacientes. La disponibilidad de la tecnología adecuada y su correcta manipulación y funcionamiento son esenciales para la práctica de la cardiología moderna. El actual marco económico ha impactado fuertemente en los programas de renovación de tecnología y la obsolescencia es un problema creciente en el ámbito sanitario europeo, como se refleja en los últimos informes disponibles al respecto1,2.
El actual informe del Comité Ejecutivo de la Sociedad Española de Cardiología trata de dar respuesta al momento y las condiciones que deben concurrir para plantear la actualización, el reemplazo o la adopción de nuevas tecnologías en el ámbito de la cardiología. Precisamente para mantener la calidad asistencial, buscar la eficiencia, no comprometer la seguridad de las actuaciones médicas y facilitar la innovación en un marco de sostenibilidad del sistema sanitario, apoyándonos en criterios de evidencia científica que proporcionen elementos objetivos para la toma de tales decisiones.
FUNDAMENTOSLa Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) recoge en su circular 3/2012 las recomendaciones aplicables a la asistencia técnica de productos sanitarios en los centros sanitarios3 basadas en la legislación europea (Directivas 90/385/CEE4, 93/42/CEE5 y 98/79/CE6). Establece que «los productos sanitarios no deben comprometer la salud ni la seguridad de los pacientes, usuarios o terceras personas cuando se encuentren correctamente instalados y mantenidos, y se utilicen según su finalidad prevista» y que «corresponde a las autoridades sanitarias de los Estados miembros adoptar las medidas necesarias y realizar el oportuno seguimiento para que estas garantías sean satisfechas de forma efectiva por los productos que son comercializados, puestos en servicio, instalados, mantenidos y utilizados en sus territorios». En cuanto al mantenimiento de los equipos, dictamina que «los productos deberán estar correctamente instalados y ser mantenidos adecuadamente de forma que se garantice que, durante su período de utilización, conservan la seguridad y prestaciones previstas por su fabricante».
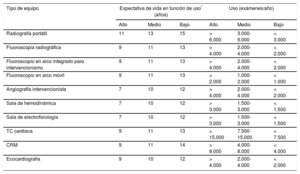
Al respecto, la Canadian Association of Radiologists emitió unas recomendaciones sobre la vida útil de los equipos de imagen basada en una revisión exhaustiva de la literatura disponible7. Así, de manera genérica no se recomienda un uso clínico superior a los 15 años de ninguna tecnología. Se realiza además una estimación de la durabilidad de los equipos en función de su grado de utilización, que se divide en alto (24 h 5 días/semana o 750 turnos de 8 h/año), medio (16 h 5 días/semana o 500 turnos de 8 h/año) y bajo (8 h 5 días/semana o 250 turnos de 8 h/año). Por último, se puntualiza que los equipos de ultrasonidos pueden experimentar una obsolescencia acelerada, dado que en ellos una óptima actualización tecnológica es esencial para mantener un alto rendimiento diagnóstico. De la misma manera, el comité de expertos de la SEC ha establecido unas recomendaciones de longevidad de equipos empleados en procedimientos diagnósticos cardiológicos en función de su utilización (tabla 1).
Longevidad esperada de los equipos de radiodiagnóstico en función de su uso
| Tipo de equipo | Expectativa de vida en función de uso* (años) | Uso (exámenes/año) | ||||
|---|---|---|---|---|---|---|
| Alto | Medio | Bajo | Alto | Medio | Bajo | |
| Radiografía portátil | 11 | 13 | 15 | > 6.000 | 3.000-6.000 | < 3.000 |
| Fluoroscopia radiográfica | 9 | 11 | 13 | > 4.000 | 2.000-4.000 | < 2.000 |
| Fluoroscopio en arco integrado para intervencionismo | 9 | 11 | 13 | > 4.000 | 2.000-4.000 | < 2.000 |
| Fluoroscopio en arco móvil | 9 | 11 | 13 | > 2.000 | 1.000-2.000 | < 1.000 |
| Angiografía intervencionista | 7 | 10 | 12 | > 4.000 | 2.000-4.000 | < 2.000 |
| Sala de hemodinámica | 7 | 10 | 12 | > 3.000 | 1.500-3.000 | < 1.500 |
| Sala de electrofisiología | 7 | 10 | 12 | > 3.000 | 1.500-3.000 | < 1.500 |
| TC cardiaca | 9 | 11 | 13 | > 15.000 | 7.500-15.000 | < 7.500 |
| CRM | 9 | 11 | 14 | > 8.000 | 4.000-8.000 | < 4.000 |
| Ecocardiografía | 9 | 10 | 12 | > 4.000 | 2.000-4.000 | < 2.000 |
CRM: cardiorresonancia magnética; TC: tomografía computarizada.
Por otro lado, el European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry (COCIR), en representación de la industria de tecnología médica en Europa, recomienda para el óptimo funcionamiento del equipamiento médico la adhesión a sus «reglas de oro» (Golden Rules)1, que aconsejan lo siguiente:
- •
Al menos el 60% del equipo instalado debe de tener menos de 5 años: estos equipos reflejan adecuadamente el estado actual de la tecnología.
- •
No más del 30% del equipo instalado debe tener una antigüedad de entre 6 y 10 años: aunque estos equipos son todavía adecuados para su propósito, se debe considerar su futura renovación.
- •
No más del 10% del equipo instalado debe tener más de 10 años: esta tecnología médica está desfasada y es complicado mantenerlo y repararlo.
Además, da unas recomendaciones generales:
- •
Reemplazar equipo obsoleto que no se pueda actualizar.
- •
Utilizar nuevos modelos de financiación con el apoyo de la European Fund for Strategic Investments para convertir la inversión en innovación tecnológica en salud en un aspecto estratégico para incrementar la eficiencia y la accesibilidad de los sistemas sanitarios y mejorar los resultados clínicos.
- •
Adoptar una posición centrada en el paciente para reducir y optimizar la dosis de radiación administrada.
La Sociedad Española de Cardiología considera muy razonables estas recomendaciones y asume que su adopción garantiza el correcto estado de las instalaciones, su uso adecuado, la calidad asistencial, la adecuación al tratamiento y la seguridad de los pacientes.
IMAGEN CARDIACAEcocardiografíaRelevancia y situación tecnológica actual en EspañaAl tratarse de una técnica de imagen de fácil acceso, inocua y dependiente del explorador, las innovaciones tanto en el hardware como en el software adquieren mayor relevancia y hacen que las recomendaciones de renovación se reduzcan a los 5-7 años. Esto resulta de vital importancia en el caso de la ecocardiografía, que ha visto que la generalización de su acceso en los últimos años la ha convertido en una prueba imprescindible para el tratamiento del paciente cardiológico, y su indicación ha aumentando de manera exponencial.
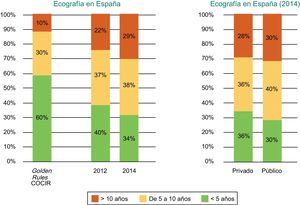
España está lejos de cumplir los estándares de las Golden Rules en lo que respecta a renovación de equipos, y se observa que 1 de cada 3 ecógrafos se encuentra obsoleto, con una antigüedad de más de 10 años (figura 1)2.
Antigüedad de los equipos de ecocardiografía instalados en España según el año (2012 frente a 2014) y según centros públicos o privados. COCIR: European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry. Reproducido con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
Es también preocupante el escaso mantenimiento de los equipos de ecografía. Más de 2 tercios no están sometidos a procedimientos de mantenimiento preventivo que garanticen su estado funcional, su calibración y, por lo tanto, la calidad y la precisión de la imagen2,8.
Recomendaciones de recursos tecnológicosLa American Society of Echocardiography emitió en 2011 unas recomendaciones de calidad que los laboratorios de ecocardiografía deben seguir9. En primer lugar, se indica que los laboratorios deben estar acreditados por la Intersocietal Commission for the Accreditation of Echocardiography Laboratories. Los equipos de ecocardiografía deben ser capaces de realizar imágenes en modos M, bidimensional y Doppler color y espectral (tanto de flujo como tisular). Debe ser posible añadir al estudio los datos de filiación del paciente y las máquinas deben ser capaces de registrar tanto el electrocardiograma (ECG) como las fases respiratorias. Para los estudios transtorácicos, se debe disponer de transductores de alta y baja frecuencia, así como transductores Doppler ciegos, aunque estos se utilizan muy escasamente en la práctica clínica. En el caso de los estudios pediátricos, se debería disponer de transductores dedicados. La ecocardiografía transesofágica se debe realizar con sondas multiplanares10. En los últimos años se ha producido un importante desarrollo tecnológico de la ecocardiografía tridimensional. Esta herramienta se ha demostrado útil en estudios transtorácicos para el cálculo del volumen y la función ventriculares y, especialmente, en estudios transesofágicos, pues permite una detallada visualización de la anatomía valvular y aporta información relevante para la guía de procedimientos de intervencionismo estructural11. Para su realización se necesita disponer de transductores matriciales transtorácicos y transesofágicos adecuados. Si bien esta técnica no es imprescindible en la práctica clínica habitual, es recomendable en centros que realicen intervencionismo estructural transcatéter12. Finalmente, los equipos deben disponer de imagen armónica y otros instrumentos de ajuste que permitan la optimización de la imagen tanto basal como tras la administración de ecopotenciadores. En caso de que se realicen estudios de estrés, la máquina debe permitir también comparar las imágenes adquiridas en las diferentes fases.
Las imágenes diagnósticas deben almacenarse en formato DICOM (Digital Imaging and Communications in Medicine) durante el plazo establecido para su posterior revisión.
Se debe realizar una evaluación periódica de la precisión de los equipos de ecocardiografía y seguir las recomendaciones del fabricante en lo que respecta a mantenimiento preventivo. Del mismo modo, se debe guardar un registro documental de estas pruebas.
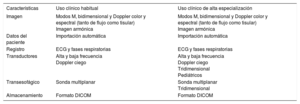
Por lo tanto, se contribuiría a asegurar la calidad asistencial si se efectuase la correspondiente valoración de sus potencialidades de cada equipo, según el tipo de uso que se vaya a hacer (tabla 2).
Requisitos de un equipo de ecocardiografía en función de su uso
| Características | Uso clínico habitual | Uso clínico de alta especialización |
|---|---|---|
| Imagen | Modos M, bidimensional y Doppler color y espectral (tanto de flujo como tisular) Imagen armónica | Modos M, bidimensional y Doppler color y espectral (tanto de flujo como tisular) Imagen armónica |
| Datos del paciente | Importación automática | Importación automática |
| Registro | ECG y fases respiratorias | ECG y fases respiratorias |
| Transductores | Alta y baja frecuencia Doppler ciego | Alta y baja frecuencia Doppler ciego Tridimensional Pediátricos |
| Transesofágico | Sonda multiplanar | Sonda multiplanar Tridimensional |
| Almacenamiento | Formato DICOM | Formato DICOM |
DICOM: Digital Imaging and Communications in Medicine; ECG: electrocardiograma.
La tomografía computarizada (TC), como técnica de imagen que emplea radiación ionizante, está sujeta a un continuo desarrollo tecnológico dirigido a mejorar la calidad de imagen y reducir la exposición del paciente. En los últimos 30 años se ha reducido significativamente el tiempo de escaneado mediante el aumento de la velocidad de rotación del gantry y del número de detectores, así como con los nuevos protocolos de adquisición.
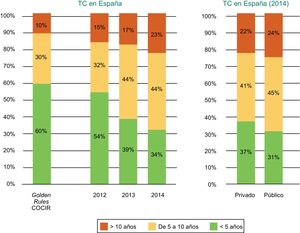
Situación tecnológica actual en EspañaLas medidas de contención del gasto sanitario, fruto de la situación económica en España, han resultado en una progresiva obsolescencia de los equipos de TC en los últimos años, que ha afectado a los centros de titularidad tanto pública como privada, según los datos de la Federación Española de Empresas de Tecnología Sanitaria (Fenin) (figura 2)2.
Antigüedad de los equipos de TC instalados en España según el año (2012-2014) y según centros públicos o privados. COCIR: European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry; TC: tomografía computarizada. Reproducido con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
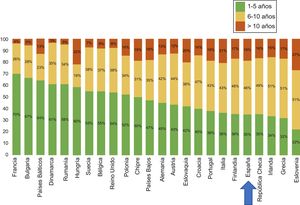
En el último informe de COCIR de 20161, se pone de manifiesto un continuo incremento de la media de edad de los escáneres instalados en Europa occidental, con un aumento en el porcentaje de equipos de más de 5 años del 40% en 2008 al 53% en 2015. Este dato es especialmente preocupante en España, que persiste entre las últimas posiciones en lo que respecta a adhesión a las Golden Rules (figura 3). Como consecuencia de ello, nuestro país presenta una mayoría de equipos que no pueden considerarse de «baja dosis», con el perjuicio que eso implica para la seguridad del paciente.
Grado de cumplimiento por países de las reglas de oro del European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry (COCIR). Adaptado con permiso de European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry1.
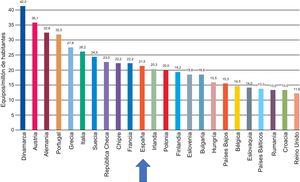
En lo que respecta al número de equipos, a pesar de que la densidad en Europa también se ha visto reducida, España se encuentra en una posición intermedia, con una media de 21,5 equipos por millón de habitantes. De este modo, se supera, aunque ligeramente, la recomendación mínima de 20 equipos por millón de habitantes (figura 4).
Densidad de equipos de tomografía computarizada por países. Adaptado con permiso de European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry1.
Recientemente la Society of Cardiovascular Computed Tomography ha realizado una actualización de Guidelines for performance and acquisition of coronary computed tomographic angiography13, previamente publicadas en 2009, que recoge los últimos avances tecnológicos de esta herramienta diagnóstica.
En esta actualización de la guía, se recomienda que las instalaciones donde se realicen las pruebas cumplan con los estándares de acreditación publicados por la ICACTL (Intersocietal Commision for the Accreditation of Computed Tomography Laboratories) o el ACR (American College of Radiology). En lo referente a los equipos de TC, los escáneres deben tener una rápida rotación del gantry (≤ 350 ms) para su uso en estudios cardiacos. Del mismo modo, se recomienda que los equipos tengan al menos 64 detectores (colimaciones de 32 × 2 o 64 × 1), con una anchura de los elementos de los detectores ≤ 0,625mm. En cuanto a los inyectores, aunque se considera suficiente la utilización de bombas de inyección monocabezal, es deseable que sean de 2 cabezales, de modo que permitan la realización de inyecciones bifásicas o trifásicas a altas velocidades.
En lo referente a la protección radiológica, se debe seguir de manera estricta el principio «tan bajo como razonablemente realizable» (ALARA, por sus siglas en inglés), que obliga a reducir la dosis de radiación al mínimo siempre que el rendimiento diagnóstico de las imágenes obtenidas no se vea perjudicado. En este sentido, algunos de los factores que determinan la dosis recibida por el paciente son fácilmente modificables en todos los equipos de TC (voltaje y corriente del tubo, área de escaneo, espesor de corte, etc.). Sin embargo, otros muchos factores, entre los que se encuentran el tipo de fuente (simple frente a dual), el tiempo de adquisición, la velocidad de rotación del gantry, el tipo de adquisición (prospectiva, retrospectiva, helicoidal de alto pitch), la modulación de dosis y los métodos de reconstrucción (filtered back projection frente a reconstrucción iterativa), están únicamente disponibles en los equipos de nueva generación. El informe de COCIR de 20161 hace especial énfasis en la utilización de las técnicas de modulación de dosis y los algoritmos de reconstrucción iterativa, que permiten una reducción de la radiación absorbida de hasta el 82%.
En este sentido, un cuarto de los equipos de TC instalados en Europa resultan demasiado antiguos para actualizarlos con estas tecnologías, y España se encuentra entre los países europeos con mayor proporción de estos equipos. Otro aspecto fundamental en el control radiológico es la realización de los preceptivos protocolos de mantenimiento. A pesar de la supervisión por un radiofísico acreditado, el informe de Fenin8 estima que hasta un 31% de los equipos no reciben un mantenimiento preventivo que permita certificar su estado de funcionalidad. Por último, se debe almacenar la información sobre la exposición a radiación de cada paciente en algún formato que después permita revisarlo y evaluarlo.
En lo que respecta al almacenamiento de las imágenes, debe ser en formato DICOM y se debe disponer de un sistema de archivo radiológico PACS (Picture Archiving and Communication System) o similar que permita el almacenamiento y la recuperación de todas las imágenes diagnósticas.
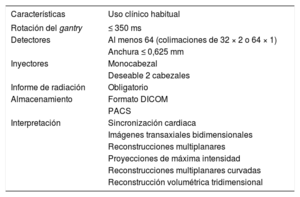
Finalmente, para el análisis y la interpretación de la TC cardiaca, deben utilizarse plataformas de software específicas que permitan evaluar las imágenes tridimensionales con sincronización cardiaca obtenidas en todos los formatos de reconstrucción convencionales: imágenes transaxiales bidimensionales, reconstrucciones multiplanares, proyecciones de máxima intensidad, reconstrucciones multiplanares curvadas y reconstrucción volumétrica tridimensional14.
Por lo tanto, se contribuiría a asegurar la calidad asistencial si se efectuase la correspondiente valoración de potencialidades y elementos de imprescindible dotación de cada equipo (tabla 3).
Requisitos de un equipo de tomografía computarizada cardiaca
| Características | Uso clínico habitual |
|---|---|
| Rotación del gantry | ≤ 350 ms |
| Detectores | Al menos 64 (colimaciones de 32 × 2 o 64 × 1) |
| Anchura ≤ 0,625 mm | |
| Inyectores | Monocabezal |
| Deseable 2 cabezales | |
| Informe de radiación | Obligatorio |
| Almacenamiento | Formato DICOM |
| PACS | |
| Interpretación | Sincronización cardiaca |
| Imágenes transaxiales bidimensionales | |
| Reconstrucciones multiplanares | |
| Proyecciones de máxima intensidad | |
| Reconstrucciones multiplanares curvadas | |
| Reconstrucción volumétrica tridimensional |
DICOM: Digital Imaging and Communications in Medicine; PACS: Picture Archiving and Communication System.
La cardiorresonancia magnética (CRM) es una técnica de imagen no invasiva que no emplea radiación ionizante y permite una evaluación detallada de la anatomía y la función cardiaca sin limitaciones de ventana acústica y una caracterización tisular. Por estos motivos, se ha establecido desde hace años como una herramienta diagnóstica de gran utilidad en la práctica clínica habitual15.
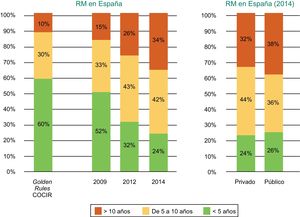
Situación tecnológica actual en EspañaEl estudio COCIR 20161 recoge que, aunque el perfil de edad de los equipos de resonancia magnética no ha empeorado con respecto a la evaluación previa, sigue sin cumplir las recomendaciones de las Golden Rules. Al respecto, como en el caso de la TC, España se sitúa en las últimas posiciones, pues tiene un gran porcentaje de equipos de más de 5 años de antigüedad, e incluso ha empeorado discretamente con respecto a registros previos (figura 5 y figura 6).
Antigüedad de los equipos de resonancia nuclear magnética instalados en España según el año (2009, 2012 y 2014) y según centros públicos o privados. COCIR: European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry; RM: resonancia magnética. Reproducido con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
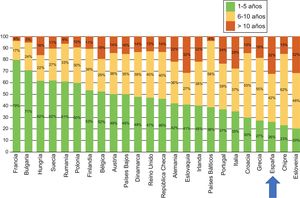
Grado de cumplimiento de las reglas de oro del European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry (COCIR) en resonancia nuclear magnética. Adaptado con permiso de European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry1.
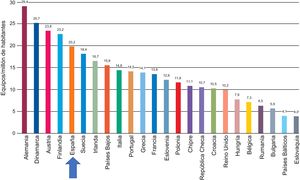
En lo que respecta a la densidad de equipos de resonancia magnética, España se encuentra en buena posición respecto a los demás países europeos y cumple con la regla de más de 20 equipos por millón de habitantes (figura 7).
Densidad de equipos de resonancia nuclear magnética por países. Adaptado con permiso de European Coordination Committee of the Radiological Electromedical and Healthcare IT Industry1.
El aspecto positivo de esta técnica de imagen es que permite realizar actualizaciones relevantes conservando las partes más importantes del equipo (imán y sistema de aislamiento por jaula de Faraday) únicamente acometiendo modificaciones en otros elementos de hardware y en el software. Esto permite acondicionar máquinas no excesivamente antiguas a los estándares diagnósticos actuales. Sin embargo, se constata que el fabricante o un representante autorizado se encargan del mantenimiento de estos equipos solo en el 83% de los casos2 y que el mantenimiento preventivo se limita al 77% de las resonancias8. Esto puede hacer que un porcentaje significativo de los equipos no se beneficien de las actualizaciones disponibles.
Recomendaciones de recursos tecnológicosEn el caso de la CRM, se requiere un equipo de resonancia magnética con un campo electromagnético de al menos 1,5 T16. Los equipos de 3 T presentan una mejor relación señal-ruido que permite una mejor evaluación de las secuencias de perfusión de primer paso, así como de las secuencias de tagging y las técnicas de flujo de 4 dimensiones, pero tienen más susceptibilidad a artefactos, por lo que pueden presentar dificultades en la adquisición de secuencias SSFP. Por estos motivos, aunque ambos campos son admisibles para realizar estudios de CRM, los equipos de 1,5 T continúan siendo el estándar. Otros elementos de hardware necesarios son una antena de radiofrecuencia multielemento de tórax y un sistema de monitorización por ECG compatible con resonancia magnética. De igual manera que en la TC, se precisa una inyectora que sea idealmente de doble cabezal y permita una inyección a alta velocidad. El aspecto más importante para la realización de un estudio de CRM es que el equipo disponga del paquete de software necesario. Debe constar al menos de las secuencias necesarias para realizar estudios clínicos: cine (SSFP, ecocardiografía de gradiente), caracterización tisular (secuencias potenciadas en T1 y T2, secuencia T2*), evaluación de flujo (secuencias de contraste de fase), perfusión miocárdica (secuencias de saturación-recuperación) y realce tardío de gadolinio (secuencia inversión-recuperación potenciada en T1). Además, para la realización de estudios de aorta y de coronarias, se precisan secuencias de angiorresonancia magnética tridimensional con o sin contraste, que en el segundo caso precisan de navegador. Por lo tanto, el equipo de resonancia magnética que se destine a estudios cardiacos debe disponer de todas estas secuencias o tener los requisitos físicos que permitan su actualización a ellas. En los últimos tiempos se está produciendo un importante desarrollo de nuevas técnicas de evaluación del espacio intersticial miocárdico mediante el mapeo en T1 y T217. Estas nuevas herramientas requieren secuencias, protocolos y software de análisis específicos18, con unos requisitos tecnológicos no disponibles en los equipos de resonancia más antiguos. Sin embargo, actualmente estos protocolos no son parte integral de los estudios clínicos habituales. Por lo tanto, aunque su desarrollo es deseable, su disponibilidad aún no es obligatoria para la práctica clínica habitual.
Del mismo modo que con las demás técnicas de imagen cardiaca, se recomienda que los datos obtenidos se almacenen en formato DICOM para su análisis y posteriores revisiones.
Para el análisis de las imágenes de CRM, se debe utilizar software y hardware que respeten unos requisitos mínimos según la Society for Cardiovascular Magnetic Resonance19. Se requiere una estación de trabajo y una pantalla con adecuadas especificaciones y suficiente resolución. El software de análisis debe permitir la visualización simultánea de todos los ejes cortos y el trazado de los bordes endocárdico y epicárdico, así como la selección del segmento más basal para el análisis de volúmenes y función ventricular. También debe permitir las referencias cruzadas para confirmar la posición de corte. Debe tener la posibilidad de comparar el mismo corte en diferentes secuencias, cortes en eje largo y corto, y diferentes estudios del mismo paciente simultáneamente. Debe tener además la posibilidad de realizar análisis semicuantitativos de intensidad de señal. En caso de que se realicen estudios vasculares, debe permitir también la sustracción previa y posterior al contraste y reconstrucciones multiplanares, de máxima intensidad y de reconstrucción volumétrica tridimensional.
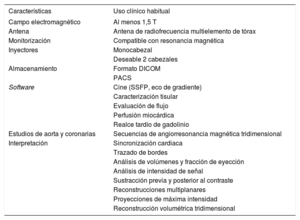
Por lo tanto, se contribuiría a asegurar la calidad asistencial si se efectuase la correspondiente valoración de las potencialidades y los elementos de imprescindible dotación de cada equipo (tabla 4).
Requisitos de un equipo de resonancia magnética para diagnóstico cardiológico
| Características | Uso clínico habitual |
|---|---|
| Campo electromagnético | Al menos 1,5 T |
| Antena | Antena de radiofrecuencia multielemento de tórax |
| Monitorización | Compatible con resonancia magnética |
| Inyectores | Monocabezal |
| Deseable 2 cabezales | |
| Almacenamiento | Formato DICOM |
| PACS | |
| Software | Cine (SSFP, eco de gradiente) |
| Caracterización tisular | |
| Evaluación de flujo | |
| Perfusión miocárdica | |
| Realce tardío de gadolinio | |
| Estudios de aorta y coronarias | Secuencias de angiorresonancia magnética tridimensional |
| Interpretación | Sincronización cardiaca |
| Trazado de bordes | |
| Análisis de volúmenes y fracción de eyección | |
| Análisis de intensidad de señal | |
| Sustracción previa y posterior al contraste | |
| Reconstrucciones multiplanares | |
| Proyecciones de máxima intensidad | |
| Reconstrucción volumétrica tridimensional |
DICOM: Digital Imaging and Communications in Medicine; PACS: Picture Archiving and Communication System; SSFP: Steady-state Free Precession.
La generación de imágenes en las salas de hemodinámica emplea básicamente equipos de rayos X. Esta tecnología genera radiación ionizante, está sujeta a una fuerte regulación relacionada con la seguridad y deberá adecuarse a la normativa de seguridad europea, la Directiva 2013/59/EURATOM20, que será transpuesta y aplicable en abril de 2018.
Equipamiento para el tratamiento percutáneo de lesiones coronariasEl tratamiento percutáneo de lesiones coronarias representa actualmente la actividad principal de los laboratorios de hemodinámica. Para abordar esta afección, es importante disponer de equipos radiológicos que generen una imagen de calidad suficiente para llevar a cabo una correcta intervención.
Además de equipos que proporcionen una calidad de imagen óptima, se recomienda disponer de técnicas de diagnóstico intracoronario adyuvantes:
- •
Reserva fraccional de flujo (FFR): actualmente es la técnica de elección para analizar la gravedad funcional de lesiones coronarias angiográficamente intermedias, pues evita revascularizaciones innecesarias en lesiones que no son significativas desde un punto de vista fisiológico. Las guías de práctica clínica recomiendan la utilización de esta técnica para identificar lesiones hemodinámicamente relevantes en pacientes estables (indicación de clase I, nivel de evidencia A)21. Por lo tanto, esta técnica debería estar disponible en todos los laboratorios de hemodinámica.
- •
Ecografía intravascular (IVUS) y tomografía de coherencia óptica: ambas técnicas de imagen permiten valorar con detalle la morfología de las lesiones coronarias, así como optimizar y analizar el resultado tras el implante del stent. La tomografía de coherencia óptica tiene mayor resolución espacial que la IVUS y permite una detección más exacta de estructuras intraluminales. Asimismo es superior a la IVUS para valorar la mala aposición del stent, el prolapso de trombo o placa y las disecciones y estudiar los mecanismos de fallo del stent. Según las guías de revascularización miocárdica21, ambas técnicas son útiles para estudiar los mecanismos de fallo del stent (IIa B) y optimizar el implante del stent (IIa B para la IVUS y IIb C para la tomografía de coherencia óptica). Además, la IVUS se recomienda para estudiar la gravedad de las lesiones del tronco de la coronaria izquierda y optimizar el resultado (IIa B). Es recomendable disponer de alguna de ellas para el abordaje de lesiones complejas.
En el tratamiento percutáneo de la enfermedad estructural valvular y no valvular, la imagen radiológica tiene un papel menos destacado que en el tratamiento de la enfermedad coronaria. La mayoría de estos procedimientos se guían fundamentalmente mediante ecografía transesofágica, y la visualización radiológica queda en un segundo plano. Por ello, para realizar la mayoría de estos procedimientos es imprescindible un ecocardiograma transesofágico bidimensional. En algunos casos, como con MitraClip o el cierre de fugas perivalvulares, el ecocardiograma transesofágico tridimensional en tiempo real proporciona ventajas en diferentes etapas del procedimiento, por lo que es preciso disponer de esta herramienta en los centros donde se atienden estas lesiones22.
Actualmente se dispone, además, de una innovadora tecnología que permite la fusión de imágenes de escopia por rayos X y de ecocardiografía en 2 y 3 dimensiones en tiempo real23,24. El movimiento del arco de rayos X se sincroniza con la sonda transesofágica del ecocardiograma, y se cortan automáticamente los distintos planos ecocardiográficos según la posición del tubo de rayos X. Esto permite integrar ambas imágenes, lo que facilita algunas de las etapas de procedimientos como el implante de MitraClip, el cierre de la orejuela o el cierre de fugas perivalvulares.
Requisitos de la unidad de hemodinámica e intervencionismo cardiacoEl documento de estándares que definen de manera integral los requisitos de carácter organizativo, estructural y de recursos de una unidad de hemodinámica e intervencionismo cardiaco datan de 200125. Aunque han pasado muchos años, muchas de estas recomendaciones siguen teniendo validez actual, y su cumplimiento asegura las adecuadas calidad asistencial y seguridad en las actuaciones clínicas e intervencionistas.
Durante los últimos años se han publicado nuevas recomendaciones tanto de la Sociedad Española de Cardiología26 como del American College of Cardiology27.
Ciclo de la vida de las salas de radiología para uso en hemodinámica y cardiología intervencionistaComo otras técnicas de imagen, las salas de intervencionismo tienen una expectativa de vida basada no solo en los años, sino también en el grado de su utilización. Otros factores que considerar serían el mantenimiento, la posibilidad de reemplazar partes o los requisitos para determinado tipo de tratamiento.
Según la guía de 2013 de la Canadian Association of Radiologists7, la expectativa de vida de una sala de intervencionismo sería 8 años si la utilización de la sala es alta (> 4.000 exámenes/año), 10 cuando es media (2.000-4.000 exámenes/año) y 12 años si es baja (< 2.000 exámenes/año). Sin embargo, las recomendaciones en cuanto a durabilidad de otras instituciones o Estados son diferentes; en España, en los estándares de las unidades asistenciales del área del corazón del Ministerio de Sanidad se recomienda la renovación de los equipos de hemodinámica cada 7 años28.
Otro aspecto importante es el control y el mantenimiento de los equipos para asegurar un correcto funcionamiento y su durabilidad y evitar problemas derivados de fallos en el equipo que pueden ser importantes para el paciente y el personal sanitario. Sin embargo, a pesar de la importancia de este aspecto, según el informe sobre el perfil tecnológico sanitario en España de Fenin8, el grado de cobertura de los sistemas de mantenimiento preventivo para las salas de hemodinámica es anormalmente bajo (58%), con las implicaciones que esto puede conllevar.
Perfil tecnológico en EspañaEl análisis del perfil tecnológico se basa en la metodología descrita en el estudio previo de Fenin «Perfil Tecnológico Hospitalario en España». Además, se ha utilizado el documento sobre el estado de obsolescencia de las tecnologías de imagen médica en Europa publicado por COCIR1, lo que permite situar a España en el contexto europeo.
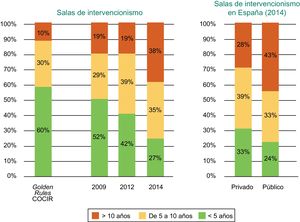
Según el informe de Fenin2, el perfil tecnológico de las salas de intervencionismo instaladas en España dista mucho de las recomendaciones de COCIR. En 2014, solo el 27% de los equipos instalados tenían una antigüedad inferior a 5 años; el 35%, entre 6 y 10 años, y el 38%, más de 10. Asimismo, se reseña el deterioro progresivo producido en los últimos años, ya que en 2009 el 52% de las salas tenían menos de 5 años; el 29%, entre 6 y 10, y el 19%, más de 10, cifras todas ellas mucho más próximas a las reglas de COCIR (figura 8).
Antigüedad de los equipos de intervencionismo cardiaco instalados en España según el año (2009, 2012 y 2014) y según centros públicos o privados. COCIR: European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry. Reproducido con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
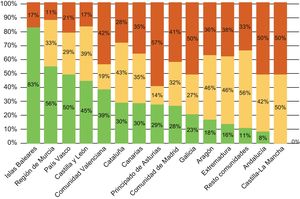
Dentro de España también hay una importante variabilidad. Castilla-La Mancha, Andalucía, Extremadura y Aragón son las comunidades autónomas con mayor grado de obsolescencia de este tipo de equipos (figura 9).
Distribución de los equipos de intervencionismo cardiaco instalados en España en el año 2014 por comunidades autónomas. Reproducido con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
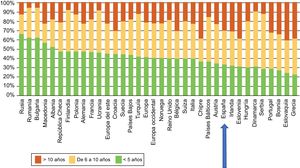
En Europa, la tendencia ha sido similar y el perfil de edad de estas tecnologías también ha experimentado un deterioro progresivo respecto a años previos. Los equipos instalados de más de 6 años están sustancialmente por encima del 60% en muchos países; en Grecia, el 77,1%; en Portugal, el 70,7%; en Dinamarca, el 69,3%, y en España, el 66,7%2 (figura 10).
Antigüedad de los equipos de intervencionismo cardiaco en Europa en el año 2014. COCIR: European Coordination Committee of the Radiological, Electromedical and Healthcare IT Industry. Adaptado con permiso de Federación Española de Empresas de Tecnología Sanitaria (Fenin)2.
Por lo tanto, se contribuiría a asegurar la calidad asistencial si se efectuase la correspondiente valoración de potencialidades y elementos de imprescindible dotación de cada equipo (tabla 5).
Requisitos de equipamiento de un laboratorio de hemodinámica en función de sus características
| Características | Uso clínico habitual | Uso clínico de alta especialización |
|---|---|---|
| Equipo de Rx | Equipo de angiografía digital fijo | Equipo de angiografía digital fijo |
| Datos de paciente | Importación automática | Importación automática |
| Cuantificación coronaria | Reserva fraccional de flujo | Reserva fraccional de flujo Ecografía intravascular o tomografía de coherencia óptica |
| Ecografía | Sonda multiplanar bidimensional | Sonda multiplanar tridimensional |
| Almacenamiento | Formato DICOM PACS | Formato DICOM PACS |
| Cirugía | Transferencia a hospital con CCV < 30 min | Bypass cardiopulmonar ≤ 90 min |
CCV: cirugía cardiovascular; DICOM: Digital Imaging and Communications in Medicine; PACS: Picture Archiving and Communication System; Rx: radiodiagnóstico.
La práctica de la electrofisiología intervencionista ha experimentado un extraordinario avance durante los últimos 15 años debido a la expansión de los sistemas de navegación no fluoroscópica y el abordaje de sustratos complejos, como la taquicardia ventricular o la fibrilación auricular. La elevada complejidad técnica de estos procedimientos es la causa de que el equipamiento material de los laboratorios de electrofisiología sea uno de los pilares para alcanzar la excelencia clínica en esta disciplina de la cardiología.
Equipamiento físicoCualquier unidad de electrofisiología debiera contar con los siguientes requisitos y dependencias para cumplir una adecuada labor clínica:
- •
El espacio físico debe tener un acceso razonable a la unidad de cuidados intensivos, planta de hospitalización y quirófanos.
- •
Debe disponer de 1 o más salas de intervencionismo con dedicación exclusiva, con una superficie de al menos 30 m2. Para un volumen de ablaciones superior a 200 al año, se recomienda disponer de 2 salas.
- •
Las salas de electrofisiología deben disponer de los aspectos habituales de una unidad de intervencionismo, que incluyan acondicionamiento de aire estándar, tomas de oxígeno, aire y vacío, etc. No es necesaria su quirofanización, salvo que se emplee para el implante de dispositivos.
- •
Dada la necesidad de integración de imágenes (fundamentalmente los ECG intracavitarios, la imagen procedente de los sistemas de navegación no fluoroscópica y la fluoroscopia), es altamente recomendable que la sala disponga de una única pantalla que recoja la información proveniente de diversas fuentes.
- •
Una sala de control, dotada de pantallas esclavas para los sistemas de fluoroscopia, poligrafía y navegación no fluoroscópica, así como 2 estaciones de trabajo con acceso a los sistemas electrónicos de historia clínica del hospital.
- •
Se debe dotar a la unidad de un espacio físico dedicado a la preparación y/o recuperación del paciente o a la realización de técnicas sencillas, como cardioversiones eléctricas. Ello permite agilizar la rotación de los pacientes y optimizar los recursos más complejos.
En la electrofisiología cardiaca, tanto para ablación como para el implante de dispositivos, los sistemas de radioscopia tienen un papel menos destacado que en el tratamiento de la enfermedad coronaria. La mayoría de los procedimientos se guían por sistemas de navegación no fluoroscópica, pese a lo cual los sistemas de radioscopia son fundamentales para varias etapas del procedimiento.
- •
Cada sala de electrofisiología debiera estar dotada de un equipo de angiografía digital monoplano fijo con las capacidades básicas. Se debe considerar la opción de angiografía digital en los centros cuya disponibilidad de TC cardiaca y equipos con tecnología biplanar no sea la óptima, especialmente en caso de que se realicen regularmente procedimientos pediátricos.
- •
Cuando haya 2 salas y en una de ellas se realicen mayoritariamente implantes de dispositivos, puede considerarse que la segunda sala disponga de un equipo de radioscopia más sencillo, como un sistema portátil de última generación (arco C móvil con intensificador de imagen).
Los sistemas de navegación no fluoroscópica son esenciales no solo para la reducción de la radiación absorbida por los pacientes y el personal sanitario, sino para asegurar el correcto posicionamiento tridimensional de los catéteres durante los procedimientos de mapeo intracardiaco y para la correcta localización de las lesiones generadas29.
A la vista de su importancia, se considera que una sala de electrofisiología en la que se realicen procedimientos terapéuticos de ablación debe disponer de al menos un sistema de navegación no fluoroscópica.
La dotación de sistemas adicionales depende del volumen de la unidad y otras consideraciones, como la existencia de programas de investigación, etc., pero también se ha de tener en cuenta que no es conveniente la excesiva atomización de procedimientos con diferentes sistemas de navegación para asegurar una correcta experiencia entre los diferentes operadores. Se considera que, a partir de 100 procedimientos de ablación con navegación no fluoroscópica, se debe tomar en consideración instalar un sistema de navegación no fluoroscópica adicional.
Sistemas adicionalesLo incluyen una serie de equipos necesarios para la realización de los procedimientos más frecuentes en electrofisiología clínica.
- •
Sistema de poligrafía. El análisis de los patrones de activación y secuencias de los electrogramas intracavitarios siguen siendo la base para el diagnóstico y la aproximación terapéutica. Cada sala de electrofisiología debe estar equipada con un sistema de poligrafía digital con un mínimo de 64 canales intracavitarios, ECG de superficie y módulo básico de hemodinámica para el registro de las presiones intracavitarias. Las señales intracavitarias son especialmente sensibles al ruido, por ello la sala debe disponer de una instalación de calidad que permita el correcto registro de múltiples señales sin interferencias.
- •
Equipo de crioablación. La crioablación aporta ventajas sobre la radiofrecuencia en vías parahisianas y taquicardias intranodulares en niños. Es muy recomendable que esté disponible en centros de más de 200 ablaciones al año. En la fibrilación auricular (FA) permite procedimientos con resultados similares a los de la radiofrecuencia, pero es una técnica menos exigente para el operador. Su incorporación es muy recomendable en centros con más de 50 ablaciones de FA al año. En cualquier caso, en los centros donde se realicen ablaciones de FA, siempre debe ser posible realizarlas mediante procedimiento de ablación punto a punto con guía mediante sistema de navegación no fluoroscópica.
- •
Fuente de radiofrecuencia. La unidad de electrofisiología debe disponer de al menos 2 fuentes de radiofrecuencia con sistemas compatibles de bomba de infusión para catéteres irrigados.
- •
Consola de ultrasonidos con capacidad para ecocardiografía transesofágica y ecografía intracardiaca. Disponer de un equipo básico de ecocardiografía es fundamental para la detección precoz de las complicaciones, así como para el apoyo para técnicas sencillas, como la punción transeptal, o más sofisticadas, como la ecografía intracardiaca.
- •
Monitor/desfibrilador. Se debe disponer de un sistema de desfibrilación externa con disponibilidad de funcionamiento manual para cada una de las salas.
- •
Sistemas de navegación robótica. Los sistemas de navegación robótica son una herramienta de alto coste económico cuya utilidad práctica hoy está en discusión. Se puede considerar su adopción en unidades de alto volumen (más de 250 ablaciones anuales) que dispongan de más de una sala de electrofisiología y programas de investigación.
Por lo tanto, se contribuiría a asegurar la calidad asistencial si se efectuase la correspondiente valoración de potencialidades y elementos de imprescindible dotación de cada equipo (tabla 6).
Requisitos mínimos de una sala de electrofisiología
| Uso clínico habitual | |
|---|---|
| Aspectos generales | Filtros de aire HEPA Tomas de oxígeno, aire y vacío Acceso a hospitalización, UCI, quirófano, etc. |
| Sala de control | Pantallas esclavas para los sistemas de fluoroscopia, poligrafía y navegación no fluoroscópica Estaciones de trabajo con acceso a los sistemas electrónicos de historia clínica del hospital |
| Espacio antesala | Preparación y/o recuperación del paciente |
| Equipo de radiodiagnóstico | Equipo de angiografía digital fijo |
| Informe de radiación | Obligatorio |
| Almacenamiento | Formato DICOM PACS |
| Polígrafo | Poligrafía digital con un mínimo de 64 canales intracavitarios y ECG de superficie Módulo básico de presiones intracavitarias |
| Sistemas de navegación | Al menos un sistema de navegación no fluoroscópico (CARTO, NavX, Rhythmia) |
| Ecocardiografía | Ecocardiógrafo transtorácico y transesofágico Recomendable ecocardiógrafo intracardiaco |
DICOM: Digital Imaging and Communications in Medicine; ECG: electrocardiograma; HEPA: High Efficiency Particulate Air; PACS: Picture Archiving and Communication System; UCI: unidad de cuidados intensivos.
La cardiología como disciplina médica ha experimentado un considerable avance durante las últimas 2 décadas, lo que ha permitido reducir significativamente la mortalidad de las principales enfermedades cardiovasculares. Esta increíble mejora no es ajena a la innovación tecnológica. El desarrollo de nuevos y mejores equipos ha permitido a los cardiólogos tratar a más pacientes y con mejores resultados. Mantener la innovación y mejorar la tecnología disponible de una manera razonable es esencial para continuar mejorando la práctica clínica y garantizar resultados en salud.
Este informe trata de ser una referencia para armonizar el tipo de tecnología necesaria en los principales procedimientos cardiológicos.
CONFLICTO DE INTERESESNo se declara ninguno.