Analizar la razón de coste-efectividad y el impacto presupuestario del tratamiento con evolocumab (inhibidor de la PCSK9) para pacientes en prevención secundaria en el Sistema Nacional de Salud español.
MétodosSe realizaron, desde la perspectiva del sistema sanitario público, análisis de impacto presupuestario, modelos de árbol de decisión y Markov, basándose en el único ensayo clínico con datos de morbimortalidad (FOURIER). Las alternativas comparadas fueron evolocumab frente a estatinas y un 5% ezetimiba conjuntamente. La medida de eficacia utilizada fue el número de eventos cardiovasculares evitados. Se realizaron análisis de sensibilidad univariable y probabilístico.
ResultadosEl coste sanitario promedio de los pacientes tratados a 26 meses con evolocumab fue de 11.134,78 euros y de 393,83 euros con el estándar (estatinas + ezetimiba). El coste-efectividad incremental superó los 600.000 euros por evento cardiovascular evitado en las 2 variables (primera: muerte cardiovascular, infarto de miocardio, accidente cerebrovascular, hospitalización por angina inestable o revascularización coronaria; segunda: incluye los 3 primeros eventos). A 10 años, el modelo de Markov mostró un coste promedio de 471.417,37 frente a 13.948,45 euros con evolocumab y estándar respectivamente. El tratamiento con evolocumab en hipercolesterolemia familiar supondría anualmente entre 3 y 6,1 millones de euros, lo que supone una diferencia de 2,5-5,1 millones de euros con el tratamiento estándar (2017). Para el año 2021, en hipercolesterolemia no familiar (prevención secundaria), la diferencia osciló entre 204,3 y 1.364,7 millones de euros.
ConclusionesEl evolocumab se asocia con menor frecuencia de eventos cardiovasculares, pero resulta ineficiente para los pacientes susceptibles de recibirlo en el Sistema Nacional de Salud.
Palabras clave
Las enfermedades cardiovasculares conllevan una elevada incidencia de morbimortalidad1. Uno de los principales factores de riesgo de evento cardiovascular es el perfil lipídico aterogénico del paciente, y destacan las altas concentraciones de colesterol unido a lipoproteínas de baja densidad (cLDL). En pacientes con intolerancia a las estatinas o que las tengan contraindicadas (tratamiento estándar), se ha demostrado que los inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (PCSK9) producen una notable reducción del cLDL2.
Una revisión Cochrane (2017) que incluyó 20 ensayos clínicos con 67.237 participantes (mediana de edad, 61 [intervalo, 52–64] años) encontró que los inhibidores de la PCSK9 mostraban una reducción del cLDL del 53,86% (intervalo de confianza del 95% [IC95%], 58,64-49,08; 4.782 participantes) frente a placebo, del 30,20% (IC95%, 34,18-26,23; 823 participantes) frente a ezetimiba y del 39,20% (IC95%, 56,15-22,26; 5.376 participantes) frente a estatinas y ezetimiba2. Los estudios incluidos presentaban un seguimiento corto (máximo 26 meses) y, aunque su objetivo principal no era comprobar la reducción de eventos cardiovasculares, se observó un discreto efecto protector (< 1%), con elevada incertidumbre. En marzo de 2017 se publicó el primer estudio realizado con un inhibidor de la PCSK9 (evolocumab), con medidas de resultado finales que estimaban la morbimortalidad cardiovascular tras un seguimiento de 26 meses3. Actualmente se está realizando otro amplio estudio de morbimortalidad con alirocumab4.
La Agencia Europea del Medicamento ha aprobado el uso de los inhibidores de la PCSK9 alirocumab y evolocumab para la hipercolesterolemia familiar o en prevención secundaria, para pacientes con niveles de colesterol insuficientemente controlados con estatinas, por refractariedad o intolerancia. Estos fármacos se comercializaron a un coste muy superior que el resto de los medicamentos hipocolesterolemiantes, cuando aún no se disponía de estudios de morbimortalidad adecuados5,6. En un contexto de recursos limitados, es necesario incrementar la eficiencia de los tratamientos disponibles. Por este motivo, el objetivo de este estudio es estimar la razón de coste-efectividad del tratamiento con evolocumab y su impacto presupuestario en el Sistema Nacional de Salud español.
MÉTODOSSe realizaron 2 tipos de análisis de evaluación económica. Un árbol de decisión (horizonte, 26 meses) y una simulación a 10 años mediante un modelo de Markov, a partir de la modelización de las curvas de supervivencia7. Ambos análisis utilizaron los datos del ensayo FOURIER3, y se consideró como medida de efectividad los eventos cardiovasculares evitados.
Opciones de tratamientoSe analizó la adición de evolocumab al tratamiento estándar con estatinas de acuerdo a las características basales de los pacientes incluidos en el ensayo clínico3. Aunque los pacientes estaban tratados con 420mg cada 4 semanas o 140mg cada 2 semanas, para el cálculo de costes se consideró esta última pauta, que es la disponible según la ficha técnica, presumiéndose una eficacia similar, al carecer de información desagregada. En el estudio, aproximadamente un 70% de los pacientes se trataban con estatinas de elevada intensidad y un 30%, con moderada intensidad. En ambos casos se tuvo en cuenta que alrededor del 5% de los pacientes recibían concomitantemente ezetimiba. La tabla 13,5,8–11 muestra los diferentes datos de costes y eficacia utilizados.
Medidas de eficaciaIdealmente, un análisis de coste-efectividad toma como medida de resultado los años de vida ajustados por calidad. Sin embargo, este análisis se centró en la comparación de la eficacia y el coste de las tecnologías para evitar eventos cardiovasculares. Las medidas utilizadas fueron las consideradas en el estudio FOURIER3: a) primaria: muerte cardiovascular, infarto de miocardio, accidente cerebrovascular, hospitalización por angina inestable o revascularización coronaria, y b) secundaria: muerte cardiovascular, infarto de miocardio o accidente cerebrovascular.
Estimación de costesSe utilizó la perspectiva del sistema sanitario público español; por ello no se incluyeron los costes indirectos por la pérdida de productividad. La estimación del coste de los eventos identificados se calculó a partir de los Grupos Relacionados por el Diagnóstico12, según la aparición de eventos en el estudio FOURIER3 y ponderando la gravedad por la incidencia en el Sistema Sanitario Público de Andalucía. Para la estimación del coste del tratamiento farmacológico de evolocumab, se consideró el coste unitario extraído del Nomenclátor (septiembre 2017). El coste del tratamiento con ezetimiba se obtuvo del BOT8 y el de las estatinas, de Villa et al.9.
Análisis del impacto presupuestarioSiguiendo los criterios del Informe de Posicionamiento Terapéutico de evolocumab, los pacientes susceptibles de tratamiento eran los no controlados (cLDL ≤ 100 mg/dl), ya fuera por inefectividad con dosis máxima de estatinas, intolerancia o contraindicación, tanto para aquellos con hipercolesterolemia familiar (homocigótica y heterocigótica) como para los que presentaban enfermedad cardiovascular establecida13.
El análisis de impacto presupuestario14 para los pacientes en prevención secundaria10,11 se realizó con base en los datos de prevalencia con un horizonte temporal de 5 años (2017-2021) (tabla 1). Para la estimación de la población susceptible, se utilizaron los datos de diferentes registros y publicaciones, y cuando fue necesario se extrapoló al total nacional15–21. Además, se consideró que el 14% de los individuos no alcanzaban valores de cLDL < 100 mg/dl, ya sea por inefectividad a dosis máximas toleradas o por intolerancia a las estatinas. Para el análisis de sensibilidad, se utilizó un intervalo de prevalencias entre el 0,9 y el 6,01% (). Se asumió para ambas alternativas que todos los pacientes estaban en tratamiento con evolocumab + estatinas frente a estatinas o estatinas + ezetimiba (en un 5% de los casos) y su probabilidad de eventos. Las poblaciones (mayores de 18 años) para cada uno de los años analizados en España se obtuvieron de la estimación de población del Instituto Nacional de Estadística (2016)22.
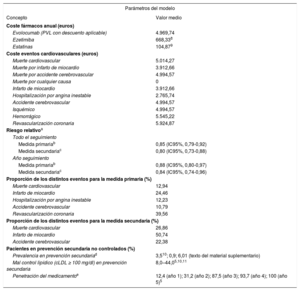
Valores de prevalencia, eficacia y costes en los análisis de impacto presupuestario y de evaluación económica
| Parámetros del modelo | |
|---|---|
| Concepto | Valor medio |
| Coste fármacos anual (euros) | |
| Evolocumab (PVL con descuento aplicable) | 4.969,74 |
| Ezetimiba | 668,338 |
| Estatinas | 104,879 |
| Coste eventos cardiovasculares (euros) | |
| Muerte cardiovascular | 5.014,27 |
| Muerte por infarto de miocardio | 3.912,66 |
| Muerte por accidente cerebrovascular | 4.994,57 |
| Muerte por cualquier causa | 0 |
| Infarto de miocardio | 3.912,66 |
| Hospitalización por angina inestable | 2.765,74 |
| Accidente cerebrovascular | 4.994,57 |
| Isquémico | 4.994,57 |
| Hemorrágico | 5.545,22 |
| Revascularización coronaria | 5.924,87 |
| Riesgo relativoa | |
| Todo el seguimiento | |
| Medida primariab | 0,85 (IC95%, 0,79-0,92) |
| Medida secundariac | 0,80 (IC95%, 0,73-0,88) |
| Año seguimiento | |
| Medida primariab | 0,88 (IC95%, 0,80-0,97) |
| Medida secundariac | 0,84 (IC95%, 0,74-0,96) |
| Proporción de los distintos eventos para la medida primaria (%) | |
| Muerte cardiovascular | 12,94 |
| Infarto de miocardio | 24,46 |
| Hospitalización por angina inestable | 12,23 |
| Accidente cerebrovascular | 10,79 |
| Revascularización coronaria | 39,56 |
| Proporción de los distintos eventos para la medida secundaria (%) | |
| Muerte cardiovascular | 26,86 |
| Infarto de miocardio | 50,74 |
| Accidente cerebrovascular | 22,38 |
| Pacientes en prevención secundaria no controlados (%) | |
| Prevalencia en prevención secundariad | 3,510; 0,9; 6,01 () |
| Mal control lipídico (cLDL ≥ 100 mg/dl) en prevención secundaria | 8,0–44,05,10,11 |
| Penetración del medicamentoe | 12,4 (año 1); 31,2 (año 2); 87,5 (año 3); 93,7 (año 4); 100 (año 5)5 |
cLDL: colesterol unido a lipoproteínas de baja densidad; IC95%: intervalo de confianza del 95%; PVL: precio de venta de laboratorio.
Datos del estudio FOURIER3: incluye a pacientes en prevención secundaria con intolerancia a estatinas o sin adecuada respuesta.
Los árboles de decisión representan de manera simplificada la elección de la alternativa más coste-efectiva. Los resultados se expresan en términos de coste por evento cardiovascular evitado con evolocumab (evolocumab + estatinas) frente al tratamiento estándar (estatinas y estatinas + ezetimiba), mediante el cálculo de la razón de coste-efectividad incremental (RCEI) = (coste alternativa B – coste alternativa A) / (eficacia B – eficacia A).
Con objeto de evaluar la incertidumbre, se realizó un análisis de sensibilidad univariable reduciendo un 46% el precio del evolocumab23, además de un análisis probabilístico con la frecuencia de eventos de las medidas primaria y secundaria (distribución probabilística beta), el cual permitió valorar la incertidumbre paramétrica de las probabilidades mediante 1.000 simulaciones. Para ello se utilizó Excel.
Efectividad y asunciones del modelo de MarkovSe consideraron 2 estados de salud mutuamente excluyentes para simular la progresión de la enfermedad. Toda la cohorte de pacientes entró en el modelo desde el estado «libres de progresión» y permanecieron en este estado o transitaron al estado «nuevo evento» dependiendo de las diferentes probabilidades de transición. Se asumió una proporción general de cada tipo de evento en el cómputo final. En este tipo de modelos, las transiciones entre los estados se realizaban en periodos discretos denominados «ciclos», con una duración de 1 mes, y se utilizó un horizonte temporal de 120 meses. Según las recomendaciones de López Bastida et al.24, se aplicaron diferentes análisis de sensibilidad con tasas de descuento del 3,5 y el 6% (la tasa de descuento se refería a que los costes y las consecuencias pueden ocurrir en un tiempo variable, aunque la comparación se realice en el momento actual, por ello la tasa de descuento es una tasa de ajuste del paso del tiempo).
Para el cálculo de probabilidades mensuales se realizó una modelización de las curvas de supervivencia. Así, a partir de los puntos obtenidos digitalizando las curvas de supervivencias y de los datos agregados de supervivencia de la publicación, se recrearon las curvas de Kaplan-Meier, según el algoritmo descrito por Guyot et al.25. Se calculó la hazard ratio (HR) por regresión de Cox para comparar los datos obtenidos con los originales. Se analizaron distintas distribuciones paramétricas (exponencial, lognormal, Weibull, gamma, gamma-generalizada y log-logística), y se seleccionó aquella con mejor ajuste según los criterios de información de Akaike y bayesiano (). Finalmente, se calculó el área bajo la curva (ABC) utilizando la regla de Simpson, que representa el tiempo medio que los pacientes estaban libres de evento () ABC0→36meses y ABC0→120meses para ambas ramas y para las 2 variables analizadas. Todo ello se realizó con el programa estadístico R y el paquete Flexsurv26.
RESULTADOSAnálisis de coste-efectividad: árbol de decisiónLos resultados a 26 meses mostraban que los tratados con evolocumab obtuvieron una tasa de eventos para las medidas primaria y secundaria del 9,8 y el 5,9%, que con el tratamiento estándar fueron respectivamente del 11,3 y el 7,4%. El coste promedio de los pacientes en tratamiento con evolocumab a los 26 meses, para las variables primaria y secundaria, fueron de 11.134,78 y 11.088,46 euros respectivamente, y 393,83 y 328,15 euros para aquellos en tratamiento estándar. La RCEI fue de 633.684,39 euros para la medida primaria, que representa el coste adicional por evento cardiovascular o muerte evitado, mientras que para la medida secundaria fue de 717.354,20 euros. Al realizar un análisis de sensibilidad reduciendo en un 46% el precio del evolocumab, las RCEI fueron de 341.795,91 y 387.520,21 euros respectivamente. Por último, el análisis probabilístico, tanto para la medida de efectividad primaria como para la secundaria, mostraba que la RCEI osciló entre 716.857,98 y 776.333,52 euros (tabla 2).
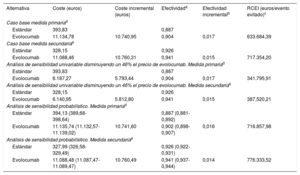
Coste-efectividad incremental del tratamiento con evolocumab frente al tratamiento estándar, caso base y análisis de sensibilidad con horizonte temporal de 26 meses
| Alternativa | Coste (euros) | Coste incremental (euros) | Efectividada | Efectividad incrementalb | RCEI (euros/evento evitado)c |
|---|---|---|---|---|---|
| Caso base medida primariad | |||||
| Estándar | 393,83 | 0,887 | |||
| Evolocumab | 11.134,78 | 10.740,95 | 0,904 | 0,017 | 633.684,39 |
| Caso base medida secundariae | |||||
| Estándar | 328,15 | 0,926 | |||
| Evolocumab | 11.088,46 | 10.760,31 | 0,941 | 0,015 | 717.354,20 |
| Análisis de sensibilidad univariable disminuyendo un 46% el precio de evolocumab. Medida primariad | |||||
| Estándar | 393,83 | 0,887 | |||
| Evolocumab | 6.187,27 | 5.793,44 | 0,904 | 0,017 | 341.795,91 |
| Análisis de sensibilidad univariable disminuyendo un 46% el precio de evolocumab. Medida secundariae | |||||
| Estándar | 328,15 | 0,926 | |||
| Evolocumab | 6.140,95 | 5.812,80 | 0,941 | 0,015 | 387,520,21 |
| Análisis de sensibilidad probabilístico. Medida primariad | |||||
| Estándar | 394,13 (389,68-398,64) | 0,887 (0,881-0,892) | |||
| Evolocumab | 11.135,74 (11.132,57-11.139,02) | 10.741,60 | 0,902 (0,898-0,907) | 0,016 | 716.857,98 |
| Análisis de sensibilidad probabilístico. Medida secundariae | |||||
| Estándar | 327,99 (326,58-329,49) | 0,926 (0,922-0,931) | |||
| Evolocumab | 11.088,48 (11.087,47-11.089,47) | 10.760,49 | 0,941 (0,937-0,944) | 0,014 | 776.333,52 |
RCEI: razón de coste-efectividad incremental.
El análisis de sensibilidad probabilístico se basa en realizar cientos de simulaciones variando aleatoriamente los valores de los parámetros según su distribución de probabilidad.
Por lo que respecta a la variable principal, el valor de la HR obtenida, mediante las cohortes simuladas, fue similar al descrito en el ensayo (HR = 0,85; IC95%, 0,79-0,91). En la modelización de las curvas de supervivencia ( y ), la distribución lognormal fue la función que presentó mejor ajuste para ambas ramas (). En el caso de la variable secundaria, la HR obtenida también fue similar que la original (HR = 0,80; IC95%, 0,73-0,87). Una vez definidas las curvas de supervivencia, se calculó la incidencia acumulada a los 120 meses, que en los grupos de evolocumab y de control alcanzó valores de 0,263 (IC95%, 0,251-0,279) y 0,313 (IC95%, 0,298-0,330) en el caso de la variable principal y 0,168 (IC95%, 0,156-0,182) y 0,216 (IC95%, 0,202-0,232) para la variable secundaria.
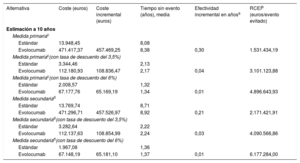
La tabla 3 muestra el análisis del modelo de Markov a 10 años. Así, el coste promedio del tratamiento estándar fue de 13.948,45 euros, frente a 471.417,37 euros con evolocumab. Así, a los 10 años, la RCEI obtenida fue de 1.531.434,19 euros, lo que supone el coste de evitar 1 evento cardiovascular adicional al cambiar del tratamiento estándar al tratamiento con evolocumab, que fue de 3.101.123,88 y 4.896.643,93 euros utilizando las tasas de descuento del 3,5 y el 6%. Para la medida secundaria, pasar del tratamiento estándar al tratamiento con evolocumab suponía pagar 2.171.421,91 euros adicionales por cada evento evitado y 4.090.566,86 y 6.177.284,00 euros al aplicar las tasas de descuento del 3,5 y el 6%.
Modelo de Markov del tratamiento con evolocumab frente al tratamiento estándar, con y sin tasa de descuento con horizonte temporal de 10 años
| Alternativa | Coste (euros) | Coste incremental (euros) | Tiempo sin evento (años), media | Efectividad incremental en añosa | RCEIb (euros/evento evitado) |
|---|---|---|---|---|---|
| Estimación a 10 años | |||||
| Medida primariac | |||||
| Estándar | 13.948,45 | 8,08 | |||
| Evolocumab | 471.417,37 | 457.469,25 | 8,38 | 0,30 | 1.531.434,19 |
| Medida primariac(con tasa de descuento del 3,5%) | |||||
| Estándar | 3.344,46 | 2,13 | |||
| Evolocumab | 112.180,93 | 108.836,47 | 2,17 | 0,04 | 3.101.123,88 |
| Medida primariac(con tasa de descuento del 6%) | |||||
| Estándar | 2.008,57 | 1,32 | |||
| Evolocumab | 67.177,76 | 65.169,19 | 1,34 | 0,01 | 4.896.643,93 |
| Medida secundariad | |||||
| Estándar | 13.769,74 | 8,71 | |||
| Evolocumab | 471.296,71 | 457.526,97 | 8,92 | 0,21 | 2.171.421,91 |
| Medida secundariad(con tasa de descuento del 3,5%) | |||||
| Estándar | 3.282,64 | 2,22 | |||
| Evolocumab | 112.137,63 | 108.854,99 | 2,24 | 0,03 | 4.090.566,86 |
| Medida secundariad(con tasa de descuento del 6%) | |||||
| Estándar | 1.967,08 | 1,36 | |||
| Evolocumab | 67.148,19 | 65.181,10 | 1,37 | 0,01 | 6.177.284,00 |
RCEI: Ratio Coste Efectividad incremental, que representa el coste adicional por evento cardiovascular o muerte evitado.
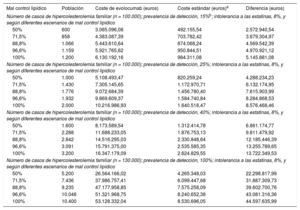
El impacto presupuestario se analizó comparando el tratamiento con evolocumab (evolocumab + estatinas) frente al tratamiento estándar (estatinas + ezetimiba), según diferentes escenarios para el año 2017. Así, el primero de ellos consideró un total de pacientes con hipercolesterolemia familiar de 100.000, una prevalencia de detección del 15% y una franja de mal control lipídico entre el 50 y el 100%. Así, el tratamiento con evolocumab supondría un coste que oscilaría entre 3 y 6,1 millones de euros, lo que supone una diferencia frente al tratamiento estándar de 2,5 y 5,1 millones de euros respectivamente. En los diferentes escenarios considerados, la gama de valores de la diferencia con el tratamiento estándar osciló entre 4,2 y 44,5 millones de euros (tabla 4).
Coste anual de los pacientes con hipercolesterolemia familiar según diferentes escenarios (2017)
| Mal control lipídico | Población | Coste de evolocumab (euros) | Coste estándar (euros)a | Diferencia (euros) |
|---|---|---|---|---|
| Número de casos de hipercolesterolemia familiar (n = 100.000); prevalencia de detección, 15%b; intolerancia a las estatinas, 8%, y según diferentes escenarios de mal control lipídico | ||||
| 50% | 600 | 3.065.096,08 | 492.155,54 | 2.572.940,54 |
| 71,5% | 858 | 4.383.087,39 | 703.782,42 | 3.679.304,97 |
| 88,8% | 1.066 | 5.443.610,64 | 874.068,24 | 4.569.542,39 |
| 96,6% | 1.159 | 5.921.765,62 | 950.844,51 | 4.970.921,12 |
| 100% | 1.200 | 6.130.192,16 | 984.311,08 | 5.145.881,08 |
| Número de casos de hipercolesterolemia familiar (n = 100.000); prevalencia de detección, 25%; intolerancia a las estatinas, 8%, y según diferentes escenarios de mal control lipídico | ||||
| 50% | 1.000 | 5.108.493,47 | 820.259,24 | 4.288.234,23 |
| 71,5% | 1.430 | 7.305.145,65 | 1.172.970,71 | 6.132.174,95 |
| 88,8% | 1.776 | 9.072.684,39 | 1.456.780,40 | 7.615.903,99 |
| 96,6% | 1.932 | 9.869.609,37 | 1.584.740,84 | 8.284.868,53 |
| 100% | 2.000 | 10.216.986,93 | 1.640.518,47 | 8.576.468,46 |
| Número de casos de hipercolesterolemia familiar (n = 100.000); prevalencia de detección, 40%; intolerancia a las estatinas, 8%, y según diferentes escenarios de mal control lipídico | ||||
| 50% | 1.600 | 8.173.589,54 | 1.312.414,78 | 6.861.174,77 |
| 71,5% | 2.288 | 11.688.233,05 | 1.876.753,13 | 9.811.479,92 |
| 88,8% | 2.842 | 14.516.295,03 | 2.330.848,64 | 12.185.446,39 |
| 96,6% | 3.091 | 15.791.375,00 | 2.535.585,35 | 13.255.789,65 |
| 100% | 3.200 | 16.347.179,09 | 2.624.829,55 | 13.722.349,53 |
| Número de casos de hipercolesterolemia familiar (n = 130.000); prevalencia de detección, 100%; intolerancia a las estatinas, 8%, y según diferentes escenarios de mal control lipídico | ||||
| 50% | 5.200 | 26.564.166,02 | 4.265.348,03 | 22.298.817,99 |
| 71,5% | 7.436 | 37.986.757,41 | 6.099.447,68 | 31.887.309,73 |
| 88,8% | 9.235 | 47.177.958,85 | 7.575.258,09 | 39.602.700,76 |
| 96,6% | 10.046 | 51.321.968,75 | 8.240.652,38 | 43.081.316,36 |
| 100% | 10.400 | 53.128.332,04 | 8.530.696,05 | 44.597.635,99 |
Se asume que el 8% de los pacientes con hipercolesterolemia familiar (homocigótica y heterocigótica) presentan intolerancia a las estatinas. Se indican posibles escenarios de mal control lipídico sin evolocumab según la bibliografía10,11,14 y distintas presunciones por elevada incertidumbre.
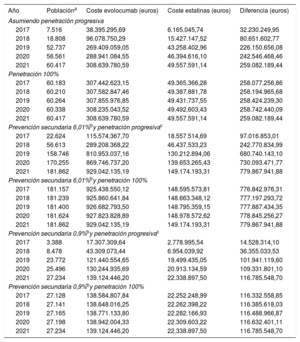
En cuanto al impacto presupuestario de los pacientes con hipercolesterolemia no controlada susceptibles de recibir tratamiento y según las asunciones consideradas, en el año 2017 habrá unos 7.516 pacientes en tratamiento, que en 2021 llegarían a 60.417, dependiendo de la penetración del fármaco. Para el año 2021 y considerando las diferentes asunciones, la diferencia de coste del tratamiento de evolocumab con el tratamiento estándar osciló entre los 116.785.548,70 y los 779.867.941,88 euros (tabla 5).
Coste de los pacientes en prevención secundaria con hipercolesterolemia no controlada susceptibles de tratamiento
| Año | Poblacióna | Coste evolocumab (euros) | Coste estatinas (euros) | Diferencia (euros) |
|---|---|---|---|---|
| Asumiendo penetración progresiva | ||||
| 2017 | 7.516 | 38.395.295,69 | 6.165.045,74 | 32.230.249,95 |
| 2018 | 18.808 | 96.078.750,29 | 15.427.147,52 | 80.651.602,77 |
| 2019 | 52.737 | 269.409.059,05 | 43.258.402,96 | 226.150.656,08 |
| 2020 | 56.561 | 288.941.084,55 | 46.394.616,10 | 242.546.468,46 |
| 2021 | 60.417 | 308.639.780,59 | 49.557.591,14 | 259.082.189,44 |
| Penetración 100% | ||||
| 2017 | 60.183 | 307.442.623,15 | 49.365.366,28 | 258.077.256,86 |
| 2018 | 60.210 | 307.582.847,46 | 49.387.881,78 | 258.194.965,68 |
| 2019 | 60.264 | 307.855.976,85 | 49.431.737,55 | 258.424.239,30 |
| 2020 | 60.338 | 308.235.043,52 | 49.492.603,43 | 258.742.440,09 |
| 2021 | 60.417 | 308.639.780,59 | 49.557.591,14 | 259.082.189,44 |
| Prevención secundaria 6,01%by penetración progresivac | ||||
| 2017 | 22.624 | 115.574.367,70 | 18.557.514,69 | 97.016.853,01 |
| 2018 | 56.613 | 289.208.368,22 | 46.437.533,23 | 242.770.834,99 |
| 2019 | 158.746 | 810.953.037,16 | 130.212.894,06 | 680.740.143,10 |
| 2020 | 170.255 | 869.746.737,20 | 139.653.265,43 | 730.093.471,77 |
| 2021 | 181.862 | 929.042.135,19 | 149.174.193,31 | 779.867.941,88 |
| Prevención secundaria 6,01%by penetración 100% | ||||
| 2017 | 181.157 | 925.438.550,12 | 148.595.573,81 | 776.842.976,31 |
| 2018 | 181.239 | 925.860.641,84 | 148.663.348,12 | 777.197.293,72 |
| 2019 | 181.400 | 926.682.793,50 | 148.795.359,15 | 777.887.434,35 |
| 2020 | 181.624 | 927.823.828,89 | 148.978.572,62 | 778.845.256,27 |
| 2021 | 181.862 | 929.042.135,19 | 149.174.193,31 | 779.867.941,88 |
| Prevención secundaria 0,9%by penetración progresivac | ||||
| 2017 | 3.388 | 17.307.309,64 | 2.778.995,54 | 14.528.314,10 |
| 2018 | 8.478 | 43.309.073,44 | 6.954.039,92 | 36.355.033,53 |
| 2019 | 23.772 | 121.440.554,65 | 19.499.435,05 | 101.941.119,60 |
| 2020 | 25.496 | 130.244.935,69 | 20.913.134,59 | 109.331.801,10 |
| 2021 | 27.234 | 139.124.446,20 | 22.338.897,50 | 116.785.548,70 |
| Prevención secundaria 0,9%by penetración 100% | ||||
| 2017 | 27.128 | 138.584.807,84 | 22.252.248,99 | 116.332.558,85 |
| 2018 | 27.141 | 138.648.016,25 | 22.262.398,22 | 116.385.618,03 |
| 2019 | 27.165 | 138.771.133,80 | 22.282.166,93 | 116.488.966,87 |
| 2020 | 27.198 | 138.942.004,33 | 22.309.603,22 | 116.632.401,11 |
| 2021 | 27.234 | 139.124.446,20 | 22.338.897,50 | 116.785.548,70 |
Se asume que el 14% de los pacientes tienen mal control lipídico pese al tratamiento optimizado con estatinas, incluida la intolerancia (8%). Coste promedio del paciente con evolocumab + estatinas, 5.511,30 euros y el de ezetimiba + estatinas, 820,26 euros.
El tratamiento con evolocumab se asocia con menor frecuencia de eventos cardiovasculares pero, según este estudio, no resulta eficiente para el Sistema Nacional de Salud. Así, los modelos de coste-efectividad realizados ponen de manifiesto que, por cada evento cardiovascular evitado, la RCEI es 650.000 euros superior comparado con el tratamiento estándar. Debido a la ausencia de umbral para este tipo de resultados en evaluación económica, resulta difícil aportar conclusiones que puedan confirmar que el tratamiento con evolocumab sea o no coste-efectivo.
LimitacionesUna de las limitaciones del presente trabajo es la proporción en el nivel de rigor de los Grupos Relacionados por el Diagnóstico12 para el cálculo de las complicaciones. Estos datos pueden diferir de los datos nacionales, aunque no es previsible una gran disparidad. No se tuvieron en cuenta los costes a medio o largo plazo de las complicaciones. Por otra parte, la modelización de las curvas de supervivencia permitió una estimación de los resultados a 10 años, pero es preciso reconocer que los datos conocidos reflejan un seguimiento de 26 meses, por lo que la incertidumbre del modelo es muy elevada. En este sentido, la carencia de datos suficientes para modelizar todos los eventos considerados y la necesidad de realizar presunciones demasiado aventuradas para llegar a determinar el coste/año de vida ajustado por calidad han hecho que se prefiera asumir esta limitación en lugar de presentar unos resultados de coste/utilidad poco sólidos para la toma de decisiones. Finalmente, y debido a la carencia de estudios con variables finales para estos pacientes, para el cálculo de costes e impacto presupuestario de la prevención primaria en pacientes con hipercolesterolemia familiar, se asumieron los datos de eficacia disponibles de pacientes con dislipemia en prevención secundaria.
El estudio FOURIER3 incluye población con cifras basales medias de cLDL no muy altas (92 mg/dl). La protección cardiovascular no mostró mejores resultados en pacientes con mayor colesterolemia basal: entre aquellos con las menores (< 80 mg/dl), el efecto protector obtuvo HR = 0,80 (IC95%, 0,69-0,93) frente a HR = 0,89 (IC95%, 0,77-1,02) en aquellos con más cLDL (> 109 mg/dl), sin diferencias significativas.
En la literatura médica se encontraron varios estudios de coste/utilidad que evaluaban el tratamiento basándose en la disminución del perfil lipídico de los pacientes con modelos a largo plazo. Aunque estos estudios mostraban una alta heterogeneidad, coinciden en unas elevadas RCEI, entre 268.637 y 506.000 dólares/año de vida ajustado por calidad27–29. Por el contrario, el estudio de Villa et al.9, realizado en España, encontró unas RCEI de 30.893 y 42.266 euros/año de vida ajustado por calidad. La diferencia entre los estudios puede deberse al precio del evolocumab, entre 14.000 y 14.600 dólares paciente/año27–29, mientras que en el estudio de Villa et al.9 el coste utilizado fue 4.969,60 euros paciente/año. Además, el estudio de Villa se basó en unas estimaciones de reducción de la mortalidad muy superiores a la descrita en el estudio FOURIER. Así, si en lugar de utilizar esas asunciones (basadas en la reducción de los niveles de cLDL) se hubieran basado en los datos del estudio FOURIER el valor del ratio coste utilidad hubiera sido más desfavorable.
Otras 2 evaluaciones económicas recientemente publicadas, realizadas con la perspectiva del sistema de salud americano y con los datos clínicos del estudio FOURIER, obtienen una RCEI que oscila entre 337.729 y 450.000 dólares/año de vida ajustado por calidad30,31.
La reducción de morbimortalidad no fue la esperada, por razones complejas y que caen en el terreno de la hipótesis28. El evento cardiovascular es multicausal, y los efectos de los fármacos son, a su vez, múltiples. Aunque epidemiológicamente se asocie una reducción del colesterol, la presión arterial o la glucemia con una reducción de morbimortalidad, esto puede no ser aplicable en la misma medida a todo mecanismo de acción o situación clínica32 (p. ej., en la diabetes, ya se comprobó con la metformina frente a las sulfonilureas)33. Por todo ello, comprobar los resultados en variables clínicas finales resulta imprescindible34. Situaciones clínicas que ya presentan importante daño y muy elevado riesgo, pero con cifras de cLDL no tan elevadas —como ocurre en los pacientes del FOURIER—, podrían ser menos sensibles a la modificación del factor lipídico que los pacientes con menos afección orgánica y una dislipemia más importante. Hay que tener en cuenta que una reducción porcentual de cLDL sobre la conseguida previamente no supondrá la misma reducción añadida de cLDL si se considera sobre el nivel basal inicial35. Entra dentro de lo posible que las expectativas de los expertos al establecer objetivos comunes de cLDL basados en datos epidemiológicos no se vean acompañadas para todos los fármacos y circunstancias por los efectos en variables clínicas finales.
A la luz de estos resultados, sería recomendable revisar considerablemente a la baja el precio de los inhibidores de la PCSK927,28,30,31,36. Eso permitiría mejorar la eficiencia y reducir el impacto presupuestario. En caso de mantenerse un precio muy alto, la selección de pacientes para el empleo de inhibidores de la PCSK9 es un punto clave36. Los criterios de financiación pública en España (emitidos antes de disponer de estudios de morbimortalidad) incluyen la presencia de cLDL > 100 mg/dl37,38. La Sociedad Española de Arterioesclerosis y organismos como el NICE (National Institute for Health and Care Excellence) británico39–42, consideraron valores de cLDL que pueden ser progresivamente más elevados para el inicio del tratamiento, dependiendo del riesgo atribuible a las distintas subpoblaciones. Sería recomendable realizar un análisis más detallado de los aspectos económicos y organizativos de la inclusión de esta tecnología, incluyendo un análisis de impacto presupuestario buscando la estrategia más eficiente.
En cualquier caso, sería posible asegurarse de obtener el mejor control lipídico posible43 antes de pasar al uso de estos fármacos, revisando la adherencia del paciente, empleando las estatinas de la manera más efectiva posible en cuanto a fármaco y dosis, mejorando las estrategias para favorecer su tolerabilidad y empleando las distintas opciones disponibles, incluida la ezetimiba. Una vez prescritos los inhibidores de la PCSK9, sería necesario realizar un seguimiento adecuado e investigar estrategias para adecuar la pauta utilizada44.
Atendiendo al análisis por subgrupos del estudio FOURIER3, la reducción de nuevos eventos cardiovasculares podría ser inferior en Europa (HR = 0,91; IC95%, 0,83-1,00) que en Norteamérica (HR = 0,77; IC95%, 0,66-0,90). Sería recomendable avanzar en el conocimiento de los factores relacionados con posibles diferencias de efecto, según comorbilidades y otros factores de riesgo, como la diabetes. Por último, cuando se publiquen los resultados del estudio ODYSSEY con alirocumab, se dispondrá de información adicional para avanzar en el conocimiento del beneficio cardiovascular aportado por los inhibidores de la PCSK94.
CONCLUSIONESEl presente estudio amplía la información disponible sobre la eficiencia del tratamiento con inhibidores de la PCSK9 y su utilidad y su proyección en el Sistema Nacional de Salud español. Los análisis realizados indican que el tratamiento con evolocumab no resulta coste-efectivo para pacientes con alto riesgo cardiovascular y cLDL > 100 mg/dl. Por todo ello, sería recomendable revisar considerablemente a la baja el precio de los inhibidores de la PCSK9.
CONFLICTO DE INTERESESNo se declara ninguno.
- –
Los ensayos pivotales con inhibidores de la PCSK9 mostraron una gran reducción del cLDL. Su precio, establecido antes de disponer de ensayos de morbimortalidad, es considerablemente mayor que el de otros fármacos empleados en prevención cardiovascular.
- –
Un ensayo clínico con evolocumab frente a placebo en prevención secundaria muestra que el 1.5% de los pacientes (el 9,8% frente al 11.3%) evitan 1 evento cardiovascular a 26 meses.
- –
En el Sistema Nacional de Salud y con el precio actual de evolocumab, la RCEI superó los 600.000 euros por evento cardiovascular evitado a los 6 meses.
- –
El impacto presupuestario de introducir evolocumab en prevención secundaria en España (año 2017) para pacientes con cLDL > 100 mg/dl podría oscilar entre 32 y 259 millones de euros.