La fuga paravalvular (FPV) es una complicación que se produce tras la cirugía de reemplazo valvular, con una incidencia de entre el 2 y el 10% en posición aórtica y entre el 7 y el 17% en posición mitral1. Aunque la mayoría de los casos tienen un curso benigno, entre el 1 y el 5% pueden tener consecuencias clínicas graves, como insuficiencia cardiaca o anemia hemolítica1,2. La mortalidad descrita tras la reintervención quirúrgica es alta (10-15%) y aumenta en relación con el número de operaciones previas2. El tratamiento percutáneo de la FPV ha surgido como una prometedora alternativa a la cirugía3, aun cuando los datos de comparación de los resultados entre corrección quirúrgica y percutánea son escasos. El objetivo del presente estudio es describir los resultados de las correcciones quirúrgica y percutánea de la FPV en una serie de pacientes contemporánea.
Se analizó a todos los pacientes tratados por una FPV aislada con un método quirúrgico o percutáneo en nuestro centro entre enero de 2006 y diciembre de 2015. La decisión de utilizar tratamiento percutáneo o quirúrgico se dejó al criterio del equipo médico encargado del tratamiento. Sin embargo, en 2012 se introdujo la corrección percutánea de la FPV, realizada por operadores experimentados. Desde entonces, todas las FPV en las que era técnicamente viable se abordaron con técnicas percutáneas tras el análisis del caso por el equipo cardiaco multidisciplinario. Para evitar sesgos, se excluyeron del análisis las medidas correctoras distintas de la corrección aislada de la FPV, como las intervenciones combinadas con revascularización coronaria o tratamiento adyuvante de otra válvula cardiaca. Se excluyó a los pacientes con endocarditis activa. Todos los pacientes dieron su consentimiento informado antes de la intervención.
A un total de 50 pacientes (32 con tratamiento percutáneo y 18 con tratamiento quirúrgico) se les practicó una corrección aislada de la FPV y, por lo tanto, se los incluyó en el estudio (tabla). Se alcanzó el éxito de la intervención en el 94 y el 87% de los pacientes quirúrgicos y percutáneos respectivamente. Los eventos adversos mayores y la mortalidad hospitalaria mostraron resultados comparables en los 2 grupos, y los pacientes tratados con corrección percutánea tuvieron una hospitalización más breve. Tras 1 año de seguimiento, no se observaron diferencias significativas entre los grupos por lo que respecta a la mortalidad por cualquier causa, los reingresos hospitalarios por síntomas de FPV y las reintervenciones (tabla).
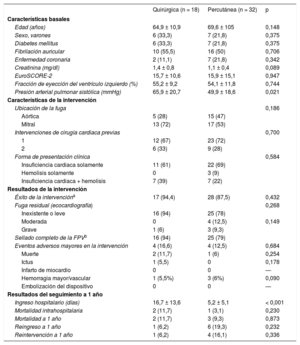
Resultados basales, de la intervención y clínicos de la reparación de la FPV percutánea en comparación con la quirúrgica
| Quirúrgica (n = 18) | Percutánea (n = 32) | p | |
|---|---|---|---|
| Características basales | |||
| Edad (años) | 64,9 ± 10,9 | 69,6 ± 105 | 0,148 |
| Sexo, varones | 6 (33,3) | 7 (21,8) | 0,375 |
| Diabetes mellitus | 6 (33,3) | 7 (21,8) | 0,375 |
| Fibrilación auricular | 10 (55,5) | 16 (50) | 0,706 |
| Enfermedad coronaria | 2 (11,1) | 7 (21,8) | 0,342 |
| Creatinina (mg/dl) | 1,4 ± 0,8 | 1,1 ± 0,4 | 0,089 |
| EuroSCORE-2 | 15,7 ± 10,6 | 15,9 ± 15,1 | 0,947 |
| Fracción de eyección del ventrículo izquierdo (%) | 55,2 ± 9,2 | 54,1 ± 11,8 | 0,744 |
| Presión arterial pulmonar sistólica (mmHg) | 65,9 ± 20,7 | 49,9 ± 18,6 | 0,021 |
| Características de la intervención | |||
| Ubicación de la fuga | 0,186 | ||
| Aórtica | 5 (28) | 15 (47) | |
| Mitral | 13 (72) | 17 (53) | |
| Intervenciones de cirugía cardiaca previas | 0,700 | ||
| 1 | 12 (67) | 23 (72) | |
| 2 | 6 (33) | 9 (28) | |
| Forma de presentación clínica | 0,584 | ||
| Insuficiencia cardiaca solamente | 11 (61) | 22 (69) | |
| Hemolisis solamente | 0 | 3 (9) | |
| Insuficiencia cardiaca + hemolisis | 7 (39) | 7 (22) | |
| Resultados de la intervención | |||
| Éxito de la intervencióna | 17 (94,4) | 28 (87,5) | 0,432 |
| Fuga residual (ecocardiografía) | 0,268 | ||
| Inexistente o leve | 16 (94) | 25 (78) | |
| Moderada | 0 | 4 (12,5) | 0,149 |
| Grave | 1 (6) | 3 (9,3) | |
| Sellado completo de la FPVb | 16 (94) | 25 (79) | |
| Eventos adversos mayores en la intervención | 4 (16,6) | 4 (12,5) | 0,684 |
| Muerte | 2 (11,7) | 1 (6) | 0,254 |
| Ictus | 1 (5,5) | 0 | 0,178 |
| Infarto de miocardio | 0 | 0 | — |
| Hemorragia mayor/vascular | 1 (5,5%) | 3 (6%) | 0,090 |
| Embolización del dispositivo | 0 | 0 | — |
| Resultados del seguimiento a 1 año | |||
| Ingreso hospitalario (días) | 16,7 ± 13,6 | 5,2 ± 5,1 | < 0,001 |
| Mortalidad intrahospitalaria | 2 (11,7) | 1 (3,1) | 0,230 |
| Mortalidad a 1 año | 2 (11,7) | 3 (9,3) | 0,873 |
| Reingreso a 1 año | 1 (6,2) | 6 (19,3) | 0,232 |
| Reintervención a 1 año | 1 (6,2) | 4 (16,1) | 0,336 |
FPV: fuga paravalvular.
Los principales resultados de este estudio son: a) tanto las técnicas de corrección de la FPV percutáneas como las quirúrgicas se asociaron con un alto porcentaje de éxito de la intervención (> 85%), con tendencia a un sellado más completo en los pacientes tratados quirúrgicamente; b) los eventos adversos mayores hospitalarios fueron comparables en los 2 grupos; c) los pacientes tratados con técnicas percutáneas tuvieron una hospitalización más breve, y d) en el seguimiento a 1 año, los resultados clínicos continuaron siendo comparables en los 2 grupos.
En nuestra serie, los pacientes quirúrgicos mostraron una tendencia a un sellado más completo de la FPV, pero el éxito de la intervención con las técnicas percutáneas fue, de todos modos, alto y similar al alcanzado con la cirugía. Estos resultados son coherentes con los de otras publicaciones previas que han descrito resultados similares tras la corrección percutánea de la FPV3. Aunque la mortalidad quirúrgica hospitalaria en esta serie podría considerarse alta (11%), refleja el alto riesgo quirúrgico de la población tratada y es coherente con lo indicado por series previas, con mortalidades de entre el 6 y el 22%1–3. Sin embargo, es importante resaltar que la reparación quirúrgica de la FPV podría ser la única alternativa terapéutica, en especial en los casos de FPV grande o múltiple. La comunicación dentro del equipo cardiaco y el examen conjunto de la complejidad técnica de la reparación percutánea, así como de la estrategia quirúrgica propuesta, son fundamentales en estos pacientes. De hecho, esta estrategia de comunicación tiende en general a ofrecer inicialmente la corrección percutánea cuando es técnicamente viable, teniendo en cuenta el carácter menos invasivo de la intervención. Tras el examen del equipo cardiaco, el fracaso de una corrección percutánea de la FPV no debe interpretarse, pues, como una «decisión errónea», sino más bien como la prueba de que está justificado el paso de una técnica menos invasiva a otra que lo es más. Además, las técnicas quirúrgicas pueden permitir la combinación con otras intervenciones correctoras además de la reparación de la FPV, que podrían suponer un mayor beneficio para el paciente. De hecho, en nuestra serie, se trató con cirugía mitral correctora a 3 pacientes con FPV mitral y fracaso de la reparación percutánea, y presentaron unos resultados clínicos excelentes. En los 3 casos, se informó con anterioridad a los pacientes y los cirujanos de la complejidad técnica de la reparación de la FPV, y la reparación quirúrgica se llevó a cabo durante el mismo ingreso hospitalario.
Otra observación relevante del estudio es la durabilidad de las correcciones percutánea y quirúrgica de la FPV, que se refleja en la incidencia relativamente baja de reintervenciones y reingresos hospitalarios a 1 año. Aunque el relativamente bajo número de pacientes es una limitación a este respecto, otras series parecen confirmar esta observación3.
En conclusión, nuestra serie indica que el tratamiento percutáneo de la FPV aislada sería una alternativa válida a la cirugía. No obstante, la corrección quirúrgica es una opción que siempre se debe tener en cuenta, ya que podría ser la única opción con resultado favorable para los pacientes con FPV no aptos para una reparación percutánea tras el fracaso de una intervención percutánea o para los que son necesarias otras intervenciones quirúrgicas adicionales. Serán necesarias series más amplias para confirmar estos resultados.
CONFLICTO DE INTERESESM. Hernández-Enríquez ha recibido becas de formación e investigación de la Sección de Hemodinámica y Cardiología Intervencionista de la Sociedad Española de Cardiología. X. Freixa es consultor de St. Jude Medical.