Los pacientes con fibrilación auricular a menudo presentan numerosas comorbilidades que conllevan un peor pronóstico. Diversos trabajos han estudiado las causas de muerte de estos pacientes, si bien los datos disponibles sobre pacientes en tratamiento con anticoagulantes orales directos (ACOD) de la práctica clínica habitual son escasos1. Dado que los pacientes que reciben estos agentes en nuestro medio suelen presentar un perfil clínico diferente que quienes reciben antagonistas de la vitamina K2,3, nos propusimos evaluar las causas y los predictores de muerte de los pacientes con fibrilación auricular no valvular (FANV) que iniciaron tratamiento con ACOD en 3 áreas de salud españolas. Para ello, entre enero de 2013 y diciembre de 2014 se incluyó consecutivamente a 973 pacientes con FANV a los que se prescribía por primera vez un ACOD. La selección de los pacientes se realizó mediante el sistema de información de prestación farmacéutica que contiene información de todas las recetas médicas de las áreas de salud evaluadas, debido a la obligatoriedad de la receta electrónica. Posteriormente se revisaron todas las historias clínicas informatizadas para comprobar la presencia de FANV. Se excluyó a los pacientes con indicación de anticoagulación temporal o diferente de la fibrilación auricular, los pacientes con miocardiopatía hipertrófica, estenosis mitral reumática moderada/grave, portadores de prótesis valvular mecánica o que ya habían tomado ACOD. Se siguió a los pacientes desde la fecha de la prescripción hasta una fecha común para todos. La variable principal de resultado fue la muerte, que se registró en el 99,8% de los casos. Inicialmente registraron las muertes los cardiólogos clínicos usando un formulario estandarizado que incluía una descripción estructurada de la fecha y el lugar de la muerte, circunstancias en las que aconteció, tratamientos aplicados, etc. La información se obtuvo a través de la revisión de historias clínicas electrónicas, certificados de defunción, informes de asistido por personal de urgencias extrahospitalarias y contacto telefónico con los familiares en caso de defunción. Para identificar los factores asociados a la mortalidad, se realizaron análisis de regresión de Cox multivariable, con los que se calcularon las razones de riesgos. Para los análisis estadísticos se emplearon los programas SPSS v21 y STATA v13. El presente estudio ha sido aprobado por el comité ético de los centros participantes.
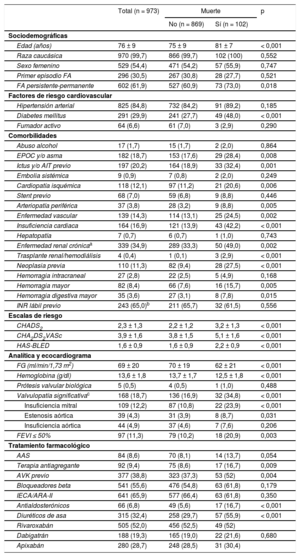
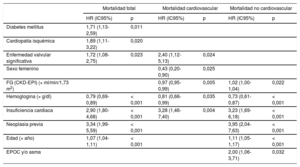
Las características de los pacientes se resumen en la tabla 1. Durante una media de seguimiento de 646 (intervalo, 470-839) días, se registraron 102 muertes (5,85/100 personas-año), de las cuales 34 fueron cardiovasculares (1,95/100 personas-año); 55, no cardiovasculares (3,16/100 personas-año), y 13, de causa indeterminada (0,74/100 personas-año). La muestra la incidencia y las causas de muerte en la población de estudio; las neoplasias (1,20/100 personas-año), las infecciones (0,92/100 personas-año) y la insuficiencia cardiaca (0,80/100 personas-año) fueron las causas más frecuentes. Los pacientes que fallecieron tenían más edad y comorbilidades y mayores puntuaciones de las escalas de riesgo tromboembólico y hemorrágico (tabla 1). Los predictores de mortalidad total, cardiovascular y no cardiovascular se muestran en la tabla 2. El estadístico C del modelo para la mortalidad total fue 0,82 (intervalo de confianza del 95% [IC95%], 0,77-0,87; p < 0,001), mientras que para la mortalidad cardiovascular fue 0,81 (IC95%, 0,73-0,89; p < 0,001) y para la no cardiovascular, 0,81 (IC95%, 0,74-0,87; p < 0,001) (test de Hosmer-Lemeshow, p > 0,05 en los 3 modelos). Durante el seguimiento, la mortalidad fue similar con independencia del tipo de anticoagulante y la causa de muerte ().
Características basales de la población en función de la muerte
| Total (n = 973) | Muerte | p | ||
|---|---|---|---|---|
| No (n = 869) | Sí (n = 102) | |||
| Sociodemográficas | ||||
| Edad (años) | 76 ± 9 | 75 ± 9 | 81 ± 7 | < 0,001 |
| Raza caucásica | 970 (99,7) | 866 (99,7) | 102 (100) | 0,552 |
| Sexo femenino | 529 (54,4) | 471 (54,2) | 57 (55,9) | 0,747 |
| Primer episodio FA | 296 (30,5) | 267 (30,8) | 28 (27,7) | 0,521 |
| FA persistente-permanente | 602 (61,9) | 527 (60,9) | 73 (73,0) | 0,018 |
| Factores de riesgo cardiovascular | ||||
| Hipertensión arterial | 825 (84,8) | 732 (84,2) | 91 (89,2) | 0,185 |
| Diabetes mellitus | 291 (29,9) | 241 (27,7) | 49 (48,0) | < 0,001 |
| Fumador activo | 64 (6,6) | 61 (7,0) | 3 (2,9) | 0,290 |
| Comorbilidades | ||||
| Abuso alcohol | 17 (1,7) | 15 (1,7) | 2 (2,0) | 0,864 |
| EPOC y/o asma | 182 (18,7) | 153 (17,6) | 29 (28,4) | 0,008 |
| Ictus y/o AIT previo | 197 (20,2) | 164 (18,9) | 33 (32,4) | 0,001 |
| Embolia sistémica | 9 (0,9) | 7 (0,8) | 2 (2,0) | 0,249 |
| Cardiopatía isquémica | 118 (12,1) | 97 (11,2) | 21 (20,6) | 0,006 |
| Stent previo | 68 (7,0) | 59 (6,8) | 9 (8,8) | 0,446 |
| Arteriopatía periférica | 37 (3,8) | 28 (3,2) | 9 (8,8) | 0,005 |
| Enfermedad vascular | 139 (14,3) | 114 (13,1) | 25 (24,5) | 0,002 |
| Insuficiencia cardiaca | 164 (16,9) | 121 (13,9) | 43 (42,2) | < 0,001 |
| Hepatopatía | 7 (0,7) | 6 (0,7) | 1 (1,0) | 0,743 |
| Enfermedad renal crónicaa | 339 (34,9) | 289 (33,3) | 50 (49,0) | 0,002 |
| Trasplante renal/hemodiálisis | 4 (0,4) | 1 (0,1) | 3 (2,9) | < 0,001 |
| Neoplasia previa | 110 (11,3) | 82 (9,4) | 28 (27,5) | < 0,001 |
| Hemorragia intracraneal | 27 (2,8) | 22 (2,5) | 5 (4,9) | 0,168 |
| Hemorragia mayor | 82 (8,4) | 66 (7,6) | 16 (15,7) | 0,005 |
| Hemorragia digestiva mayor | 35 (3,6) | 27 (3,1) | 8 (7,8) | 0,015 |
| INR lábil previo | 243 (65,0)b | 211 (65,7) | 32 (61,5) | 0,556 |
| Escalas de riesgo | ||||
| CHADS2 | 2,3 ± 1,3 | 2,2 ± 1,2 | 3,2 ± 1,3 | < 0,001 |
| CHA2DS2VASc | 3,9 ± 1,6 | 3,8 ± 1,5 | 5,1 ± 1,6 | < 0,001 |
| HAS-BLED | 1,6 ± 0,9 | 1,6 ± 0,9 | 2,2 ± 0,9 | < 0,001 |
| Analítica y ecocardiograma | ||||
| FG (ml/min/1,73 m2) | 69 ± 20 | 70 ± 19 | 62 ± 21 | < 0,001 |
| Hemoglobina (g/dl) | 13,6 ± 1,8 | 13,7 ± 1,7 | 12,5 ± 1,8 | < 0,001 |
| Prótesis valvular biológica | 5 (0,5) | 4 (0,5) | 1 (1,0) | 0,488 |
| Valvulopatía significativac | 168 (18,7) | 136 (16,9) | 32 (34,8) | < 0,001 |
| Insuficiencia mitral | 109 (12,2) | 87 (10,8) | 22 (23,9) | < 0,001 |
| Estenosis aórtica | 39 (4,3) | 31 (3,9) | 8 (8,7) | 0,031 |
| Insuficiencia aórtica | 44 (4,9) | 37 (4,6) | 7 (7,6) | 0,206 |
| FEVI ≤ 50% | 97 (11,3) | 79 (10,2) | 18 (20,9) | 0,003 |
| Tratamiento farmacológico | ||||
| AAS | 84 (8,6) | 70 (8,1) | 14 (13,7) | 0,054 |
| Terapia antiagregante | 92 (9,4) | 75 (8,6) | 17 (16,7) | 0,009 |
| AVK previo | 377 (38,8) | 323 (37,3) | 53 (52) | 0,004 |
| Bloqueadores beta | 541 (55,6) | 476 (54,8) | 63 (61,8) | 0,179 |
| IECA/ARA-II | 641 (65,9) | 577 (66,4) | 63 (61,8) | 0,350 |
| Antialdosterónicos | 66 (6,8) | 49 (5,6) | 17 (16,7) | < 0,001 |
| Diuréticos de asa | 315 (32,4) | 258 (29,7) | 57 (55,9) | < 0,001 |
| Rivaroxabán | 505 (52,0) | 456 (52,5) | 49 (52) | |
| Dabigatrán | 188 (19,3) | 165 (19,0) | 22 (21,6) | 0,680 |
| Apixabán | 280 (28,7) | 248 (28,5) | 31 (30,4) | |
AAS: ácido acetilsalicílico; AIT: accidente isquémico transitorio; ARA-II: antagonista del receptor de la angiotensina II; AVK: antagonista de la vitamina K; CHADS2: insuficiencia cardiaca, hipertensión, edad > 75 años, diabetes mellitus e ictus (doble); CHA2DS2VASc: insuficiencia cardiaca, hipertensión, edad ≥ 75 años [doble], diabetes mellitus, ictus (doble); CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; FG: filtrado glomerular; HAS-BLED: hipertensión, función renal/hepática anormal, ictus, antecedentes de hemorragia o predisposición a ella, labilidad de la INR, edad > 65 años y toma concomitante de fármacos o alcohol; IECA: inhibidor de la enzima de conversión de la angiotensina; INR: razón internacional normalizada.
Los datos expresados media ± desviación estándar o n (%).
Análisis multivariable de riesgos proporcionales de Cox para la predicción de muerte total, cardiovascular y no cardiovascular
| Mortalidad total | Mortalidad cardiovascular | Mortalidad no cardiovascular | ||||
|---|---|---|---|---|---|---|
| HR (IC95%) | p | HR (IC95%) | p | HR (IC95%) | p | |
| Diabetes mellitus | 1,71 (1,13-2,59) | 0,011 | ||||
| Cardiopatía isquémica | 1,89 (1,11-3,22) | 0,020 | ||||
| Enfermedad valvular significativa | 1,72 (1,08-2,75) | 0,023 | 2,40 (1,12-5,13) | 0,024 | ||
| Sexo femenino | 0,43 (0,20-0,90) | 0,025 | ||||
| FG (CKD-EPI) (× ml/min/1,73 m2) | 0,97 (0,95-0,99) | 0,005 | 1,02 (1,00-1,04) | 0,022 | ||
| Hemoglogina (× g/dl) | 0,79 (0,69-0,89) | < 0,001 | 0,81 (0,66-0,99) | 0,035 | 0,73 (0,61-0,87) | < 0,001 |
| Insuficiencia cardiaca | 2,90 (1,80-4,68) | < 0,001 | 3,28 (1,46-7,40) | 0,004 | 3,23 (1,69-6,18) | < 0,001 |
| Neoplasia previa | 3,34 (1,99-5,59) | < 0,001 | 3,95 (2,04-7,63) | < 0,001 | ||
| Edad (× año) | 1,07 (1,04-1,11) | < 0,001 | 1,11 (1,05-1,17) | < 0,001 | ||
| EPOC y/o asma | 2,00 (1,06-3,71) | 0,032 | ||||
AIT: accidente isquémico transitorio; CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; EPOC: enfermedad pulmonar obstructiva crónica; FG: filtrado glomerular; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Modelos multivariables ajustados por edad, sexo, fibrilación auricular persistente-permanente, diabetes mellitus, EPOC y/o asma, ictus y/o AIT previo, cardiopatía isquémica, arteriopatía periférica, insuficiencia cardiaca, neoplasia, hemorragia mayor previa, FG estimado según CKD-EPI, hemoglobina, enfermedad valvular significativa, fracción de eyección del ventrículo izquierdo y anticoagulante oral directo recibido.
En este trabajo se evaluaron por primera vez las causas de muerte en una cohorte contemporánea y multicéntrica de pacientes con FANV que inician tratamiento con ACOD. Nuestro trabajo muestra una elevada mortalidad en este tipo de pacientes, y las causas más frecuentes fueron las neoplasias, las infecciones y la insuficiencia cardiaca, mientras que las muertes por eventos embólicos y/o hemorrágicos fueron poco frecuentes. A diferencia de nuestro estudio, la principal causa de muerte en los ensayos clínicos pivotales ha sido el origen cardiovascular1–3, lo cual puede reflejar las diferencias existentes entre el perfil clínico de los pacientes incluidos en los ensayos clínicos y los que reciben ACOD en nuestra práctica clínica diaria. Por ello consideramos relevante describir las causas de mortalidad y la identificación de los predictores específicos de muerte en estos pacientes, con el fin de mejorar la planificación de estrategias encaminadas a aumentar su supervivencia. Tal y como se ha mostrado anteriormente, en este estudio se identificaron como predictores, por un lado, «marcadores de riesgo» como la edad y el sexo y, por otro, «factores de riesgo modificables» como diabetes mellitus, cardiopatía isquémica, insuficiencia cardiaca, neoplasias, insuficiencia renal, anemia, enfermedad pulmonar obstructiva crónica y valvulopatías, contra los que se puede actuar desde un punto de vista preventivo y terapéutico. Por lo tanto, la mejora del control de los factores de riesgo cardiovascular y el adecuado cumplimiento de las recomendaciones de las guías de práctica clínica sobre el manejo de las comorbilidades asociadas a la fibrilación auricular deben ser el objetivo primordial4. Por último, debemos reconocer que el diseño retrospectivo y la ausencia de un grupo de control son las principales limitaciones de este trabajo, pues impiden saber con certeza si la elevada mortalidad observada ocurre en todos los pacientes con FANV independientemente del anticoagulante prescrito o el tratamiento con ACOD selecciona de algún modo a los pacientes con más alto riesgo.