Los sistemas de atención urgente del infarto se han creado para mejorar su tratamiento y la revascularización, pero pueden mejorar el manejo de todos los pacientes con síndrome coronario agudo.
MétodosEstudio comparativo de todos los pacientes ingresados por síndrome coronario agudo antes y tras la implantación de un código infarto.
ResultadosSe incluyó a 1.210 pacientes, y aunque la media de edad fue igual en ambos periodos, los pacientes ingresados tras la implantación del código infarto presentaron menor prevalencia de diabetes mellitus e hipertensión pero más tabaquismo activo y mayor GRACE. Se observó un incremento significativo en el porcentaje de pacientes ingresados por síndrome coronario agudo con elevación del segmento ST (29,8-39,5%) y de revascularizaciones coronarias (82,1-90,1%), así como la generalización de la angioplastia primaria (51,9-94,9%), además de una reducción en el tiempo hasta el cateterismo e incremento de la revascularización precoz. La estancia hospitalaria media fue significativamente más corta tras la implantación del código infarto. No se observaron diferencias en la mortalidad hospitalaria, salvo entre los pacientes de alto riesgo (38,8-22,4%). Tras el alta no se observan diferencias entre ambos periodos en mortalidad cardiovascular, mortalidad por cualquier causa, reinfarto o complicaciones cardiovasculares mayores.
ConclusionesLa implantación del código infarto conllevó un incremento de pacientes ingresados por síndrome coronario agudo con elevación del segmento ST y mayor GRACE. Se redujo la estancia hospitalaria, se generalizó la angioplastia primaria y se redujo la mortalidad hospitalaria de los pacientes de alto riesgo. El pronóstico tras el alta fue igual en ambos periodos.
Palabras clave
La revascularización coronaria percutánea es la base del tratamiento del síndrome coronario agudo (SCA)1, especialmente para el SCA con elevación del segmento ST (SCACEST)2. La generalización de la revascularización coronaria ha llevado a la creación de más unidades de hemodinámica y, además, sistemas locales y/o regionales de atención urgente del SCACEST3. Se ha demostrado que estas iniciativas mejoran las tasas y los tiempos de reperfusión4–11. La mayoría de las publicaciones que han analizado los resultados de algún código infarto se han centrado únicamente en los pacientes con SCACEST4–7,9,11 aunque esto supone menos del 35% del total de los pacientes que presentan un SCA12,13.
La incidencia de SCACEST ha ido en decremento en la última década, mientras que se ha mantenido constante o incluso ha aumentado la del SCA sin elevación del segmento ST (SCASEST)12,14,15. Aunque la estrategia invasiva se ha demostrado superior al tratamiento conservador en el SCASEST16,17, el porcentaje de revascularización suele ser menor que en el SCACEST, aparte de que los pacientes suelen presentar un perfil clínico y hemodinámico bastante diferente12. La creación e implantación de un programa de código infarto solo regula la actividad urgente, casi siempre en relación únicamente con el SCACEST, pero es fácil inferir que el cumplimiento de un protocolo estandarizado y unificado entre diferentes servicios y centros puede llevar a una mejora general del tratamiento de los pacientes con SCACEST y también con SCASEST13,18,19; sin embargo, esto no se ha analizado hasta el momento, y toda la evidencia disponible está relacionada con el SCACEST. El objetivo de este estudio es describir el cambio en el perfil clínico, el tratamiento y el pronóstico de los pacientes admitidos por cualquier tipo de SCA en un hospital secundario, dotado de unidad de hemodinámica, tras la implantación en el centro de un código infarto regional.
MÉTODOSEstudio observacional de todos los pacientes ingresados por SCA en el Hospital Universitario de San Juan, en Alicante, en dos periodos concretos: los 2 años previos y el primer año tras la implantación del código infarto. El registro de pacientes con SCA y el consentimiento informado los aprobó el comité ético del hospital. Se definió SCA como la elevación de enzimas marcadoras de daño miocárdico por encima del límite de normalidad del laboratorio del centro (troponina I ≥ 0,04ng/dl o troponina ultrasensible > 0,056ng/dl) y/o alteraciones en el electrocardiograma indicativas de lesión o isquemia miocárdica acompañando al dolor torácico compatible1. Se categorizó a los pacientes en función de la escala GRACE (Global Registry of Acute Coronary Events) en bajo riesgo (< 108), riesgo intermedio (109-140) y alto riesgo (> 140)20.
Durante el ingreso se registraron los diagnósticos, antecedentes, factores de riesgo cardiovascular, tratamientos, exploraciones complementarias y complicaciones hospitalarias. El filtrado glomerular se estimó a partir de los valores séricos de creatinina mediante la euación Modification of Diet in Renal Disease Study21. De acuerdo con la clasificación de la guía americana de dislipemia de 201322, se consideró tratamiento intensivo con estatinas las dosis de 40–80mg/día de atorvastatina y 20–40mg/día de rosuvastatina. El análisis conjunto de las comorbilidades se realizó mediante el índice de Charlson adaptado a pacientes con cardiopatía isquémica23.
Se realizó seguimiento del primer año tras el alta de los pacientes mediante la revisión de las historias clínicas, su historial clínico informatizado (tanto de atención primaria como de consultas al servicio de urgencias) y por teléfono. El objetivo primario pronóstico durante el seguimiento fue la mortalidad por causa cardiovascular y los secundarios fueron la mortalidad por cualquier causa, el reinfarto y la incidencia de complicaciones cardiovasculares mayores (reinfarto, revascularización urgente no programada, reingreso por insuficiencia cardiaca o accidente cerebrovascular).
Análisis estadísticoEl análisis se llevó a cabo con el programa IBM SPSS 22.0 para Mac. Las variables cualitativas se evaluaron mediante la prueba de la χ2 y el test de Fisher cuando fue preciso; las variables cuantitativas se compararon mediante prueba de la t de Student y ANOVA. La identificación de los factores asociados a la mortalidad hospitalaria se llevó a cabo mediante regresión logística y en el modelo se incluyeron los factores de riesgo, los antecedentes de enfermedad cardiovascular, los tratamientos recibidos durante el ingreso y la revascularización. Se analizó la calibración del modelo de regresión logística mediante el método de Hosmer-Lemeshow y capacidad diagnóstica mediante el área bajo la curva ROC de la probabilidad estimada por el modelo. El análisis de la supervivencia se realizó mediante regresión de riesgos proporcionales de Cox, con el método de inclusión por pasos hacia delante, en el que se incluyeron edad, sexo, todos los factores de riesgo, cualquier enfermedad cardiovascular ya presente, los tratamientos al alta y la revascularización coronaria. Se atribuyó significación estadística a valores de p<0,05.
RESULTADOSEn el periodo de estudio se incluyó a 1.210 pacientes con diagnóstico de SCA. Como se muestra en la tabla 1, se observaron diferencias en los antecedentes clínicos de los pacientes en cada periodo, de tal forma que, aunque la media de edad fue igual en ambos periodos, los pacientes ingresados tras la implantación del código infarto presentaron menor prevalencia de diabetes mellitus e hipertensión, pero más tabaquismo activo; además, presentaron en general menos comorbilidades, lo que se refleja en un índice de Charlson inferior. Se observó un incremento en el porcentaje de pacientes ingresados por SCACEST y también en la puntuación GRACE media tras la implantación del código infarto. Globalmente se observó un incremento significativo en la revascularización coronaria percutánea y la práctica generalización de la angioplastia coronaria transluminal percutánea primaria en el SCACEST. En el periodo previo, el 21,3% de los pacientes con SCACEST fueron tratados con trombolisis y angioplastia coronaria transluminal percutánea precoz, pero se abandonó completamente esta estrategia tras la implantación del código infarto. Además, también se observó un incremento en la utilización de inhibidores de la glucoproteína IIb/IIIa, balón de contrapulsación y tromboaspiración para los pacientes atendidos tras la implantación del código infarto.
Características generales y procedimientos de los pacientes antes y después de la implantación del código infarto
| Antes | Después | p* | |
|---|---|---|---|
| Pacientes | 866 (71,6) | 344 (28,4) | |
| Estancia (días) | 6,4±5,8 | 5,6±5,1 | 0,03 |
| Varones (%) | 75,1 | 75,1 | 0,20 |
| Edad (años) | 68,94±12,6 | 67,8±13,3 | 0,16 |
| Diabetes mellitus (%) | 38,9 | 29,1 | < 0,01 |
| Estancia en UCI (%) | 46,2 | 50,3 | 0,20 |
| Días en UCI | 1,4±2,1 | 1,2±1,8 | 0,14 |
| Días en UCI, pacientes con SCACEST | 2,5±2,5 | 2,0±2,2 | 0,04 |
| Días en UCI, pacientes con SCASEST | 0,9±1,6 | 0,8±1,2 | 0,13 |
| Hipertensión arterial (%) | 71,1 | 63,1 | < 0,01 |
| Fumadores (%) | 28,4 | 35,5 | 0,02 |
| Dislipemia (%) | 52,5 | 48,3 | 0,18 |
| CI previa (%) | 34,3 | 20,1 | < 0,01 |
| IC previa (%) | 4,3 | 1,7 | 0,03 |
| ACV previo (%) | 6,2 | 7,0 | 0,64 |
| Índice de Charlson | 3,0±2,0 | 2,7±2,2 | 0,04 |
| Índice de Charlson > 4 (%) | 32,7 | 25,3 | 0,02 |
| FG (ml/min/1,72 m2) | 74,9±25,7 | 76,5±26,2 | 0,38 |
| FG<60 ml/min (%) | 26,3 | 25,5 | 0,70 |
| SCACEST (%) | 29,8 | 39,5 | < 0,01 |
| Puntuación GRACE | 130,2±36,6 | 140,1±40,1 | < 0,01 |
| Puntuación GRACE>140 (%) | 6,3 | 15,4 | < 0,01 |
| Clase Killip ≥ 3 (%) | 6,3 | 11,3 | < 0,01 |
| Revascularización percutánea (%) | 82,1 | 90,1 | < 0,01 |
| Revascularización quirúrgica (%) | 2,8 | 1,5 | 0,20 |
| ACTPp en SCACEST (%) | 51,9 | 94,9 | < 0,01 |
| Tromboaspiración en SCACEST (%) | 11,0 | 42,6 | < 0,01 |
| Anti-GPIIb/IIIa en cateterismo (%) | 2,2 | 15,5 | < 0,01 |
| Balón de contrapulsación (%) | 1,0 | 3,5 | 0,02 |
ACTPp: angioplastia coronaria transluminal percutánea primaria; ACV: accidente cerebrovascular; CI: cardiopatía isquémica; FG: filtrado glomerular; GPIIb/IIIa: glucoproteína IIb/IIIa; GRACE: Global Registry of Acute Coronary Events; IC: insuficiencia cardiaca; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST; UCI: unidad de cuidados intensivos.
Salvo otra indicación, los datos expresan n (%) o media±desviación estándar.
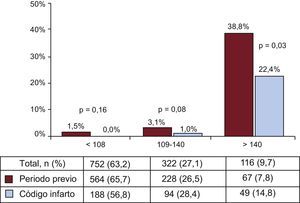
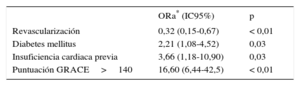
Tras la implantación, se observó una reducción en el tiempo hasta el cateterismo (de 1,8±2,5 a 1,0±1,7; p<0,01), lo cual llevó a aumento de los pacientes revascularizados antes de las 48 h, del 65,4 al 78,6% (p<0,01); estos cambios se debieron especialmente a los pacientes ingresados con SCACEST, ya que no se observaron cambios en el tiempo ni en la tasa de revascularización de los pacientes con SCASEST. La estancia hospitalaria media fue significativamente más corta tras la implantación del código infarto, debida especialmente al acortamiento observado en los pacientes con SCACEST (7,0±5,1 frente a 5,9±4,5 días; p=0,03); aunque la tasa general de ingresos en la unidad de cuidados intensivos fue similar en ambos periodos, se observó un acortamiento de la estancia en dicha unidad de los pacientes que ingresaron con SCACEST tras la implantación del código infarto. No se observaron diferencias en la mortalidad total hospitalaria entre ambos periodos (el 4,9 frente al 3,8%; p=0,42), pero sí una tendencia a menor mortalidad entre los pacientes ingresados por SCASEST tras la implantación (el 3,9 frente al 1,1%; p=0,05); la mortalidad hospitalaria de los pacientes con SCACEST fue similar en ambos periodos (el 7,4 frente al 8,1%; p=0,80). Cuando se analizó a los pacientes por categorías de la escala GRACE, sí que se observó una reducción de la mortalidad hospitalaria de los pacientes de alto riesgo (figura 1). Como se muestra en la tabla 2, la diabetes mellitus, el antecedente de insuficiencia cardiaca y puntuación GRACE de alto riesgo fueron las variables independientes asociadas a la mortalidad hospitalaria, mientras que la revascularización coronaria se asoció negativamente.
Variables asociadas a la mortalidad hospitalaria
| ORa* (IC95%) | p | |
|---|---|---|
| Revascularización | 0,32 (0,15-0,67) | < 0,01 |
| Diabetes mellitus | 2,21 (1,08-4,52) | 0,03 |
| Insuficiencia cardiaca previa | 3,66 (1,18-10,90) | 0,03 |
| Puntuación GRACE>140 | 16,60 (6,44-42,5) | < 0,01 |
GRACE: Global Registry of Acute Coronary Events; IC95%: intervalo de confianza del 95%; ORa: odds ratio ajustada.
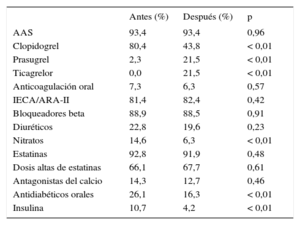
En la tabla 3 se presentan los cambios en los fármacos recomendados en el momento del alta en cada periodo, y se puede observar diferencias significativas, especialmente en el descenso de clopidogrel y el ascenso de los nuevos antiagregantes.
Tratamientos al alta de los pacientes antes y después de la implantación del código infarto
| Antes (%) | Después (%) | p | |
|---|---|---|---|
| AAS | 93,4 | 93,4 | 0,96 |
| Clopidogrel | 80,4 | 43,8 | < 0,01 |
| Prasugrel | 2,3 | 21,5 | < 0,01 |
| Ticagrelor | 0,0 | 21,5 | < 0,01 |
| Anticoagulación oral | 7,3 | 6,3 | 0,57 |
| IECA/ARA-II | 81,4 | 82,4 | 0,42 |
| Bloqueadores beta | 88,9 | 88,5 | 0,91 |
| Diuréticos | 22,8 | 19,6 | 0,23 |
| Nitratos | 14,6 | 6,3 | < 0,01 |
| Estatinas | 92,8 | 91,9 | 0,48 |
| Dosis altas de estatinas | 66,1 | 67,7 | 0,61 |
| Antagonistas del calcio | 14,3 | 12,7 | 0,46 |
| Antidiabéticos orales | 26,1 | 16,3 | < 0,01 |
| Insulina | 10,7 | 4,2 | < 0,01 |
AAS: ácido acetilsalicílico; ARA-II: antagonistas de los receptores de la angiotensina II; IECA: inhibidores de la enzima de conversión de la angiotensina.
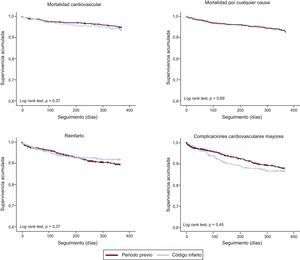
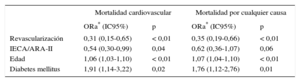
Se consiguió dar seguimiento durante el primer año al 93,1% de los pacientes dados de alta en cada periodo, con una mediana de seguimiento de 370 [intervalo intercuartílico, 359-382] días, que fue igual en ambos periodos. Entre los 1.154 pacientes dados de alta, se registraron 82 (7,1%) fallecimientos, de los cuales 61 (5,3%) fueron de causa cardiovascular. Como se muestra en la figura 2, no se observaron diferencias en la mortalidad cardiovascular (el 5,0 frente al 6,0%), la mortalidad por cualquier causa (el 7,3 frente al 6,6%), los reinfartos (el 9,3 frente al 7,0%) o las complicaciones cardiovasculares mayores (el 10,9 frente al 11,7%) en la comparación del periodo previo frente al del código infarto. En el análisis multivariable no se encontró ninguna asociación entre la mortalidad en el seguimiento y la implantación del código infarto (tabla 4); sí que se observó asociación entre revascularización y menor mortalidad.
Variables asociadas a la mortalidad cardiovascular o por cualquier causa durante el seguimiento
| Mortalidad cardiovascular | Mortalidad por cualquier causa | |||
|---|---|---|---|---|
| ORa* (IC95%) | p | ORa* (IC95%) | p | |
| Revascularización | 0,31 (0,15-0,65) | < 0,01 | 0,35 (0,19-0,66) | < 0,01 |
| IECA/ARA-II | 0,54 (0,30-0,99) | 0,04 | 0,62 (0,36-1,07) | 0,06 |
| Edad | 1,06 (1,03-1,10) | < 0,01 | 1,07 (1,04-1,10) | < 0,01 |
| Diabetes mellitus | 1,91 (1,14-3,22) | 0,02 | 1,76 (1,12-2,76) | 0,01 |
ARA-II: antagonistas de los receptores de la angiotensina II; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina; ORa: odds ratio ajustada.
La instauración del código infarto en el centró conllevó cambios en el perfil clínico global de los pacientes ingresados por SCA, con un incremento de la puntuación GRACE media además del aumento de pacientes ingresados con SCACEST, y un aumento general en el empleo de la revascularización. Aunque no se observaron diferencias en la mortalidad en el primer año tras el alta, sí que se observó menor mortalidad hospitalaria de los pacientes de alto riesgo y, llamativamente, los pacientes con SCASEST tras la implantación del código infarto. Por otra parte, se redujo la estancia hospitalaria 1 día pese a la mayor gravedad de los pacientes ingresados en el segundo periodo. La mayoría de las publicaciones que han analizado el impacto de la implantación de algún código infarto se han centrado únicamente en los pacientes con SCACEST4–7,9,11, pero dado que esto supone menos del 35%12,13 del total de los pacientes que presentan un SCA, los autores consideran que el análisis realizado en este estudio es más global y representativo de la práctica clínica diaria mediante la comparación de todos los pacientes ingresados por SCA en el primer año tras la implantación del código infarto respecto a los que habían ingresado en los 2 años previos. Además, dado que las características generales, la puntuación GRACE y la incidencia de complicaciones de los pacientes incluidos fue similar a la de otros registros4–13,18, se piensa que los resultados obtenidos pueden ser representativos de la práctica clínica real y, además, se alinean con las recomendaciones de la Sociedad Europea de Cardiología de que la creación de un nuevo plan asistencial del infarto debe acompañarse de un registro prospectivo que evalúe sus resultados3.
La consecuencia más inmediata para un centro con unidad de hemodinámica de la implantación del código infarto es la generalización de la angioplastia primaria como estrategia de reperfusión en el SCACEST. Este hecho explicaría, además, el mayor empleo de la revascularización observado en el segundo periodo en los pacientes con SCA. El aumento en el porcentaje de pacientes ingresados con diagnóstico de SCACEST puede deberse a distintos motivos. Si bien no es descartable una mayor incidencia de este tipo de SCA, el cese del traslado de pacientes con indicación de angioplastia primaria al antiguo hospital de referencia con guardia de hemodinámica de 24 h, parece la explicación más lógica, a pesar de que la mayoría de estos pacientes, salvo en la minoría de casos en que la situación clínica no lo permitía, retornaban al centro; otro motivo puede haber sido una mayor sensibilidad diagnóstica. La instauración del plan se ha acompañado de una intensa campaña de formación y recordatorio de criterios diagnósticos y terapéuticos con los distintos servicios implicados, siguiendo las recomendaciones de la Sociedad Europea de Cardiología3. Diagnósticos previos dudosos, en presencia de electrocardiogramas no concluyentes como bloqueo de rama izquierda, ritmo de marcapasos, clínicas atípicas o paradas extrahospitalarias, se reconocieron en el segundo periodo como SCACEST y se dio el tratamiento y el diagnóstico adecuados. En este sistema, el hemodinamista de alerta ha servido frecuentemente como «consultor» de casos dudosos y ha contribuido a mejorar la precisión diagnóstica en estos casos. En el análisis del impacto de la implantación del código infarto en el área metropolitana sur de Barcelona, por el contrario, se observó un perfil de menor riesgo en los pacientes tras la puesta en marcha del plan local. A diferencia del presente estudio, el trabajo de Gómez-Hospital et al6 incluyó únicamente a pacientes remitidos para angioplastia primaria o de rescate. Sus resultados reflejan, posiblemente, que en la fase previa solo se incluía para reperfusión mecánica a los pacientes más graves y con criterios más restrictivos, como los que presentaban contraindicaciones para la trombolisis6. Más recientemente, el registro DICOCLES12 mostró que casi el 20% de los pacientes con SCACEST no reciben ningún tratamiento de reperfusión, que es mediante angioplastia primaria solo para dos tercios de los reperfundidos. En el presente estudio, pacientes de mayor gravedad, y quizá de más difícil diagnóstico, se identificaron correctamente como SCACEST y se incluyeron en el programa. La reperfusión mecánica inmediata contribuye a un diagnóstico precoz de la enfermedad multivaso, una disminución de las complicaciones hospitalarias y un manejo más eficaz de estos pacientes24.
El traslado urgente a unidades de hemodinámica para revascularización del SCACEST se ha demostrado seguro y eficaz4,5,11, lo que ha llevado a la generalización de los sistemas locales y/o regionales de atención al SCACEST, los denominados código infarto, pero que también pueden conllevar demoras relevantes en la atención de los pacientes5,9. Los resultados de estos sistemas de atención han demostrado que mejoran los tiempos6,7,11 y las tasas globales de reperfusión4,7,9; sin embargo, casi ningún programa ha sido capaz de demostrar reducciones significativas en la mortalidad4–7,9. En el registro DICOCLES12, el 74% de los pacientes con SCACEST llegaron al hospital mediante ambulancia, mientras que en el caso del SCASEST fueron el 55,4%. Los resultados coinciden globalmente en este dato y muestran, además, reducciones en la mortalidad hospitalaria de los pacientes de más alto riesgo. Por último, la estrategia farmacoinvasiva, no considerada una primera opción actualmente, dejó de utilizarse en el centro, aunque esta opción ha demostrado ser bastante similar a la angioplastia primaria en en cuanto a repercusión en el ventrículo izquierdo y mortalidad25.
La mortalidad en el primer año tras el alta fue igual en ambos periodos. Este hallazgo podría parecer desalentador para el esfuerzo que representa la instauración y el mantenimiento de un programa de código infarto, aunque teniendo en cuenta que los pacientes del segundo periodo presentaban una puntuación GRACE media más elevada y mayor porcentaje de SCACEST, el mero hecho de que no presentaran mayor mortalidad ya podría ser positivo. De hecho, la tasa de mortalidad bruta fue ligeramente superior entre los pacientes del periodo con código infarto, aunque la diferencia no fuera estadísticamente significativa. Estos hallazgos coinciden plenamente con lo publicado por otros registros nacionales7 e internacionales8,10. Para explicar este hallazgo se ha argumentado la inclusión de pacientes cada vez más complejos, situaciones más críticas, como la parada cardiaca extrahospitalaria reanimada, o los pacientes con mayores tiempos de demora que no se habrían incluido en los primeros programas de atención urgente del SCACEST10. En el análisis de los resultados de la implantación del código infarto en el área metropolitana de Barcelona sí se observó al año una reducción en la mortalidad y las complicaciones cardiovasculares mayores6. Pero como se ha dicho, este estudio incluye solo a pacientes tratados con reperfusión percutánea, por lo que, a diferencia del presente estudio, sus resultados podrían ser reflejo del esfuerzo por mejorar los tiempos de traslado y atención al paciente6, que se ha asociado invariablemente a mejoras en el pronóstico9,10, así como a una generalización de la técnica, no circunscrita solo a los casos más graves.
LimitacionesLas principales limitaciones de este estudio se derivan de tratarse de un estudio observacional desarrollado en un único centro. Sin embargo, el tamaño muestral es superior al de las publicaciones nacionales que han evaluado los resultados de planes regionales4–7,11 y con seguimiento del primer año tras el alta. Por otra parte, los recursos técnicos y farmacológicos, así como sus recomendaciones en las guías de práctica clínica, pudieron haber variado entre ambos periodos2,26,27; sin embargo, el personal médico fue el mismo durante ambos y no se cambió la forma de trabajo salvo por la organización del programa código infarto. Además, puesto que no se recogió toda la medicación administrada durante el ingreso, no se puede excluir que hubiera diferencias en el manejo farmacológico entre periodos, aunque se cree que estas diferencias debieron ser mínimas. Por último, el estudio no pudo analizar las diferencias en el coste derivadas de la implantación del código infarto; si bien es cierto que se observaron reducciones en la estancia hospitalaria media, no se puede excluir que se produjese un incremento en el consumo de materiales, recursos humanos y logísticos que pudiesen contrarrestar este ahorro.
CONCLUSIONESLa implantación del código infarto para un hospital secundario con unidad de hemodinámica se tradujo en un incremento del porcentaje de pacientes ingresados con SCACEST y con mayor puntuación GRACE. No se observaron cambios en la mortalidad hospitalaria total, salvo un mejor pronóstico en los pacientes de alto riesgo y una tendencia a la mejora en los pacientes con SCASEST. La angioplastia primaria se generalizó como forma de reperfusión y se redujo significativamente la estancia hospitalaria. Sin embargo, el pronóstico en el primer año tras el alta fue igual antes y después de la implantación del código infarto. Estos resultados indican que la implantación del código infarto conlleva mejoras en la organización y en la revascularización de todos los pacientes con SCA, no solo para los pacientes con SCACEST. La generalización de la angioplastia primaria conlleva la necesidad de organizar diferentes servicios relacionados con la atención urgente del SCACEST y los datos obtenidos muestran que la implantación de un código infarto condujo a mejorías en el tratamiento del SCA en general, pero especialmente de los pacientes de alto riesgo y/o con SCACEST. Estos datos respaldan la necesidad de implantar estos sistemas en los hospitales que no estén integrados en planes locales o regionales.
CONFLICTO DE INTERESESNinguno.