La aparición de trombosis del stent (TS) durante el seguimiento sigue siendo la complicación más temida tras la intervención coronaria percutánea (ICP). La TS se relaciona con resultados de mal pronóstico, y estudios previos notifican tasas de mortalidad de hasta el 30%1. Aunque la aparición de los stents farmacoactivos (SFA) superó considerablemente a los stents metálicos en términos de reestenosis, según los primeros informes, los SFA de primera generación se asociaban con mayor riesgo de TS2. La posterior introducción de los SFA de nueva generación (nuevos SFA), con struts más delgados y polímeros biodegradables o permanentes biocompatibles (o sin polímeros), redujo la tasa de TS, en particular en pacientes con TS muy tardía (TSMT)3. No obstante, hay pocos datos que comparen la tasa de TS entre los primeros SFA y los nuevos a muy largo plazo.
En un artículo recientemente publicado en Revista Española de Cardiología, Coughlan et al.4 contribuyeron con datos importantes en este campo. El estudio DECADE es un análisis conjunto de los datos de cada uno de los pacientes de 5 ensayos con SFA y 10 años de seguimiento5–9. Se dividió a los pacientes en 2 grupos (con SFA de primera generación y con los nuevos SFA) y el objetivo principal fue la TS definitiva hasta 10 años después de la ICP. En este estudio de colaboración multicéntrico se incluyó a 9.700 pacientes: 6.866 en el grupo con los nuevos SFA y 2.834 en el grupo con SFA de primera generación. Cabe destacar que los pacientes del grupo con los nuevos SFA eran de más edad y padecían con mayor frecuencia diabetes y enfermedad multivaso. Además, en este mismo grupo se constató una mayor proporción de lesiones en bifurcación y complejas. A todos los pacientes se les prescribió un tratamiento antiagregante plaquetario doble con ácido acetilsalicílico por tiempo indefinido y clopidogrel durante un periodo de 6 a 12 meses tras la ICP.
Los principales resultados del estudio se resumen en: a) en dicho análisis conjunto de 5 ensayos multicéntricos, la incidencia acumulada de TS definitiva a los 10 años de seguimiento con los nuevos SFA fue del 1%; b) la TS definitiva fue menos frecuente con los nuevos SFA que con los de primera generación (el 1 frente al 3,5%; hazard ratio [HR] ajustada=0,32; intervalo de confianza del 95% [IC95%], 0,23-0,45), en especial con respecto a la TSMT (el 0,3 frente al 1,5%; HR ajustada=0,16; IC95%, 0,09-0,28) y TS extremadamente tardía (más de 5 años tras la ICP) (el 0,2 frente al 0,9%; HR ajustada=0,25; IC95%, 0,23-0,45). Este es el primer estudio conjunto que compara la TS entre los SFA de primera generación y los nuevos a los 10 años de seguimiento, y constituye la cohorte más grande en la que la atención se fija en resultados muy tardíos con SFA de nueva generación.
Se debe felicitar a los autores por este esfuerzo de colaboración con significativas implicaciones clínicas. Además, algunos aspectos del estudio de Coughlan et al. merecen otros comentarios. En primer lugar, este estudio4 es en buena medida una comparación indirecta, ya que en solo 2 de los 5 ensayos se compararon directamente los SFA de primera generación con los nuevos y la mayoría de los pacientes con SFA de primera generación procedían de estudios más antiguos. Puede que los resultados hayan mejorado por las técnicas de implante y el mejor tratamiento médico (p. ej., se ha observado que el tratamiento intensivo con rosuvastatina y ácido eicosapentaenoico previene la neoateroesclerosis del stent10, que da cuenta de una tercera parte de la TSMT, y una combinación de rosuvastatina y alirocumab fomenta la estabilización de la placa y reduce el infarto de miocardio11). Además, en un estudio con tomografía de coherencia óptica de pacientes con TSMT (media tras el implante, 4,8 años) se observaron diferencias mínimas entre los SFA de primera generación y los nuevos12. En segundo lugar, el objetivo principal no incluyó datos sobre la TS probable o posible y se limitó a la TS definitiva, lo que puede haber subestimado parcialmente la incidencia de TS. Cabe destacar que en el ensayo SIRTAX8, que incluía un tercio de pacientes del grupo tratado con SFA de primera generación, se hizo una definición de TS distinta. No obstante, el análisis actual tiene gran valor clínico y añade información importante en este contexto.
La TS pasó a ser una preocupacón seria con la introducción de los SFA de primera generación, y en los primeros informes no se observaron indicios claros de atenuación del riesgo de TS más allá del primer año tras la ICP. Aunque la etiología de la TSMT es multifactorial, al parecer la respuesta inflamatoria al polímero permanente utilizado en el SFA de primera generación tuvo un papel importante. En el presente estudio, Coughlan et al. demostraron que las mejoras incluidas en los nuevos SFA al parecer reducían la TS definitiva en el seguimiento a largo plazo frente a los SFA de primera generación. Cabe destacar que la incidencia acumulada de TS definitiva fue baja (el 1% a los 10 años) y se observó una disminución constante de su aparición al cabo de 1 año de la ICP2. Esto añade datos tranquilizadores en relación con los últimos resultados clínicos tras la ICP con SFA de nueva generación.
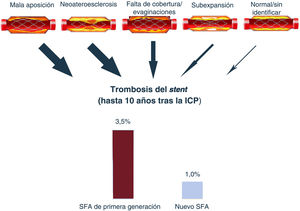
En el presente análisis no se observaron diferencias en la TS entre los SFA de primera generación y los nuevos durante el primer año tras la ICP, tanto en la subaguda (< 1 mes) como en la tardía (entre 1 y 12 meses)4. Aunque esto podría explicarse por error, podría indicar que, a diferencia de la TSMT, su aparición en los primeros meses tras la ICP (en especial las primeras semanas) podría depender más de factores relacionados con la intervención quirúrgica y con la lesión, con riesgo inicial del paciente y con el tratamiento antitrombótico. En cambio, las principales causas relacionadas con la TSMT son, por orden: posición anómala (∼35%), neoateroesclerosis (∼30%), ausencia de cobertura del strut (10-15%), incapacidad de expansión de este (5-10%) y otras (enfermedad del borde, reestenosis, etc.) (∼5%)12 (figura 1). Así pues, aunque la ausencia de toxicidad de los polímeros y los struts finos podrían explicar la reducción considerable de la TSMT, hay que reconocer que las modernas técnicas de implante y el tratamiento intensivo también pueden haber cumplido una función en esta disminución de los episodios.
Por otro lado, la duración del tratamiento dual con antiagregantes plaquetarios junto con el uso de inhibidores de P2Y12 más potentes es clave en los resultados clínicos durante los primeros meses tras la ICP. En el presente estudio, no se utilizaron el prasugrel ni el ticagrelor, lo que podría haber reducido la tasa de TS durante el primer año tras la ICP. Además, la tasa muy reducida de TS a largo plazo con las técnicas de implante y el tratamiento actuales coincide con la tendencia actual de reducir la duración del tratamiento antiagregante plaquetario doble tras la ICP13. Esta tasa tan baja de episodios hasta los 10 años de seguimiento no justificaría el riesgo de hemorragia asociado con la larga duración del tratamiento antiagregante plaquetario doble.
Cabe destacar que la tecnología de los SFA sigue mejorando. Los modernos SFA ultrafinos (< 60 μm) han superado a los nuevos SFA incluidos en el presente análisis14, y los SFA de segunda generación con tecnología mejorada para la liberación del fármaco han mostrado mejores resultados clínicos que otras plataformas contemporáneas de stents en subgrupos con alto riesgo como el de los pacientes con diabetes15,16.
En conclusión, el estudio de Coughlan et al.4 añade información nueva sobre la tolerabilidad a largo plazo de los nuevos SFA, con una baja incidencia de TS definitiva durante los 10 años de seguimiento. Aunque el tratamiento general de los pacientes con una arteriopatía coronaria debería seguir mejorando, este estudio de colaboración multicéntrico añade datos tranquilizadores en el difícil contexto de los resultados tardíos relacionados con el stent tras la ICP.
FINANCIACIÓNNinguna.
CONFLICTO DE INTERESESR. Romaguera ha recibido honorarios de conferenciante de Medtronic, Biosensors, Alvimedica y Biotronik, y es proctor para Boston Scientific. Los demás autores afirman no tener ningún conflicto de intereses.