El desarrollo de anticuerpos contra antígenos leucocitarios humanos es una complicación conocida de la asistencia ventricular de larga duración. El propósito del presente estudio es evaluar su incidencia durante el empleo de dispositivos de asistencia ventricular de corta duración (DAVC) (CentriMag), sus determinantes y su repercusión en los resultados del trasplante cardiaco.
MétodosEstudio retrospectivo con pacientes tratados con DAVC como puente al trasplante entre 2009 y 2019. Se consideró sensibilización un panel reactivo de anticuerpos calculado> 10%. Las variables de respuesta fueron supervivencia y supervivencia libre de rechazo agudo (RA).
ResultadosSe trató con DAVC a 89 pacientes, con una mediana de edad de 56,0 [intervalo intercuartílico, 50,0-59,9] años y el 16,8% de mujeres, durante una mediana de 23,6 [16,6-35,0] días. El 12,4% se sensibilizó durante la asistencia. El único determinante independiente de la sensibilización fue el sexo femenino (OR=8,67; IC95%, 1,93-38,8; p=0,005). De los 89 pacientes, 21 fallecieron durante la asistencia y 68 se sometieron a trasplante. De los pacientes trasplantados, 8 (11,8%) fallecieron y 20 (29,4%) tuvieron algún episodio de RA tras un seguimiento promedio de 49,6 ±31,2 meses tras el trasplante. Tras ajuste multivariable, la sensibilización aumentó el riesgo de RA (HR=3,64; IC95%, 1,42-9,33; p=0,007), con una tendencia no significativa a mayor mortalidad (HR=4,07; IC95%, 0,96-17,3; p=0,057).
ConclusionesLa sensibilización relacionada con los DAVC es posible, predomina en el sexo femenino y se asocia de manera significativa con el RA, con una tendencia no significativa a mayor mortalidad.
Palabras clave
Está bien establecido el papel de las asistencias ventriculares de media-larga duración en el desarrollo de anticuerpos contra antígenos leucocitarios humanos (HLA). Este fenómeno se asocia con diferentes factores como la interacción entre el biomaterial del dispositivo implantado y el sistema inmunitario del receptor, la mayor necesidad de transfusiones, el sexo femenino, la multiparidad y las cirugías previas1. La sensibilización podría tener un impacto negativo en el resultado tras el trasplante, pues se ha asociado con un mayor riesgo de rechazo agudo (RA), particularmente mediado por anticuerpos, y de enfermedad vascular del injerto1,2. Algunos estudios han encontrado mayor mortalidad tras el trasplante, aunque esto no es un hallazgo universal2,3.
Los dispositivos de asistencia ventricular de corta duración (DAVC) como puente directo al trasplante son un recurso poco extendido, y se utilizan fundamentalmente como puente a sistemas de asistencia más larga. Por ello, se ha estudiado poco hasta ahora su papel como potencial factor sensibilizante y el impacto pronóstico de dicha sensibilización4. Sin embargo, en España, el mayor acceso al trasplante y las mayores restricciones económicas para el implante de dispositivos de asistencia ventricular de larga duración (DAVL) condicionan una situación particular, en la que los DAVC son la estrategia más utilizada como puente al trasplante5.
En la literatura actual, el impacto de la sensibilización durante la asistencia se limita a los pacientes a los que se han implantado DAVL como puente al trasplante6. Por lo tanto, el propósito de este estudio es evaluar la incidencia de sensibilización durante la asistencia con DAVC de tipo CentriMag como puente al trasplante y sus determinantes, describir la actitud terapéutica en los pacientes sensibilizados y determinar el impacto de la sensibilización en la evolución tras el trasplante.
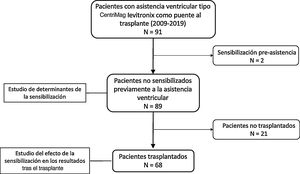
MÉTODOSDiseño y población del estudioSe realizó un estudio observacional retrospectivo y se incluyó a los pacientes a los que se implantó un DAVC (CentriMag, Abbott, Estados Unidos) como puente al trasplante entre julio de 2009 y noviembre de 2019 en nuestro centro (figura 1). Se recogieron datos sobre las características demográficas y clínicas de los pacientes (edad, sexo, miocardiopatía de base, presencia de diabetes mellitus, insuficiencia renal, cirugía cardiaca previa), las características de la asistencia (derecha, izquierda o biventricular, duración, reintervenciones, empleo previo de oxigenador extracorpóreo de membrana [ECMO] y balón de contrapulsación intraaórtico, infecciones y transfusiones) y el estado de sensibilización. Del grupo de trasplantados, se recogieron las características de los tratamientos de inducción y desensibilizante y de la inmunosupresión inicial.
El objetivo primario del estudio fue analizar la mortalidad por todas las causas tras el trasplante. El objetivo secundario, evaluar la incidencia de RA en el seguimiento, definido como todo evento clínico —observación en la biopsia endomiocárdica de un grado de rechazo ≥ 2R según la clasificación de la Sociedad Internacional de Trasplante de Corazón y Pulmón de 2004 o una ecocardiografía que indicara una caída en la fracción de eyección (FE)> 10% o una FE<40% que antes era superior— que motivara un aumento transitorio de la inmunosupresión, consistente en una tanda corta de corticoides por vía oral o intravenosa, junto con tratamiento citolítico o no7.
El estudio fue aprobado por el Comité de Ética de Investigación Clínica correspondiente.
Protocolo de uso de asistencias ventriculares de corta duración como puente a trasplanteLa asistencia con DAVL es un tratamiento establecido para la insuficiencia cardiaca terminal en otros países de nuestro entorno. La mayor disponibilidad de donantes en nuestro medio ha permitido en los últimos años la utilización de DAVC como puente al trasplante cardiaco (TxC) para los pacientes que sufren un deterioro clínico a la espera de trasplante o se presentan en situación INTERMACS avanzada. En nuestro centro se opta por los DAVC tipo Levitronix como puente al trasplante en detrimento de otro tipo de sistemas por el mayor potencial para conseguir una asistencia adecuada y que permita una recuperación orgánica y funcional óptima para afrontar el trasplante. Incluso para los pacientes en situación de shock cardiogénico profundo que precisan asistencia percutánea con ECMO venoarterial, una vez desestimada la opción de recuperación y evaluada la aptitud para el trasplante, se opta por la conversión a un sistema de asistencia ventricular central antes de incluirlos en lista de espera.
El paciente entra en lista de espera una vez ha alcanzado la recuperación orgánica y ha sido posible una relativa optimización de su situación funcional. Como norma general, la ventilación mecánica invasiva, la presencia de infecciones no resueltas o el fallo orgánico persistente se consideran contraindicación para la inclusión en lista de espera.
La estrategia quirúrgica de elección es la esternotomía media y la canulación de la aurícula derecha y la arteria pulmonar para la asistencia derecha y el ápex ventricular izquierdo y la aorta ascendente para la asistencia izquierda.
El momento de inicio de la anticoagulación y el objetivo terapéutico se individualizan en función de los riesgos hemorrágico y trombótico particulares, y se demora el inicio de la anticoagulación al menos 16 h tras el implante. La heparina sódica es el fármaco de elección, con determinación de anticuerpos anti-Xa y controles de tiempo de tromboplastina activado (TTPa) para monitorizar el ajuste de dosis.
Determinación de anticuerposLa presencia de anticuerpos anti-HLA se analizó en los sueros seleccionados mediante tecnología Luminex con los reactivos Single Antigen (LABScreen, Single Antigenclass-I and class-II, One Lambda), antes del implante del dispositivo en los casos en que se implantó electivamente, 2 semanas tras un evento sensibilizante en los casos factibles y antes de la inclusión en lista de espera de TxC. Se consideraron eventos sensibilizantes la transfusión de hemoderivados durante la asistencia y las reintervenciones quirúrgicas, incluido el cambio de sistema durante la asistencia.
Se obtuvo el panel reactivo de anticuerpos calculado (PRAc) total antes y después del implante del dispositivo a partir de las especificidades detectadas con el Luminex, utilizando la calculadora Eurotrasplant8. A efectos de este trabajo, se definió la sensibilización como un PRAc> 10%1,6.
Análisis estadísticoLas variables continuas se describen como media ±desviación estándar o como mediana [intervalo intercuartílico] en función de que se cumpliera la presunción de normalidad comprobada mediante el test de Kolmogorov-Smirnov. Las variables categóricas se expresan como frecuencia y porcentaje. Las diferencias entre pacientes sensibilizados y no sensibilizados se analizaron mediante los test de la t de Student o de la U de Mann-Whitney para variables continuas y el test de la χ2 o el exacto de Fisher para variables categóricas.
La asociación entre las variables de estudio y la incidencia de sensibilización se analizó mediante regresión logística. El tiempo hasta la muerte por todas las causas tras el trasplante y el tiempo hasta la incidencia de rechazo se analizaron mediante regresión de Cox. Para los análisis multivariables, se ajustaron 2 modelos alternativos que incluyen las variables con nivel de significación<0,10 (modelo 1) o<0,20 (modelo 2) en el análisis univariable. Las variables se introdujeron escalonadamente hacia atrás. Todos los test fueron de 2 colas y el nivel de significación se fijó en p<0,05. El análisis estadístico se realizó mediante SPSS 25.0 (SPSS Inc., Estados Unidos).
RESULTADOSCaracterísticas de los pacientesEntre los años 2009 y 2019, se implantaron en nuestro centro 91 DAVC de tipo Levitronix CentriMag como puente al trasplante. Dos pacientes mostraron valores altos de PRAc antes del implante y se los excluyó del análisis (figura 1). Por lo tanto, formaron el grupo de estudio 89 pacientes, con una mediana de edad de 56 [50,0-59,9] años y el 16,8% de mujeres. La cardiopatía de base más frecuente fue la miocardiopatía dilatada (51 pacientes, 57,3%). En nuestra serie, 23 pacientes (25,84%) se encontraban ya en lista de TxC electiva. En estos, los anticuerpos anti-HLA se determinaron antes de incluir en lista electiva. Tras el implante de la asistencia, se realizó al menos una nueva determinación de anticuerpos antes de la inclusión en alarma 0. En el 44,9% de los pacientes, una segunda determinación fue factible a las 2 semanas de un evento sensibilizante. Con ello, el número medio de determinaciones de anticuerpos anti-HLA por paciente fue de 1,55 ±0,5. Se implantó un DAVC izquierdo en el 56,2% de los casos. La mediana de duración de la asistencia fue de 23,6 [16,6-35,0] días. Las características de la población total y según su estado de sensibilización se resumen en la tabla 1.
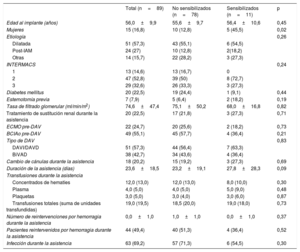
Características basales de los pacientes del estudio
| Total (n=89) | No sensibilizados (n=78) | Sensibilizados (n=11) | p | |
|---|---|---|---|---|
| Edad al implante (años) | 56,0±9,9 | 55,6±9,7 | 56,4±10,6 | 0,45 |
| Mujeres | 15 (16,8) | 10 (12,8) | 5 (45,5) | 0,02 |
| Etiología | 0,26 | |||
| Dilatada | 51 (57,3) | 43 (55,1) | 6 (54,5) | |
| Post-IAM | 24 (27) | 10 (12,8) | 2(18,2) | |
| Otras | 14 (15,7) | 22 (28,2) | 3 (27,3) | |
| INTERMACS | 0,24 | |||
| 1 | 13 (14,6) | 13 (16,7) | 0 | |
| 2 | 47 (52,8) | 39 (50) | 8 (72,7) | |
| 3 | 29 (32,6) | 26 (33,3) | 3 (27,3) | |
| Diabetes mellitus | 20 (22,5) | 19 (24,4) | 1 (9,1) | 0,44 |
| Esternotomía previa | 7 (7,9) | 5 (6,4) | 2 (18,2) | 0,19 |
| Tasa de filtrado glomerular (ml/min/m2) | 74,6±47,4 | 75,1±50,2 | 68,0±16,8 | 0,82 |
| Tratamiento de sustitución renal durante la asistencia | 20 (22,5) | 17 (21,8) | 3 (27,3) | 0,71 |
| ECMO pre-DAV | 22 (24,7) | 20 (25,6) | 2 (18,2) | 0,73 |
| BCIAo pre-DAV | 49 (55,1) | 45 (57,7) | 4 (36,4) | 0,21 |
| Tipo de DAV | 0,83 | |||
| DAVI/DAVD | 51 (57,3) | 44 (56,4) | 7 (63,3) | |
| BiVAD | 38 (42,7) | 34 (43,6) | 4 (36,4) | |
| Cambio de cánulas durante la asistencia | 18 (20,2) | 15 (19,2) | 3 (27,3) | 0,69 |
| Duración de la asistencia (días) | 23,6±18,5 | 23,2±19,1 | 27,8±28,3 | 0,09 |
| Transfusiones durante la asistencia | ||||
| Concentrados de hematíes | 12,0 (13,0) | 12,0 (13,0) | 8,0 (10,0) | 0,30 |
| Plasma | 4,0 (5,0) | 4,0 (5,0) | 5,0 (9,0) | 0,48 |
| Plaquetas | 3,0 (5,0) | 3,0 (4,0) | 3,0 (6,0) | 0,87 |
| Transfusiones totales (suma de unidades transfundidas) | 19,0 (19,5) | 18,5 (20,0) | 19,0 (18,0) | 0,73 |
| Número de reintervenciones por hemorragia durante la asistencia | 0,0±1,0 | 1,0±1,0 | 0,0±1,0 | 0,37 |
| Pacientes reintervenidos por hemorragia durante la asistencia | 44 (49,4) | 40 (51,3) | 4 (36,4) | 0,52 |
| Infección durante la asistencia | 63 (69,2) | 57 (71,3) | 6 (54,5) | 0,30 |
BCIAo: balón de contrapulsación intraaórtico; BiVAD: dispositivo de asistencia biventricular; DAV: dispositivo de asistencia ventricular; DAVD: dispositivo de asistencia ventricular derecha; DAVI: dispositivo de asistencia ventricular izquierda; ECMO: oxigenador extracorpóreo de membrana; IAM: infarto agudo de miocardio; INTERMACS: Interagency Registry for Mechanically Assisted Circulatory Support.
Los valores expresan n (%) o media±desviación estándar.
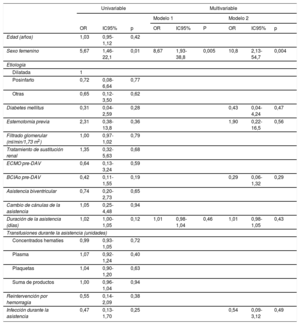
Once pacientes (12,4%) desarrollaron anticuerpos anti-HLA de novo durante la asistencia. Todos los pacientes sensibilizados llegaron al TxC. El PRAc promedio fue de 45,6%±27,8% [11,0%-90,2%]. Se consideró positivo un anticuerpo si la intensidad de fluorescencia media era> 1.000-1.500 y de significado dudoso si la intensidad de fluorescencia media se encontraba entre 500 y 1.000. En nuestro caso, 10 de los pacientes sensibilizados presentaban un título> 1.500 —mediana, 5.758 [3.200-7.000]— y no se dispuso de dicha información del restante. Todos desarrollaron anticuerpos anti-HLA de clase I y 4, también anticuerpos de clase II. Hubo un mayor porcentaje de mujeres (45,5%) en el grupo de sensibilizados que en el de no sensibilizados (12,8%; p=0,02). Asimismo, se observó una tendencia no significativa a una mayor duración de la asistencia en los sensibilizados, con una mediana de 27,8 [23,6-51,8] días respecto a los no sensibilizados: mediana, 23,2 [15,2-34,3] días (p=0,09). En el análisis univariable (tabla 2), solo el sexo femenino se asoció significativamente con la aparición de anticuerpos durante la asistencia (odds ratio [OR]=5,67; intervalo de confianza del 95% [IC95%], 1,46-22,1; p=0,01), con una tendencia no significativa para la duración de la asistencia (OR=1,02; IC95%, 1,00-1,05; p=0,12). Otras variables con gran tendencia a la asociación, pero sin significación estadística, se recogen en la tabla 2. En un primer modelo que incluye el sexo y la duración de la asistencia, solo el sexo femenino se asoció con sensibilización durante la asistencia (OR=8,67; IC95%, 1,93-38,8; p=0,005). Un resultado similar se obtuvo en un segundo modelo que incluye además el segundo grupo de variables descrito (OR=10,8; IC95%, 2,13-54,7; p=0,004) (tabla 2).
Determinantes de la sensibilización durante la asistencia circulatoria de corta duración como puente al trasplante
| Univariable | Multivariable | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Modelo 1 | Modelo 2 | ||||||||
| OR | IC95% | p | OR | IC95% | P | OR | IC95% | p | |
| Edad (años) | 1,03 | 0,95-1,12 | 0,42 | ||||||
| Sexo femenino | 5,67 | 1,46-22,1 | 0,01 | 8,67 | 1,93-38,8 | 0,005 | 10,8 | 2,13-54,7 | 0,004 |
| Etiología | |||||||||
| Dilatada | 1 | ||||||||
| Posinfarto | 0,72 | 0,08-6,64 | 0,77 | ||||||
| Otras | 0,65 | 0,12-3,50 | 0,62 | ||||||
| Diabetes mellitus | 0,31 | 0,04-2,59 | 0,28 | 0,43 | 0,04-4,24 | 0,47 | |||
| Esternotomía previa | 2,31 | 0,38-13,8 | 0,36 | 1,90 | 0,22-16,5 | 0,56 | |||
| Filtrado glomerular (ml/min/1,73 m2) | 1,00 | 0,97-1,02 | 0,79 | ||||||
| Tratamiento de sustitución renal | 1,35 | 0,32-5,63 | 0,68 | ||||||
| ECMO pre-DAV | 0,64 | 0,13-3,24 | 0,59 | ||||||
| BCIAo pre-DAV | 0,42 | 0,11-1,55 | 0,19 | 0,29 | 0,06-1,32 | 0,29 | |||
| Asistencia biventricular | 0,74 | 0,20-2,73 | 0,65 | ||||||
| Cambio de cánulas de la asistencia | 1,05 | 0,25-4,48 | 0,94 | ||||||
| Duración de la asistencia (días) | 1,02 | 1,00-1,05 | 0,12 | 1,01 | 0,98-1,04 | 0,46 | 1,01 | 0,98-1,05 | 0,43 |
| Transfusiones durante la asistencia (unidades) | |||||||||
| Concentrados hematíes | 0,99 | 0,93-1,05 | 0,72 | ||||||
| Plasma | 1,07 | 0,92-1,24 | 0,40 | ||||||
| Plaquetas | 1,04 | 0,90-1,20 | 0,63 | ||||||
| Suma de productos | 1,00 | 0,96-1,04 | 0,94 | ||||||
| Reintervención por hemorragia | 0,55 | 0,14-2,09 | 0,38 | ||||||
| Infección durante la asistencia | 0,47 | 0,13-1,70 | 0,25 | 0,54 | 0,09-3,12 | 0,49 | |||
BCIAo: balón de contrapulsación intraaórtico; DAV: dispositivo de asistencia ventricular; ECMO: oxigenador extracorpóreo de membrana; IC95%: intervalo de confianza del 95%; OR: odds ratio.
Modelo 1 incluye sexo y duración de la asistencia (días).
Modelo 2 incluye las variables de modelo 1 más diabetes, esternotomía previa, balón de contrapulsación previo al DAV e infección durante la asistencia.
Un total de 21 pacientes (23,6%) fallecieron durante la asistencia, tras una mediana de 17,4 [3,3-23,2] días desde el inicio de esta. Las causas de fallecimiento fueron infección (28,6%), ictus isquémico (14,3%), hemorragia (14,3%), fracaso multiorgánico (9,5%), futilidad (9,5%), ictus hemorrágico (4,8%) y otras (19%). Se trasplantó a 68 pacientes (76,4%) tras una mediana de 28,2 [19,6-39,8] días de asistencia. Las características demográficas y clínicas de los pacientes trasplantados se resumen en la .
Todos los pacientes recibieron un protocolo de inmunosupresión inicial basado en tacrolimus, micofenolato y corticoides, con los ajustes pertinentes en casos de alto riesgo infeccioso o insuficiencia renal. Se indujo con basiliximab a 56 (70%) de los pacientes no sensibilizados, y de los pacientes sensibilizados, a 10 (91%) con anticuerpos antitimocito inmediatamente después del trasplante. Al restante, con basiliximab. Antes del trasplante, se dio tratamiento desensibilizante mediante plasmaféresis y rituximab a 3 pacientes que presentaban valores de PRAc >25%. Para los otros 3 pacientes altamente sensibilizados se descartó la desensibilización por un balance riesgo-beneficio desfavorable (tabla 3). En los 11 pacientes se realizaron las pruebas cruzadas donante-receptor (crossmatch retrospectivo), que resultaron negativas en 10 (91%).
Características, actitud terapéutica y evolución de los pacientes sensibilizados durante la asistencia circulatoria de corta duración como puente al trasplante
| Paciente | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Edad (años) | 56 | 55 | 52 | 57 | 62 | 55 | 67 | 36 | 63 | 50 | 60 |
| Sexo | Varón | Varón | Varón | Varón | Mujer | Mujer | Mujer | Varón | Mujer | Varón | Mujer |
| Indicación de la asistencia | MCD | MCD | MCD | Post-IAM | MCD | MCH | Post-IAM | Congénita | Post-CEC | MCD | MCD |
| Dispositivo | DAVI | DAVI | DAVI | BiVAD | BiVAD | DAVI | DAVI | DAVI | BiVAD | BiVAD | DAVI |
| % PRA | 30,0 | 11,0 | 19,7 | 22,0 | 23,4 | 79,0 | 74,0 | 39,6 | 90,2 | 70,0 | 43,0 |
| Clase de anti-HLA | I | I y II | I | I | I | I y II | I y II | I | I y II | I | I |
| Anticuerpos específicos de donante | No | Posible | No | No | No | No | No | No | No | No | No |
| Inducción con timoglobulina | No | Sí | Sí | Sí | Sí | Sí | Sí | Sí | Sí | Sí | Sí |
| Inducción con basiliximab | Sí | No | No | No | No | No | No | Sí | No | No | No |
| Plasmaféresis+rituximab | No | No | No | No | No | Sí | Sí | Sí | No | No | No |
| Rechazo tras el trasplante | Sí | Sí | No | No | No | No | Sí | Sí | Sí | Sí | Sí |
| Biopsia endomiocárdica | No | No | - | - | - | - | Sí | Sí | No | No | No |
| Rechazo mediado por anticuerpos (clasificación ISHLT) | - | Sí/pAMR2 | - | - | - | - | Sí/pAMR2 | No | - | - | - |
| Rechazo celular (clasificación ISHLT) | - | No | - | - | - | - | Sí/2R | Sí/2R | - | - | - |
| Mortalidad tras el trasplante | No | No | No | No | No | Sí | Sí | No | No | Sí | No |
| Fallecimiento por rechazo | - | - | - | - | - | No | Sí | - | - | Sí | - |
BiVAD: dispositivo de asistencia biventricular; CEC: circulación extracorpórea; DAVI: dispositivo de asistencia ventricular izquierda; HLA: antígenos leucocitarios humanos; IAM: infarto agudo de miocardio; ISHLT: International Society of Heart and Lung Transplantation; MCD: miocardiopatía dilatada; MCH: miocardiopatía hipertrófica; pAMR: rechazo mediado por anticuerpos; PRA: panel reactivo de anticuerpos.
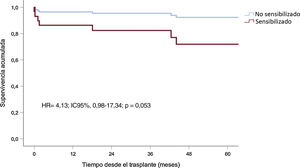
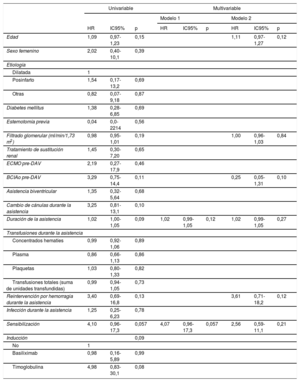
Durante un seguimiento medio tras el trasplante de 49,6±31,2 meses, fallecieron 8 (11,8%) de los 68 pacientes trasplantados, 3 de ellos en el grupo de los sensibilizados (27,3%) y 5 en el de los no sensibilizados (8,8%; p=0,046) (HR=4,10; IC95%, 0,96-17,28; p=0,057). La duración de la asistencia antes del trasplante mostró una tendencia no significativa a asociarse con mayor mortalidad (HR=1,02; IC95%, 1,00-1,05; p=0,09) (tabla 4). El uso de inducción (p=0,09) o el cambio de cánulas durante la asistencia (p=0,10) mostraron una tendencia no significativa a la asociación con la mortalidad. Las últimas 2 variables no se introdujeron en los análisis multivariables para limitar su posible colinealidad debido a la alta correlación que mostraron con la sensibilización pretrasplante (ρ=0,63; p=7,9×10–19) y la duración de la asistencia circulatoria (ρ=0,76; p=6,3×10–14) respectivamente. En el modelo multivariable abreviado, incluyendo solo el estado de sensibilización y la duración del soporte, la sensibilización pretrasplante mostró una tendencia a la asociación con la supervivencia tras el trasplante (HR=4,07; IC95%, 0,96-17,28; p=0,057) (figura 2). En el modelo ampliado, la asociación entre sensibilización y mortalidad tras el trasplante fue menor y no alcanzó significación estadística (HR=2,56; IC95%, 0,59-11,1; p=0,21) (tabla 4).
Determinantes de la mortalidad tras el trasplante en pacientes con asistencia ventricular temporal previa al trasplante (regresión de Cox)
| Univariable | Multivariable | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Modelo 1 | Modelo 2 | ||||||||
| HR | IC95% | p | HR | IC95% | p | HR | IC95% | p | |
| Edad | 1,09 | 0,97-1,23 | 0,15 | 1,11 | 0,97-1,27 | 0,12 | |||
| Sexo femenino | 2,02 | 0,40-10,1 | 0,39 | ||||||
| Etiología | |||||||||
| Dilatada | 1 | ||||||||
| Posinfarto | 1,54 | 0,17-13,2 | 0,69 | ||||||
| Otras | 0,82 | 0,07-9,18 | 0,87 | ||||||
| Diabetes mellitus | 1,38 | 0,28-6,85 | 0,69 | ||||||
| Esternotomía previa | 0,04 | 0,0-2214 | 0,56 | ||||||
| Filtrado glomerular (ml/min/1,73 m2) | 0,98 | 0,95-1,01 | 0,19 | 1,00 | 0,96-1,03 | 0,84 | |||
| Tratamiento de sustitución renal | 1,45 | 0,30-7,20 | 0,65 | ||||||
| ECMO pre-DAV | 2,19 | 0,27-17,9 | 0,46 | ||||||
| BCIAo pre-DAV | 3,29 | 0,75-14,4 | 0,11 | 0,25 | 0,05-1,31 | 0,10 | |||
| Asistencia biventricular | 1,35 | 0,32-5,64 | 0,68 | ||||||
| Cambio de cánulas durante la asistencia | 3,25 | 0,81-13,1 | 0,10 | ||||||
| Duración de la asistencia | 1,02 | 1,00-1,05 | 0,09 | 1,02 | 0,99-1,05 | 0,12 | 1,02 | 0,99-1,05 | 0,27 |
| Transfusiones durante la asistencia | |||||||||
| Concentrados hematíes | 0,99 | 0,92-1,06 | 0,89 | ||||||
| Plasma | 0,86 | 0,66-1,13 | 0,86 | ||||||
| Plaquetas | 1,03 | 0,80-1,33 | 0,82 | ||||||
| Transfusiones totales (suma de unidades transfundidas) | 0,99 | 0,94-1,05 | 0,73 | ||||||
| Reintervención por hemorragia durante la asistencia | 3,40 | 0,69-16,8 | 0,13 | 3,61 | 0,71-18,2 | 0,12 | |||
| Infección durante la asistencia | 1,25 | 0,25-6,23 | 0,78 | ||||||
| Sensibilización | 4,10 | 0,96-17,3 | 0,057 | 4,07 | 0,96-17,3 | 0,057 | 2,56 | 0,59-11,1 | 0,21 |
| Inducción | 0,09 | ||||||||
| No | 1 | ||||||||
| Basiliximab | 0,98 | 0,16-5,89 | 0,99 | ||||||
| Timoglobulina | 4,98 | 0,83-30,1 | 0,08 | ||||||
BCIAo: balón de contrapulsación (intraaórtico); DAV: dispositivo de asistencia ventricular; ECMO: oxigenador extracorpóreo de membrana; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Modelo 1 incluye estado de sensibilización y duración de la asistencia.
Modelo 2 incluye las variables del modelo 1 más edad, filtrado glomerular, reintervención durante el soporte y BCIAo previo a la asistencia ventricular.
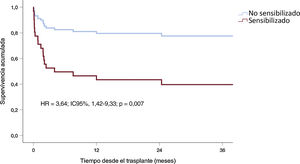
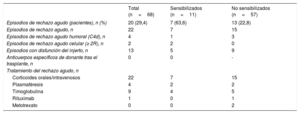
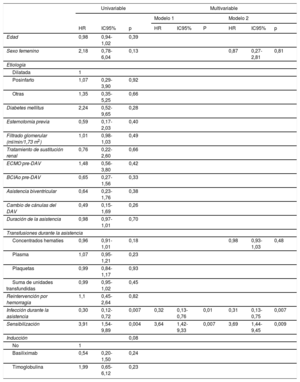
En el seguimiento, 20 pacientes (29,4%) tuvieron al menos 1 evento de RA (18 pacientes, 1 eventos; 2 pacientes, 2 eventos), una mediana de 1,6 [0,1-63,9] meses después del trasplante. De los episodios de rechazo, 4 fueron RA mediado por anticuerpos y 2, RA celular, demostrados mediante biopsia endomiocárdica. Un 59,1% de los episodios de rechazo se presentaron con disfunción del injerto (caída en la FE >10% o una FE< 40% tras haber sido superior). Las principales características de los episodios de rechazo en el grupo de pacientes sensibilizados y no sensibilizados se resumen en la tabla 5. Hubo rechazo en 7 pacientes sensibilizados (63,6%) y en 13 no sensibilizados (23,2%; p=0,01). El riesgo de un primer rechazo de los sensibilizados fue significativamente superior que el de los no sensibilizados (HR=3,90; IC95%, 1,54-9,90; p=0,004). La incidencia de infección durante la asistencia fue un factor protector contra el rechazo (HR=0,30; IC95%, 0,12-0,72; p=0,007). Ninguna otra variable de las analizadas se asoció con la incidencia de rechazo, aunque la inducción pretrasplante mostró una tendencia no significativa (tabla 6). Esta variable no se introdujo en los modelos ajustados debido a su alta correlación con el estado de sensibilización pretrasplante. En el ajuste multivariable, la sensibilización continuó mostrando una asociación estadísticamente significativa con la incidencia de rechazo (HR=3,64; IC95%, 1,42-9,33; p=0,007) tanto en el modelo simplificado como en el ampliado (tabla 6, figura 3).
Características y protocolo diagnóstico-terapéutico de los pacientes según su estado de sensibilización
| Total (n=68) | Sensibilizados (n=11) | No sensibilizados (n=57) | |
|---|---|---|---|
| Episodios de rechazo agudo (pacientes), n (%) | 20 (29,4) | 7 (63,6) | 13 (22,8) |
| Episodios de rechazo agudo, n | 22 | 7 | 15 |
| Episodios de rechazo agudo humoral (C4d), n | 4 | 1 | 3 |
| Episodios de rechazo agudo celular (≥ 2R), n | 2 | 2 | 0 |
| Episodios con disfunción del injerto, n | 13 | 5 | 9 |
| Anticuerpos específicos de donante tras el trasplante, n | 0 | 0 | - |
| Tratamiento del rechazo agudo, n | |||
| Corticoides orales/intravenosos | 22 | 7 | 15 |
| Plasmaféresis | 4 | 2 | 2 |
| Timoglobulina | 9 | 4 | 5 |
| Rituximab | 1 | 0 | 1 |
| Metotrexato | 0 | 0 | 2 |
Determinantes de la incidencia de rechazo agudo en pacientes con asistencia ventricular temporal antes del trasplante (regresión de Cox)
| Univariable | Multivariable | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Modelo 1 | Modelo 2 | ||||||||
| HR | IC95% | p | HR | IC95% | P | HR | IC95% | p | |
| Edad | 0,98 | 0,94-1,02 | 0,39 | ||||||
| Sexo femenino | 2,18 | 0,78-6,04 | 0,13 | 0,87 | 0,27-2,81 | 0,81 | |||
| Etiología | |||||||||
| Dilatada | 1 | ||||||||
| Posinfarto | 1,07 | 0,29-3,90 | 0,92 | ||||||
| Otras | 1,35 | 0,35-5,25 | 0,66 | ||||||
| Diabetes mellitus | 2,24 | 0,52-9,65 | 0,28 | ||||||
| Esternotomía previa | 0,59 | 0,17-2,03 | 0,40 | ||||||
| Filtrado glomerular (ml/min/1,73 m2) | 1,01 | 0,98-1,03 | 0,49 | ||||||
| Tratamiento de sustitución renal | 0,76 | 0,22-2,60 | 0,66 | ||||||
| ECMO pre-DAV | 1,48 | 0,56-3,80 | 0,42 | ||||||
| BCIAo pre-DAV | 0,65 | 0,27-1,56 | 0,33 | ||||||
| Asistencia biventricular | 0,64 | 0,23-1,76 | 0,38 | ||||||
| Cambio de cánulas del DAV | 0,49 | 0,15-1,69 | 0,26 | ||||||
| Duración de la asistencia | 0,98 | 0,97-1,01 | 0,70 | ||||||
| Transfusiones durante la asistencia | |||||||||
| Concentrados hematíes | 0,96 | 0,91-1,01 | 0,18 | 0,98 | 0,93-1,03 | 0,48 | |||
| Plasma | 1,07 | 0,95-1,21 | 0,23 | ||||||
| Plaquetas | 0,99 | 0,84-1,17 | 0,93 | ||||||
| Suma de unidades transfundidas | 0,99 | 0,95-1,02 | 0,45 | ||||||
| Reintervención por hemorragia | 1,1 | 0,45-2,64 | 0,82 | ||||||
| Infección durante la asistencia | 0,30 | 0,12-0,72 | 0,007 | 0,32 | 0,13-0,76 | 0,01 | 0,31 | 0,13-0,75 | 0,007 |
| Sensibilización | 3,91 | 1,54-9,89 | 0,004 | 3,64 | 1,42-9,33 | 0,007 | 3,69 | 1,44-9,45 | 0,009 |
| Inducción | 0,08 | ||||||||
| No | 1 | ||||||||
| Basiliximab | 0,54 | 0,20-1,50 | 0,24 | ||||||
| Timoglobulina | 1,99 | 0,65-6,12 | 0,23 | ||||||
BCIAo: balón de contrapulsación intraaórtico; DAV: dispositivo de asistencia ventricular; ECMO: oxigenador extracorpóreo de membrana; HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Modelo 1 incluye estado de sensibilización e infección durante la asistencia.
Modelo 2 incluye las variables del modelo 1 más sexo, diabetes, cambio de cánulas del dispositivo de asistencia y suma total de las unidades de productos hemáticos transfundidos.
La variable Inducción no se introduce en los modelos multivariables por su alta correlación con la variable sensibilización.
Los resultados del presente estudio muestran que el desarrollo de anticuerpos anti-HLA durante la asistencia con DAVC como puente al trasplante es posible, lo que afecta a un 12% de los pacientes. Esto se aprecia sobre todo en mujeres y conlleva un impacto pronóstico, fundamentalmente en la incidencia de RA tras el trasplante.
La sensibilización durante la asistencia es una complicación ampliamente estudiada en los DAVL, y se han comunicado incidencias muy variables en los distintos trabajos dependiendo de la definición de sensibilización y del tipo de estudio9. Esta complicación supone un desafío clínico cuando el dispositivo se implanta como puente al trasplante, tanto por las complicaciones asociadas con el desarrollo de anticuerpos como por los efectos secundarios que acarrea el tratamiento desensibilizante (infecciones, insuficiencia renal, coagulopatía, enfermedades linfoproliferativas)10. En estudios previos se ha definido la sensibilización como un PRAc >10%, y se considera muy sensibilizados a los pacientes con un PRAc >50-90%, según el estudio1,6.
Parece que los DAVL aumentan la incidencia de sensibilización por la interacción entre el biomaterial implantado y el sistema inmunitario del receptor y la mayor necesidad de transfusiones en estos pacientes. Esto da lugar a un incremento en la respuesta inmunológica e inflamatoria11. Se ha propuesto que el tipo de dispositivo podría influir en la frecuencia de sensibilización, más frecuente con dispositivos de flujo pulsátil, como resultado de un estímulo constante de la activación linfocitaria (requieren válvulas biológicas y una mayor superficie de contacto con la sangre)11. Otros factores asociados con la sensibilización de estos pacientes son el antecedente de embarazos, la transfusión de hemoderivados, la sensibilización antes de la asistencia, la edad joven y la cirugía cardiaca previa6. En el presente estudio, en los pacientes con un único tipo de DAVC (CentriMag), el sexo femenino fue el único factor que mostró una relación estadísticamente significativa con la sensibilización durante la asistencia, lo que se podría explicar por la aloinmunización durante embarazos previos. Por otro lado, se observó una mayor incidencia de anticuerpos anti-HLA en los pacientes con asistencia más larga, que podría haber alcanzado la significación estadística con un mayor tamaño muestral. La transfusión de hemoderivados, que generalmente se considera un evento sensibilizante, no fue en nuestro caso un predictor independiente de la sensibilización. Esto podría estar en relación con el uso de productos sanguíneos leucodeplecionados, habitualmente realizado en nuestro centro. Otros factores como la edad, la cirugía cardiaca previa y las reintervenciones quirúrgicas no mostraron una asociación estadísticamente significativa con la sensibilización.
El desarrollo de anticuerpos anti-HLA se ha relacionado con un peor pronóstico tras el trasplante en términos de RA, enfermedad vascular del injerto y mortalidad de manera más o menos coincidente, aparte del resultado de las pruebas cruzadas. Nwakanma et al.2 demostraron en 8.160 receptores sensibilizados la asociación estadísticamente significativa de un PRA >25% con la reducción en la supervivencia y con un aumento en la tasa de rechazo. Sin embargo, la mayor parte de los estudios no han conseguido relacionar la sensibilización durante la asistencia con una peor evolución tras el trasplante1,7. En el estudio publicado por Alba et al.1, la sensibilización durante la asistencia no se tradujo en un peor pronóstico tras el trasplante en cuanto a episodios de rechazo o mortalidad. Esto se podría explicar por protocolos de inmunosupresión más agresivos y una monitorización más estrecha del rechazo en estos pacientes. Por otro lado, se asoció con una menor probabilidad de trasplante y mayores tiempos de espera. A diferencia del estudio publicado por Alba et al.1, en los pacientes incluidos en nuestro estudio no se realizaron las pruebas cruzadas virtuales. Hay que destacar que el estudio de Alba et al.1 incluye a pacientes trasplantados con dispositivos de asistencia circulatoria de larga duración en lista no urgente, sin restricciones temporales a la hora de encontrar un donante histocompatible. Esta situación es completamente diferente de la planteada en nuestro estudio, cuyos pacientes se someten a trasplante en situación de urgencia 0 con dispositivos de asistencia circulatoria homologados para 30 días, lo que supone un factor limitante en el tiempo a la hora de encontrar un donante histocompatible. Por otro lado, la importancia de limitar el tiempo de isquemia en el TxC implica que en muchas ocasiones en nuestro entorno no se disponga de información con respecto a la tipificación de HLA del donante.
Sin embargo, de los 11 pacientes sensibilizados, los 3 fallecidos tras el trasplante se encontraban altamente sensibilizados. En estos casos, a pesar de los factores limitantes descritos, la realización del cross-match virtual prospectivo habría permitido la selección de donantes con HLA compatibles, lo que habría permitido probablemente mejorar el pronóstico de estos pacientes.
El presente estudio, hasta donde sabemos, analiza por primera vez la sensibilización durante la asistencia en una cohorte de pacientes con DAVC de tipo CentriMag como puente al trasplante y su impacto pronóstico. En este caso, se observó un mayor riesgo de un primer episodio de rechazo en los pacientes sensibilizados, significativamente superior al de los no sensibilizados. Hubo una tendencia a la asociación con la mortalidad que, aunque no alcanzó la significación estadística, podría tener relevancia clínica. La infección se mostró como factor protector contra el RA. Es conocido que una mayor frecuencia de infecciones es un marcador de inmunidad disminuida. Tests como el ImmuKnow son una herramienta adicional que podría ayudar a identificar a los pacientes con mayor riesgo de infección o rechazo. Estas pruebas no se realizan en la práctica clínica habitual y no se encuentran disponibles en nuestro laboratorio.
En los pacientes trasplantados, se determinaron los anticuerpos anti-HLA antes del implante de la asistencia en los casos de implante electivo 2 semanas tras un evento sensibilizante (si no se los trasplantaba antes) y antes del TxC mediante tecnología Luminex. El tratamiento de los pacientes sensibilizados se basó en inducción con anticuerpos antitimocito inmediatamente tras el trasplante en el 91% de los pacientes y tratamiento desensibilizante pretrasplante con plasmaféresis y rituximab en 3 pacientes (27,3%) con valores elevados de PRAc (> 25%). Para otros 3 pacientes muy sensibilizados se descartó la desensibilización por un balance riesgo-beneficio desfavorable.
El tratamiento de la sensibilización durante la asistencia no se encuentra estandarizado y la estrategia ideal de desensibilización está todavía por definir6,10. La mayor parte del conocimiento en este campo se basa en estudios observacionales con pequeño tamaño muestral12. La detección por ensayos de fase sólida (Luminex) es el método de referencia por ser el más sensible, específico y reproducible para la determinación de anticuerpos anti-HLA. Pruebas adicionales, como el test de fijación de complemento, pueden ser útiles para ayudar a determinar su relevancia clínica, pues se ha correlacionado la capacidad de fijación de complemento con el RA precoz13. Sin embargo, esta técnica aún no está estandarizada en la mayor parte de los laboratorios. Otro factor que puede mediar el impacto pronóstico de la sensibilización está en el carácter específico del donante de los anticuerpos desarrollados. En nuestro estudio, el 91% de los pacientes tuvieron pruebas cruzadas negativas, lo que podría indicar que los anticuerpos detectados eran en su mayoría no específicos del donante o que la terapia de desensibilización los hubiera aclarado. No obstante, el riesgo de RA se ha visto incrementado incluso en pacientes sin anticuerpos específicos del donante2. Estudios previos indican que la presencia de anticuerpos dirigidos contra antígenos no HLA podría tener un papel en el RA mediado por anticuerpos. Esto queda recogido en el documento de consenso de la International Society of Heart and Lung Transplantation (ISHLT): The management of antibodies in heart transplantation: An ISHLT consensus document, aunque se necesitan más estudios para determinar su relevancia clínica14,15.
Las terapias de desensibilización se suelen aplicar cuando el PRAc es >25-50%2,10, lo que concuerda con la actitud terapéutica en esta cohorte. El algoritmo publicado en el documento de consenso de la Sociedad Americana de Cardiología recomienda no desensibilizar ni monitorizar anticuerpos si el PRAc es< 20%. Se recomienda la monitorización de anticuerpos y de rechazo si el PRAc está en un 20-50% y considerar la desensibilización con un PRAc ≥ 50%, aunque no hacen recomendaciones específicas para pacientes con DAVC como puente al trasplante6.
Los pacientes hipersensibilizados son buenos candidatos para la terapia de desensibilización, que se basa en 2 pilares: eliminación de los anticuerpos circulantes mediante técnicas de depuración extracorpórea como la plasmaféresis o la inmunoadsorción y disminución de la producción de anticuerpos de novo por los linfocitos B con fármacos como el rituximab. La combinación de ambas estrategias disminuye la cantidad de anticuerpos de manera efectiva y podría mejorar el pronóstico tras el trasplante10. La estrategia específica depende en gran medida del centro trasplantador y de un balance riesgo-beneficio individualizado. En este sentido, hay que tener en cuenta el riesgo particularmente elevado de complicaciones hemorrágicas y trombóticas, así como la mayor vulnerabilidad a la infección en la situación clínica planteada, que condiciona el umbral de PRAc a la hora de plantear dichas terapias y la elección de la estrategia desensibilizante.
LimitacionesEl presente es un estudio observacional retrospectivo, con todas las limitaciones inherentes a este tipo de diseños, fundamentalmente la posibilidad de sesgos ocultos. El tamaño muestral y el número de eventos son muy pequeños, lo que afecta a la potencia estadística. Esto puede ser especialmente relevante en nuestro caso respecto a los resultados de mortalidad tras el trasplante.
En cuanto al tiempo de exposición a la asistencia, en principio, resulta intuitivo aceptar que, a mayor tiempo de asistencia, mayor riesgo de sensibilización. Sin embargo, podría haber también en esta asociación un componente espurio, ya que los pacientes sensibilizados pueden ver pospuesto el trasplante hasta la valoración del resultado de la desensibilización.
En nuestro centro se aplica una estrategia de seguimiento periódico clínico-ecocardiográfico para la monitorización del rechazo, sin la realización sistemática de biopsia endomiocárdica, que solo se lleva a cabo en caso de dudas o eventos clínicos sospechosos. La falta de evidencia histopatológica en el diagnóstico del rechazo en parte de los pacientes es otra de las limitaciones de nuestro estudio.
Por otro lado, el grado de sensibilización representado por el PRAc puede ser variable, dado que su valor depende de la composición del panel de anticuerpos y la técnica utilizada para su detección.
Sin embargo, los resultados reflejan la práctica clínica en un grupo de TxC en los últimos 10 años, y se centra por primera vez en la actitud terapéutica y el pronóstico de los pacientes sensibilizados durante la asistencia con DAVC.
CONCLUSIONESLa sensibilización durante la asistencia circulatoria con dispositivos de corta duración afecta a alrededor del 12% de los pacientes, ocurre fundamentalmente en mujeres y puede repercutir en los resultados del TxC, sobre todo en mayor riesgo de RA tras el trasplante y con una tendencia no significativa a mayor mortalidad.
- –
Los DAVL se asocian con un incremento en la producción de anticuerpos anti-HLA, por su propia inmunogenicidad y el mayor número de transfusiones en estos pacientes, que son factores de riesgo de sensibilización bien establecidos. Esta se puede asociar con una peor evolución tras el trasplante, en términos de RA, enfermedad vascular del injerto y mortalidad.
- –
Sin embargo, no existen estudios que analicen la sensibilización durante la asistencia con DAVC y su impacto pronóstico.
- –
Se trata del primer estudio que analiza la sensibilización durante la asistencia con DAVC.
- –
Se observó que el desarrollo de anticuerpos anti-HLA en esta situación es posible, ocurre fundamentalmente en mujeres y se asocia significativamente con un mayor riesgo de RA.
- –
Se aportan datos sobre la actitud diagnóstico-terapéutica en la sensibilización durante la asistencia con DAVC en un grupo de TxC.
Ningún autor tiene conflictos de intereses.