El estudio SAFEHEART se diseñó para analizar la situación y mejorar el conocimiento de la hipercolesterolemia familiar heterocigota (HFH) en España. Nuestro objetivo es determinar la tasa de incidencia de eventos cardiovasculares, el riesgo estimado de sufrir un evento y su modificación, el empleo de tratamiento hipolipemiante y la consecución de objetivos de colesterol unido a lipoproteínas de baja densidad en pacientes con HFH.
MétodosEl SAFEHEART es un estudio prospectivo de cohorte, abierto, multicéntrico, de escala nacional, con seguimiento protocolizado a largo plazo en una población de HFH caracterizada molecularmente. Se analizó a los pacientes mayores de 18 años con seguimiento completo.
ResultadosEl análisis en este estudio se hizo con 2.648 pacientes con HFH. La mediana de seguimiento fue de 6,6 (4,8-9,7) años. La tasa de incidencia general de eventos cardiovasculares fue de 1,3 eventos/100 pacientes-año. El riesgo estimado de sufrir un evento cardiovascular a 10 años se redujo en el seguimiento, y pasó del 1,6 al 1,3% (p <0,001). En el último seguimiento, el 20,6 y el 22,2% de los pacientes en prevención primaria y secundaria consiguieron un colesterol unido a lipoproteínas de baja densidad <100 y <70 mg/dl respectivamente.
ConclusionesEn este estudio se muestra la tasa de incidencia de eventos cardiovasculares, el riesgo estimado de sufrir un evento cardiovascular en la mayor población de pacientes con HF en España, así como su modificación, la consecución de objetivos en colesterol unido a lipoproteínas de baja densidad y su tratamiento. Aunque el riesgo cardiovascular de la HFH es elevado, un adecuado tratamiento reduce la probabilidad de sufrir un evento.
Estudio registrado en ClinicalTrials.gov (Identificador: NCT02693548).
Palabras clave
La hipercolesterolemia familiar heterocigota (HFH) es un trastorno autosómico codominante con una prevalencia de aproximadamente 1/300 casos en la población general1. Es el trastorno genético más frecuente asociado con enfermedad cardiovascular ateroesclerótica (ECVA) prematura. Aunque el tratamiento hipolipemiante (THL) ha mostrado reducción en la mortalidad coronaria y total en la HFH2, y el THL ha mejorado en los últimos años, la mayoría de los pacientes con HFH no alcanzan un nivel terapéutico óptimo de colesterol unido a lipoproteínas de baja densidad (cLDL)3,4 y, por lo tanto, siguen teniendo un elevado riesgo de aparición prematura de ECVA. Sin embargo, no todos los pacientes con HFH tienen el mismo riesgo de sufrir un evento cardiovascular. Recientemente, hemos publicado una ecuación que permite definir el riesgo de un determinado individuo con HFH basada en 8 sencillas variables5. Entre ellas, hay que destacar el papel que desempeña la lipoproteína (a) —Lp(a)— en la predicción de ECVA incidente en pacientes con HFH6.
La última guía de hiperlipemias de la Sociedad Europea de Cardiología7 considera a los pacientes con HFH con alto o muy alto riesgo cardiovascular y, por lo tanto, el objetivo de cLDL debe ser <100mg/dl o <70mg/dl en pacientes sin y con antecedentes de enfermedad cardiovascular respectivamente, debiéndose en ambos casos cumplir un segundo objetivo que consiste en al menos una reducción del cLDL> 50%. Sin embargo, poco se sabe sobre el uso de THL y el logro de los objetivos de cLDL alcanzados en nuestro país. Los registros nacionales son una valiosa fuente para proporcionar esta información clave, necesaria para mejorar los modelos de atención para la salud, la educación de médicos y pacientes y ayudar a definir prioridades en guías terapéuticas y políticas de planificación de salud8. El estudio SAFEHEART (Spanish Familial Hypercholesterolemia Cohort Study), un registro nacional de pacientes con HFH, se diseñó para mejorar el conocimiento de esta enfermedad en nuestro país.
El objetivo del presente trabajo es conocer la tasa de incidencia de eventos cardiovasculares, el riesgo de sufrir un evento cardiovascular según la ecuación SAFEHEART-RE (Spanish Familial Hypercholesterolaemia Cohort Study-Risk Equation) y su modificación, el empleo de THL y la consecución de objetivos terapéuticos en pacientes con HFH en el momento de la inclusión en el registro y en su último seguimiento.
MÉTODOSDiseño del estudio y poblaciónEl SAFEHEART es un estudio prospectivo de cohorte, abierto, multicéntrico, a escala nacional, con seguimiento protocolizado a largo plazo en una población de HFH molecularmente definida y con participación de la atención primaria y la especializada9. La selección de familias con HFH comenzó en 2004. Este estudio se aprobó por el Comité Ético del Hospital Fundación Jiménez Díaz de Madrid y todos los sujetos dieron su consentimiento informado por escrito.
Los objetivos de tratamiento se definieron de acuerdo con la guía de hiperlipemias7. Estas pautas se utilizaron para informar, educar y capacitar a los médicos participantes e incluir a los pacientes y las familias en este registro. La asignación de pacientes a una determinada comunidad autónoma se hizo según cuál fuera su residencia habitual y no por su lugar de nacimiento.
SeguimientoEl centro coordinador del estudio SAFEHEART gestionó el seguimiento de los pacientes. Se contactó con los pacientes cada año mediante una encuesta telefónica estandarizada para registrar cambios relevantes en los hábitos de vida, medicación y aparición de eventos cardiovasculares9. En todos los pacientes, el seguimiento más reciente se realizó en los 12 meses previos al análisis. Se definió seguimiento completo como aquel realizado a un paciente contactado por última vez en los 12 meses previos al análisis y que ha aportado todos los datos requeridos por el formulario estandarizado de seguimiento anual. Las definiciones de ECVA previa e incidente se han publicado previamente5. Siempre que al hacer el seguimiento anual se detecta algún evento o los pacientes o familiares de los pacientes contactan para informar que ha existido un evento, se analizan los informes médico-legales necesarios por parte del Comité de eventos del registro y los eventos son catalogados de una forma estandarizada.
Variables clínicas y de laboratorioAdemás de las variables demográficas y clínicas mencionadas, se incluyeron la edad, los factores de riesgo cardiovascular clásicos, el examen físico y el THL9. Las concentraciones del perfil lipídico y de Lp(a) se determinaron en muestras de sangre venosa en un laboratorio centralizado9. La concentración sérica de cLDL se calculó utilizando la fórmula de Friedewald. El ADN se aisló de la sangre completa utilizando métodos estándar y el diagnóstico genético de HFH se realizó como se ha descrito previamente10. El riesgo cardiovascular se definió mediante la ecuación de cálculo de riesgo SAFEHEART-RE5. La clasificación de la intensidad del THL se ha publicado previamente5, pero en el presente trabajo, el empleo de inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (iPCSK9) se incluye dentro del THL máximo.
Análisis estadísticoEl análisis estadístico se realizó utilizando la versión 18.0 del programa SPSS. Los datos cuantitativos se expresan como mediana [intervalo intercuartílico], excepto en el análisis desglosado por comunidades autónomas (CCAA), en el que solo se muestra la mediana. Los riesgos estimados y sus modificaciones se muestran como media tras comprobar su ajuste a una distribución normal. Los datos cualitativos se muestran como número absoluto y porcentaje, excepto en el análisis desglosado por CCAA, en el que solo se muestra el porcentaje. La tasa de incidencia de eventos cardiovasculares se calculó como el cociente en el que el numerador es el número de eventos observados y el denominador es el tiempo en riesgo para el evento. El tiempo en riesgo es la suma del tiempo de seguimiento de los pacientes que no tienen evento más la suma del tiempo hasta que aparece el evento en los pacientes en que se produce el evento. La tasa de incidencia se expresó como número de eventos cada 100 pacientes-año. Solo se consideró el primer evento, fuera mortal o no mortal. Se empleó el test de McNemar para comparación de pares de proporciones, el test de Wilcoxon para comparación de pares de variables cuantitativas, la prueba binomial para comparar la proporción observada en cada comunidad autónoma con el valor de la población total y la prueba de Wilcoxon de los rangos con signo para una muestra para comparar la mediana de las variables de cada comunidad con la de la población total. Se consideró significativa una diferencia con p <0,05.
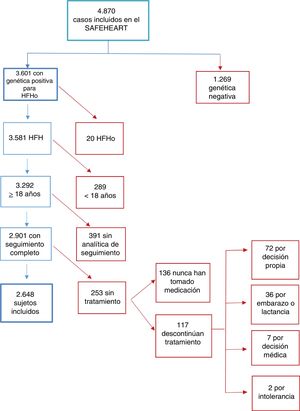
RESULTADOSSe reclutó a 4.870 sujetos, 3.601 con diagnóstico genético de HFH y 1.269 familiares no afectos. El análisis en este estudio se hizo con 2.648 pacientes con HFH, después de excluir a los sujetos sin un seguimiento completo y a los que no recibían THL en el último seguimiento (figura 1). La mediana de seguimiento fue de 6,6 [4,8-9,7] años. Las características principales de la cohorte a la inclusión y en el último seguimiento se describen en la tabla 1 y la tabla 2. La tabla 1 del material adicional muestra la distribución de pacientes según su comunidad autónoma de residencia. Como se puede observar, hay pacientes de todas las CCAA excepto de Cantabria, Región de Murcia y Comunidad Foral de Navarra y de las ciudades autónomas de Ceuta y Melilla.
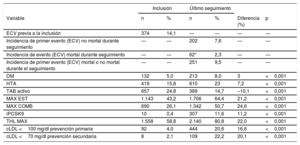
Características de la población. Variables binarias
| Inclusión | Último seguimiento | |||||
|---|---|---|---|---|---|---|
| Variable | n | % | n | % | Diferencia (%) | p |
| ECV previa a la inclusión | 374 | 14,1 | — | — | — | — |
| Incidencia de primer evento (ECV) no mortal durante seguimiento | — | — | 202 | 7,6 | — | — |
| Incidencia de evento (ECV) mortal durante seguimiento | — | — | 62* | 2,3 | — | — |
| Incidencia de primer evento (ECV) mortal o no mortal durante el seguimiento | — | — | 251 | 9,5 | — | — |
| DM | 132 | 5,0 | 213 | 8,0 | 3 | <0,001 |
| HTA | 419 | 15,8 | 610 | 23 | 7,2 | <0,001 |
| TAB activo | 657 | 24,8 | 389 | 14,7 | –10,1 | <0,001 |
| MAX EST | 1.143 | 43,2 | 1.706 | 64,4 | 21,2 | <0,001 |
| MAX COMB | 690 | 26,1 | 1.342 | 50,7 | 24,6 | <0,001 |
| iPCSK9 | 10 | 0,4 | 307 | 11,6 | 11,2 | <0,001 |
| THL MAX | 1.558 | 58,8 | 2.140 | 80,8 | 22,0 | <0,001 |
| cLDL <100 mg/dl prevención primaria | 92 | 4,0 | 444 | 20,6 | 16,6 | <0,001 |
| cLDL <70 mg/dl prevención secundaria | 8 | 2,1 | 109 | 22,2 | 20,1 | <0,001 |
cLDL: colesterol unido a lipoproteínas de baja densidad; DM: diabetes mellitus; ECV: enfermedad cardiovascular; HTA: hipertensión arterial; iPCSK9: proproteína convertasa subtilisina/kexina tipo 9; MAX COMB: tratamiento máximo combinado; MAX EST: tratamiento máximo con estatinas; TAB: tabaquismo; THL MAX: tratamiento hipolipemiante máximo.
Tratamiento máximo combinado con estatinas junto con ezetimiba 10mg/día.
Tratamiento máximo con estatinas (atorvastatina 40-80mg/día o rosuvastatina 20-40mg/día).
Tratamiento hipolipemiante máximo con potencia suficiente para reducir al menos un 50% las cifras de cLDL previas al tratamiento. Simvastatina 20, 40 u 80mg/día en combinación con ezetimiba 10mg/día, pravastatina 40mg/día en combinación con ezetimiba 10mg/día, fluvastatina 80mg/día en combinación con ezetimiba 10 mg/día, atorvastatina 40 u 80mg/día con o sin combinación con ezetimiba 10 mg/día, atorvastatina 10 o 20mg/día en combinación con ezetimiba 10mg/día, rosuvastatina 20 o 40mg/día con o sin combinación con ezetimiba 10 mg/día, rosuvastatina 10 mg/día en combinación con ezetimiba 10 mg/día, pitavastatina 4 mg/día en combinación con ezetimiba 10 mg/día y empleo de iPCSK9.
De los 62 pacientes con evento mortal, 13 (21,0%) ya habían sufrido un evento no mortal durante el seguimiento.
Características de la población. Variables continuas
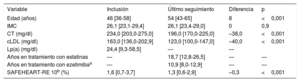
| Variable | Inclusión | Último seguimiento | Diferencia | p |
|---|---|---|---|---|
| Edad (años) | 46 [36-58] | 54 [43-65] | 8 | <0,001 |
| IMC | 26,1 [23,1-29,4] | 26,1 [23,4-29,0] | 0 | 0,9 |
| CT (mg/dl) | 234,0 [203,0-275,0] | 196,0 [170,0-225,0] | –38,0 | <0,001 |
| cLDL (mg/dl) | 163,0 [136,0-202,9] | 123,0 [100,0-147,0] | –40,0 | <0,001 |
| Lp(a) (mg/dl) | 24,4 [9,3-58,5] | — | — | |
| Años en tratamiento con estatinas | — | 18,7 [12,8-26,5] | — | — |
| Años en tratamiento con ezetimibaa | — | 10,9 [8,0-12,9] | — | — |
| SAFEHEART-RE 10b (%) | 1,6 [0,7-3,7] | 1,3 [0,6-2,9] | –0,3 | <0,001 |
cLDL: colesterol unido a lipoproteínas de baja densidad; CT: colesterol total; IMC: índice de masa corporal.
Los valores expresan mediana [intervalo intercuartílico].
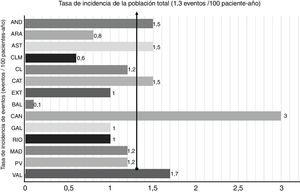
Durante el seguimiento se registraron un total de 251 primeros ECVA mortales o no mortales: 202 primeros eventos no mortales y 62 eventos mortales. Los eventos no mortales fueron: síndrome coronario agudo no mortal en 83 pacientes (3,1%), revascularización coronaria en 64 (2,4%), ictus no mortal en 23 (0,9%), revascularización periférica en 15 (0,6%) y sustitución valvular aórtica en 17 (0,6%). Los eventos mortales fueron: síndrome coronario agudo mortal en 16 pacientes (0,6%), ictus mortal en 8 (0,3%) y otro tipo de muerte cardiovascular, incluida la muerte súbita, en 38 (1,4%). De los 62 pacientes que sufrieron un evento mortal, 13 (21%) ya habían sufrido un evento no mortal durante el seguimiento. Se contactó con todos los pacientes que sufrieron eventos y/o sus familiares. De los 251 pacientes que sufrieron un evento mortal o no mortal durante el seguimiento, 114 (45,4%) habían sufrido un evento cardiovascular antes de su inclusión en el registro. La tasa de incidencia general de eventos cardiovasculares fue de 1,3 eventos/100 pacientes-año y se encuentra desglosada por CCAA de residencia en la figura 2. En cuanto al tratamiento, el 58,8% de los pacientes seguían a la inclusión un THL máximo, frente al 80,8% en el último seguimiento (p <0,001). En la inclusión había un pequeño porcentaje de pacientes tratados con iPCSK9 (el 0,4 frente al 11,6% en el último seguimiento; p <0,001). Entre los 253 pacientes que fueron excluidos por no estar tratados a fecha del último seguimiento, se registraron 5 primeros eventos no mortales y 6 eventos mortales; 2 de los pacientes que sufrieron un evento mortal ya habían sufrido un evento no mortal. Entre los 391 pacientes excluidos por no disponer de determinación de cLDL en el último seguimiento, se registraron 10 primeros eventos no mortales y 12 eventos mortales; 1 de los pacientes que sufrieron un evento mortal ya había sufrido un evento no mortal.
Tasa de incidencia de eventos cardiovasculares en función de la comunidad autónoma de residencia. AND: Andalucía; ARA: Aragón; AST: Principado de Asturias; BAL: Islas Baleares; CAN: Canarias; CAT: Cataluña; CLM: Castilla-La Mancha; CL: Castilla y León; EXT: Extremadura; GAL: Galicia; RIO: La Rioja; MAD: Comunidad de Madrid; PV: País Vasco; VAL: Comunidad Valenciana.
Respecto a la consecución de objetivos de cLDL en la inclusión, un 4,0% de los pacientes en prevención primaria conseguían un cLDL <100mg/dl y un 2,1% en prevención secundaria conseguía un cLDL <70mg/dl. En el último seguimiento, un 20,6 y un 22,2% de los pacientes en prevención primaria y secundaria respectivamente conseguían los objetivos en cLDL (p <0,001). El tabaquismo activo en la inclusión fue del 24,8 frente al 14,7% en el último seguimiento (p <0,001). No hubo diferencias en el índice de masa corporal entre la inclusión y el último seguimiento.
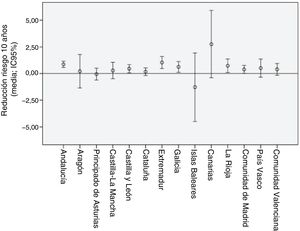
En cuanto al riesgo cardiovascular estimado mediante la SAFEHEART-RE a la inclusión y en el último seguimiento, los resultados se muestran en la figura 3. La figura muestra el cambio medio de riesgo y sus intervalos de confianza en pacientes distribuidos en función de su lugar de residencia. La tabla 2 del material adicional y la tabla 3 del material adicional muestran los resultados de las variables previamente analizadas, desglosadas por comunidad autónoma de residencia. El 37,5% de los pacientes con HFH fueron tratados en atención primaria.
DISCUSIÓNEl presente estudio describe por primera vez la tasa de incidencia de eventos cardiovasculares, el riesgo cardiovascular, el uso de THL y la consecución de objetivos terapéuticos de la HFH en España y distribuidos por CCAA de residencia. La tasa de incidencia general de eventos cardiovasculares fue de 1,3 eventos/100 pacientes-año.
El estudio muestra como el cLDL en pacientes con HFH se modifica favorablemente en los 6 años de seguimiento al intensificar el THL. La proporción de pacientes con THL máximo aumentó del 58,8 al 80,8%. Aunque en el momento del último seguimiento el 80,8% de los casos de HFH se encontraban en THL máximo y el 11,6% estaba en tratamiento con iPCSK9, solo el 20,6% de los pacientes en prevención primaria y el 22,2% en prevención secundaria alcanzaron un cLDL <100mg/dl y <70mg/dl respectivamente. En este punto, es importante destacar varios hechos: a) respecto a datos previos de este mismo registro, se ha doblado el porcentaje de pacientes que alcanzan objetivos terapéuticos3; b) un mayor porcentaje de pacientes en prevención secundaria que en prevención primaria alcanzan objetivos en cLDL, hecho que probablemente se deba a la reciente incorporación de los iPCSK9 para los pacientes en mayor riesgo, y c) aún existe un porcentaje elevado de pacientes que no alcanzan objetivos terapéuticos; una posible explicación es que los pacientes con HF parten de cifras basales de cLDL muy elevadas, por lo que se debe enfatizar en la recomendación de utilizar estatinas potentes y terapia combinada con ezetimiba e iPCSK9 en pacientes con HFH11. El presente trabajo muestra que aún existe una importante brecha entre objetivos y tratamiento empleado y, por lo tanto, una sustancial capacidad de mejora. Sin embargo, nuestros resultados también muestran la enorme dificultad que tienen estos pacientes para alcanzar los objetivos de cLDL a pesar de utilizar el mejor THL disponible. Un punto que destacar es la limitación de la potencia estadística para la comparación entre diferentes CCAA debido a las características del registro. Existe un trabajo reciente que muestra la incidencia de eventos cardiovasculares en la Comunidad Autónoma de Cataluña, con resultados superponibles a pesar de las diferencias metodológicas12.
La mejoría del riesgo estimado de sufrir un evento cardiovascular en el seguimiento probablemente se deba a la importante reducción del cLDL. Aunque aumentan la prevalencia de enfermedad cardiovascular clínica y la prevalencia de hipertensión arterial, también hay que destacar una marcada reducción del consumo de tabaco en esta población. El valor medio del índice de masa corporal es 26,1, cifra inferior a lo observado en la población adulta española: 26,7 (27,2 en varones y 26,1 en mujeres). Además, el índice de masa corporal medio no ha variado desde el momento de la inclusión, al contrario de lo observado en la población española, donde aumenta significativamente con la edad13. Estos resultados se deben en parte a que los pacientes con HFH tienen una mayor concienciación en cuanto a la prevención cardiovascular y por ello tienen mejores hábitos de vida que la población general14.
Hasta la aparición de nuevas formas de valorar el riesgo cardiovascular en pacientes con HF, las cifras de cLDL antes de THL se usaban para identificar los fenotipos graves15,16. La ecuación SAFEHEART-RE, basada en datos prospectivos, proporciona un enfoque más preciso para definir el riesgo y el manejo terapéutico más adecuado en pacientes con HFH5.
Por último, es interesante que el 37,5% de los pacientes con HFH se traten en atención primaria. Sin embargo, la variabilidad de este porcentaje en función de la comunidad autónoma de residencia es muy alta, como en Castilla y León, donde existe un plan regional de detección de la HF con la participación del médico de atención primaria17.
Somos conscientes de las fortalezas y limitaciones del presente estudio. Este trabajo es el estudio longitudinal más grande con una población con HFH definida molecularmente que refleja la práctica clínica real del tratamiento de los pacientes en los diferentes niveles asistenciales. Aunque es un registro nacional, la muestra no proviene de todas las CCAA. Estos resultados enfatizan la necesidad de un registro prospectivo para evaluar las tendencias en el cuidado de la salud cardiovascular en la HFH.
Implicaciones prácticasLa falta de programas de detección crea una barrera para la prevención eficaz de la ECVA prematura y afecta a la calidad de vida y a la carga económica y social de las familias con HFH. La detección temprana y el tratamiento de los pacientes con HFH son un desafío para los sistemas de salud y representa una necesidad médica no cubierta. Para evitar las desigualdades regionales en el cuidado de las familias con HFH es necesaria la implementación de una estrategia nacional de detección de esta enfermedad que es muy eficiente y contribuirá a mejorar su atención y a evitar la morbimortalidad cardiovascular18.
CONCLUSIONESEste estudio muestra la tasa de incidencia de eventos cardiovasculares durante el seguimiento, el riesgo de sufrir un evento cardiovascular en una amplia población de pacientes con HFH en España, su modificación, la consecución de objetivos y el manejo terapéutico de estos pacientes. Aunque el riesgo de la HFH es elevado, un adecuado tratamiento reduce considerablemente la probabilidad de sufrir un evento cardiovascular. Por lo tanto, se deben centrar los esfuerzos en lograr un adecuado control del cLDL y en mejorar los factores de riesgo de estos pacientes.
FINANCIACIÓNEste trabajo ha sido financiado por la Fundación Hipercolesterolemia Familiar; ayuda G03/181 y FIS PI12/01289 del Instituto de Salud Carlos III (ISCIII) y ayuda 08-2008 del Centro Nacional de Investigación Cardiovascular (CNIC).
CONFLICTO DE INTERESESNinguno.
- –
La hipercolesterolemia familiar heterocigota es un trastorno prevalente y se asocia frecuentemente a enfermedad cardiovascular ateroesclerótica prematura.
- –
Diferentes estudios han mostrado una reducción en la mortalidad en la hipercolesterolemia familiar debida al tratamiento hipolipemiante.
- –
Los registros nacionales son una valiosa fuente para proporcionar información clave. El estudio SAFEHEART se diseñó para mejorar el conocimiento de esta enfermedad en nuestro país.
- –
Este estudio es el primero que muestra el riesgo de sufrir un evento cardiovascular en una amplia población de pacientes con hipercolesterolemia familiar heterocigota en España, su modificación, la consecución de objetivos y el manejo terapéutico de estos pacientes.
- –
Aunque el riesgo de estos pacientes es elevado, un adecuado tratamiento reduce considerablemente la probabilidad de sufrir un evento cardiovascular.
- –
Es importante centrar los esfuerzos en lograr un control adecuado de las cifras de colesterol unido a lipoproteínas de baja densidad de estos pacientes.
Agradecemos al personal de la Fundación Hipercolesterolemia Familiar por su inestimable ayuda en el reclutamiento y seguimiento de pacientes en el registro y a todas las familias que han participado pon su inestimable colaboración.
Rocío Aguado, Begoña Perez-Corral (Hospital Universitario de León); Fátima Almagro (Hospital Donostia, San Sebastián); Rodrigo Alonso, Raquel Arroyo, Nelva Mata, Pedro Mata, Leopoldo Pérez de Isla, Adriana Saltijeral (Fundación Hipercolesterolemia Familiar); Francisco Arrieta (Hospital Ramón y Cajal, Madrid); Lina Badimón, Teresa Padró (Instituto Ciencias Cardiovasculares, IIB-Sant Pau, Barcelona); Miguel Ángel Barba (Hospital Universitario, Albacete); Ángel Brea, Daniel Mosquera, Marta Casañas (Hospital San Pedro, Logroño); Julio Carbayo (Clínica Virgen del Rosario, Albacete); Jose María Cepeda (Hospital de Vega Baja, Orihuela); Raimundo de Andrés (Fundación Jiménez Díaz, Madrid); José L. Díaz (Hospital Abente y Lago, A Coruña); Gonzalo Díaz-Soto (Hospital Clínico, Valladolid); Marta Diéguez, María Riestra (Hospital de Cabueñes, Gijón); Francisco Fuentes, José López-Miranda (Hospital Reina Sofía, Córdoba); Jesús Galiana, M. Dolores Mañas (Hospital de Ciudad Real); Jesús García-Cruces (Hospital Río Hortega, Valladolid); Juan Antonio Garrido (Hospital de Ferrol; Luis Irigoyen (Hospital Clínico Universitario Lozano Blesa, Zaragoza); Pedro L. Martínez (Hospital La Paz, Madrid); Ceferino Martínez-Faedo, Lorena Suárez (Hospital Central de Asturias, Oviedo); Marta Mauri, Rosa M. Borrallo (Hospital de Terrassa, Barcelona); Juan Diego Mediavilla, Fernando Jaén, Pablo González (Hospital Virgen de las Nieves, Granada); Alfredo Michán, Patricia Rubio (Hospital Jerez de la Frontera); Pablo Miramontes (Hospital Clínico Universitario, Salamanca); Juan L. Morera (Hospital Vital Álvarez Buylla, Mieres); Ovidio Muñiz, Aurora González (Hospital Virgen del Rocío, Sevilla); Francisca Pereyra (Hospital Universitario Nta. Sra. Candelaria, Tenerife); Leire Pérez (Hospital Universitario de Álava); Mar Piedecausa, José Pastor (Hospital Universitario de Elche); José Miguel Pinilla (Centro de Salud San Miguel de Salinas, Alicante); Xavier Pintó (Hospital de Bellvitge, Barcelona); Manuel J. Romero (Hospital Infanta Elena, Huelva); Enrique Ruiz, M. Pilar Álvarez (Hospital Universitario, Burgos); Pedro Sáenz (Hospital de Mérida); Juan F. Sánchez (Hospital San Pedro de Alcántara, Cáceres); Consuelo Sanz (Centro de Salud de Lerma-Zael); Jose I. Vidal, Rosa Argüeso (Hospital Universitario, Lugo), y Daniel Zambón (Hospital Clínic, Barcelona).
Lista completa disponible en: https://www.colesterolfamiliar.org/estudio-safeheart/centros-participantes-en-el-estudio/.