El impacto del brote de COVID-19 en el tratamiento del infarto agudo de miocardio con elevación del segmento ST (IAMCEST) no está claro. El objetivo de este estudio es evaluar los cambios en el tratamiento del IAMCEST durante el brote de COVID-19.
MétodosSe utilizó un registro multicéntrico, nacional, retrospectivo y observacional de pacientes consecutivos atendidos en 75 centros, se compararon las características de los pacientes y de los procedimientos y los resultados hospitalarios en 2 cohortes según se los hubiera tratado antes o durante la COVID-19.
ResultadosLos casos con sospecha de IAMCEST disminuyeron el 27,6% y los pacientes con IAMCEST confirmado se redujeron de 1.305 a 1.009 (22,7%). No hubo diferencias en la estrategia de reperfusión (más del 94% tratados con angioplastia primaria). El tiempo de isquemia fue más largo durante la COVID-19 (233 [150-375] frente a 200 [140-332] min; p <0,001), sin diferencias en el tiempo primer contacto médico-reperfusión. La mortalidad hospitalaria fue mayor durante la COVID-19 (el 7,5 frente al 5,1%; OR bruta=1,50; IC95%, 1,07-2,11; p <0,001); esta asociación se mantuvo tras ajustar por factores de confusión (OR ajustada=1,88; IC95%, 1,12-3,14; p=0,017). La incidencia de infección confirmada por SARS-CoV-2 fue del 6,3%.
ConclusionesEl brote de COVID-19ha implicado una disminución en el número de pacientes con IAMCEST, un aumento del tiempo entre el inicio de los síntomas y la reperfusión y un aumento en la mortalidad hospitalaria. No se han detectado cambios en la estrategia de reperfusión. La combinación de infección por SARS-CoV-2 e IAMCEST fue relativamente infrecuente.
Palabras clave
El 31 de diciembre de 2019 se notificó una agrupación de casos de neumonía de etiología desconocida en Wuhan, provincia de Hubei (China). El 9 de enero de 2020 se identificó un nuevo coronavirus, el SARS-CoV-2, como agente causal de este brote epidémico, y la enfermedad asociada a este virus se denominó enfermedad por coronavirus 2019 (COVID-19). La infección se propagó rápidamente y el 11 de marzo la Organización Mundial de la Salud declaró que la COVID-19 constituía una pandemia1. El 1 de mayo de 2020 se habían diagnosticado ya 1,6 millones de casos en 179 países de los 5 continentes, con casi 100.000 muertes confirmadas1. El 14 de marzo, el Gobierno de España activó el estado de alarma, que limitaba la movilidad de todos los ciudadanos, excepto los que trabajaban en hospitales o centros de salud y en instituciones financieras o en la venta de alimentos, productos farmacéuticos o en la cobertura de necesidades básicas2.
Las repercusiones de esta nueva enfermedad en el comportamiento de la sociedad y en el funcionamiento del sistema de asistencia sanitaria no tienen precedentes en la historia reciente. Durante el actual brote de la COVID-19, algunos estudios preliminares han resaltado una disminución del número de pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) que han sido atendidos en los hospitales de Europa y Norteamérica3–5, pero apenas se dispone de información sobre cómo el brote ha afectado a las redes de IAMCEST por lo que respecta a demora hasta la reperfusión, las estrategias de revascularización y los resultados clínicos6,7.
El objetivo de este estudio es comparar las características clínicas, el tratamiento y los resultados hospitalarios en una cohorte de ámbito nacional de pacientes con IAMCEST que fueron atendidos en los primeros 30 días siguientes al confinamiento aplicado en España durante el actual brote de COVID-19 con las de los pacientes que fueron atendidos en antes de la COVID-19.
MÉTODOSRegistro español de IAMCESTEn España existen 17 redes regionales de servicio público de asistencia del IAMCEST, que incluyen 83 hospitales con capacidad de intervención coronaria percutánea primaria (ICPp) en programas que están en funcionamiento ininterrumpido todos los días del año. En 2018, se realizaron 21.261 intervenciones por IAMCEST (el 91,6% ICPp, el 3,2% ICP de rescate y el 5,1% estrategias de ICP ordinaria temprana tras la fibrinolisis), lo cual representa 417 ICPp/millón de habitantes8.
En 2019, la Asociación de Cardiología Intervencionista de la Sociedad Española de Cardiología patrocinó un registro prospectivo de pacientes consecutivos con IAMCEST que fueron tratados en estas redes de asistencia al IAMCEST. El objetivo de este Registro de Código Infarto de España es detectar las diferencias interregionales en el tratamiento del IAMCEST. Se recogió información sobre el número de casos, las características clínicas, el tratamiento clínico y los resultados obtenidos en los pacientes con IAMCEST. Entre abril y junio de 2019, se incluyó en este registró a 5.240 pacientes consecutivos.
Durante el brote actual de COVID-19, la Asociación de Cardiología Intervencionista puso en marcha un registro paralelo, con una recogida retrospectiva de información de todos los pacientes consecutivos con IAMCEST de los mismos centros que participaban en el registro en 2019. Se registró retrospectivamente información sobre el número de casos, las características clínicas, el tratamiento y los resultados obtenidos a partir del 16 de marzo, es decir, inmediatamente después de la activación en España del estado de alarma y el confinamiento en todo el país.
El protocolo de investigación fue aprobado por el Grupo de Trabajo sobre Código IAMCEST de la Asociación de Cardiología Intervencionista y por un comité de ética central de las Áreas Sanitarias de León y El Bierzo.
Diseño del estudioSe trata de un estudio de cohortes, observacional, multicéntrico y retrospectivo, en el que se han evaluado las intervenciones registradas en la base de datos del Registro Código Infarto de España para determinar si el brote actual de COVID-19ha tenido alguna repercusión de interés en el tratamiento del IAMCEST en cuantoa número de casos, características clínicas, demora hasta la reperfusión, tratamiento hospitalario y resultados clínicos hospitalarios. Se establecieron 2 cohortes de pacientes en función de que se hubieran tratado entre el 1 y el 30 de abril de 2019 (cohorte previa a la COVID-19) o entre el 16 de marzo y el 14 de abril de 2020 (cohorte durante la COVID-19). El análisis incluyó datos de 75 hospitales en los que se incluyó a pacientes en los 2 periodos. Los intervalos de tiempo considerados se definieron según la guía europea pertinente9. A los pacientes con un diagnóstico final distinto del de IAMCEST no se los incluyó en el análisis final. La recogida de los datos se realizó examinando las historias clínicas. El objetivo primario fue la mortalidad hospitalaria.
Análisis estadísticoLas variables continuas se resumen mediante la media±desviación estándar, mientras que las variables cualitativas se presentan en forma de frecuencia y porcentaje. Las comparaciones de las 2 cohortes en la situación basal se realizaron con la prueba de la t de Student o la prueba de la χ2, según procediera. Las variables con una distribución muy asimétrica (es decir, los tiempos hasta el primer contacto médico, inicio de los síntomas, llegada al laboratorio de hemodinámica y reperfusión) se presentan en forma de mediana [intervalo intercuartílico] y se compararon con la prueba de la U de Mann-Whitney no paramétrica. Se elaboraron modelos de regresión logística univariantes para evaluar la asociación entre el grupo de cohorte y la mortalidad hospitalaria. Se elaboraron modelos de regresión logística multivariante para eliminar los posibles factores de confusión y evaluar la uniformidad de los resultados. Las covariables incluidas en los modelos multivariantes (tiempo del inicio de los síntomas a la reperfusión, edad, sexo, clase de Killip y resultado positivo de la prueba de reacción en cadena de la polimerasa [PCR] para la COVID-19) se eligieron en función del conocimiento médico disponible y de los resultados del análisis univariante. Se utilizaron los valores de odds ratio (OR) ajustada y sus correspondientes intervalos de confianza del 95% (IC95%) para estimar la asociación entre la cohorte y el resultado clínico.
La robustez de los resultados se evaluó mediante 2 análisis de sensibilidad: a) excluyendo a los individuos con COVID-19 de los análisis principales con objeto de tener en cuenta su posible contribución a un aumento en los resultados, y b) utilizando un modelo de regresión mixto, que incluía el hospital como variable aleatoria, lo cual permitía cierta heterogeneidad para tener en cuenta las diferencias esperadas entre los hospitales (variación interhospitalaria) ponderando según ello a cada hospital para obtener una estimación global. Los valores de p bilaterales <0,05 se consideraron estadísticamente significativos. Todos los análisis se llevaron a cabo con el programa informático STATA versión 15.1 (Stata Corp, Estados Unidos).
RESULTADOSPacientesLas redes de IAMCEST de 75 hospitales atendieron a un total de 1.113 pacientes durante el brote de COVID-19 frente los 1.538 tratados en el mismo periodo del año anterior, lo cual representa una reducción del 27,6%. En la figura 1 se muestra un diagrama de flujo de los pacientes tratados en las redes de IAMCEST en los 2 periodos de tiempo. Los pacientes con un diagnóstico confirmado de IAMCEST fueron 1.009 y 1.305 respectivamente (una disminución del 22,7%). La tendencia fue uniforme en los distintos centros (65 de los 75 centros [87%] notificaron menos eventos de IAMCEST). También hubo diferencias significativas en el número de pacientes que necesitaron asistencia de las redes de IAMCEST pero cuyo diagnóstico final fue un infarto agudo de miocardio sin elevación del segmento ST: 232 (15,1%) en 2019 frente a 104 (9,3%) en 2020 (p <0,001).
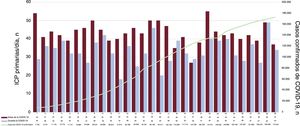
En la figura 2 se indica el número absoluto de ICPp practicadas por día en los 2 periodos de tiempo, así como el número oficial de casos confirmados según los datos del Gobierno de España7.
Número absoluto de ICP primarias/día durante los 2 periodos de tiempo y número oficial de casos de COVID-19 confirmados. El número de casos de COVID-19 confirmados procede de los datos oficiales del Gobierno de España7. ICP: intervención coronaria percutánea.
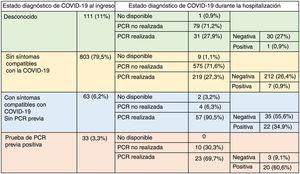
Durante el brote de COVID-19, solo 33 pacientes (3,3%) tenían diagnóstico confirmado de COVID-19 al ingreso; durante el ingreso se diagnosticó COVID-19 a otros 30 pacientes más (3,0%), con lo que hubo un total de 63 (6,3%) con diagnóstico de COVID-19. En la figura 3 se muestra la vía por la que se estableció el diagnóstico de COVID-19 en la cohorte de 2020.
Ruta diagnóstica de COVID-19. Se clasificó a los pacientes a su ingreso en 4 grupos según su estado de posible COVID-19: desconocido; ausencia de síntomas compatibles con la COVID-19 y sin prueba previa de reacción en cadena de la polimerasa (PCR); síntomas compatibles con la COVID-19 pero sin prueba de PCR previa, y resultado positivo de PCR previa. Aunque es necesario realizar una PCR al ingreso a todos los pacientes, debe señalarse que en muchos centros no se disponía de pruebas de PCR al inicio de la pandemia, cuando se llevó a cabo este estudio.
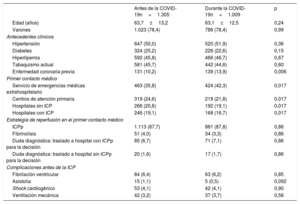
Las características clínicas basales de los pacientes se muestran en la tabla 1. Con la excepción de la enfermedad coronaria previa (más frecuente en la cohorte durante la COVID-19), las características clínicas no mostraron diferencias entre los grupos. En lo que respecta a la forma de presentación, sí se evidenciaron diferencias significativas entre los grupos: durante la COVID-19, los pacientes llegaron con más frecuencia al hospital a través del servicio de emergencias médicas extrahospitalario y, una vez en el hospital con capacidad de ICPp, fue más frecuente el ingreso directo en el laboratorio de hemodinámica.
Características clínicas basales de los pacientes con diagnóstico de IAMCEST confirmado
| Antes de la COVID-19n=1.305 | Durante la COVID-19n=1.009 | p | |
|---|---|---|---|
| Edad (años) | 63,7±13,2 | 63,1±12,5 | 0,24 |
| Varones | 1.023 (78,4) | 786 (78,4) | 0,99 |
| Antecedentes clínicos | |||
| Hipertensión | 647 (50,0) | 520 (51,9) | 0,36 |
| Diabetes | 324 (25,2) | 226 (22,6) | 0,15 |
| Hiperlipemia | 592 (45,8) | 466 (46,7) | 0,67 |
| Tabaquismo actual | 581 (45,7) | 442 (44,6) | 0,60 |
| Enfermedad coronaria previa | 131 (10,2) | 139 (13,9) | 0,006 |
| Primer contacto médico | |||
| Servicio de emergencias médicas extrahospitalario | 463 (35,8) | 424 (42,3) | 0,017 |
| Centros de atención primaria | 319 (24,6) | 219 (21,8) | 0,017 |
| Hospitales sin ICP | 266 (20,6) | 192 (19,1) | 0,017 |
| Hospitales con ICP | 246 (19,1) | 168 (16,7) | 0,017 |
| Estrategia de reperfusión en el primer contacto médico | |||
| ICPp | 1.113 (87,7) | 881 (87,8) | 0,86 |
| Fibrinolisis | 51 (4,0) | 34 (3,3) | 0,86 |
| Duda diagnóstica: traslado a hospital con ICPp para la decisión | 85 (6,7) | 71 (7,1) | 0,86 |
| Duda diagnóstica: traslado a hospital sin ICPp para la decisión | 20 (1,6) | 17 (1,7) | 0,86 |
| Complicaciones antes de la ICP | |||
| Fibrilación ventricular | 84 (6,4) | 63 (6,2) | 0,85 |
| Asistolia | 15 (1,1) | 5 (0,5) | 0,092 |
| Shock cardiogénico | 53 (4,1) | 42 (4,1) | 0,90 |
| Ventilación mecánica | 42 (3,2) | 37 (3,7) | 0,56 |
IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; ICPp: intervención coronaria percutánea primaria.
Los valores expresan n (%) o media±desviación estándar.
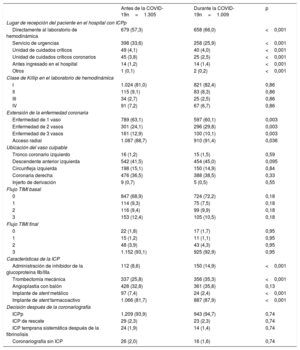
Las características angiográficas y el tratamiento aplicado se indican en la tabla 2. La vía de acceso radial fue más frecuente en la cohorte de la COVID-19 y, aunque no hubo diferencias en los flujos TIMI basal y final, en esta cohorte se observó un aumento en trombectomía mecánica y administración de un inhibidor de la glucoproteína IIb/IIIa. No hubo diferencias en la estrategia de reperfusión tras la coronariografía, de tal manera que se trató hasta al 94% de los pacientes mediante ICPp en ambas cohortes y a menos del 2% de los pacientes no se les practicó ICP.
Características angiográficas y de la intervención de los pacientes con diagnóstico de IAMCEST confirmado
| Antes de la COVID-19n=1.305 | Durante la COVID-19n=1.009 | p | |
|---|---|---|---|
| Lugar de recepción del paciente en el hospital con ICPp | |||
| Directamente al laboratorio de hemodinámica | 679 (57,3) | 658 (66,0) | <0,001 |
| Servicio de urgencias | 398 (33,6) | 258 (25,9) | <0,001 |
| Unidad de cuidados críticos | 49 (4,1) | 40 (4,0) | <0,001 |
| Unidad de cuidados críticos coronarios | 45 (3,8) | 25 (2,5) | <0,001 |
| Antes ingresado en el hospital | 14 (1,2) | 14 (1,4) | <0,001 |
| Otros | 1 (0,1) | 2 (0,2) | <0,001 |
| Clase de Killip en el laboratorio de hemodinámica | |||
| I | 1.024 (81,0) | 821 (82,4) | 0,86 |
| II | 115 (9,1) | 83 (8,3) | 0,86 |
| III | 34 (2,7) | 25 (2,5) | 0,86 |
| IV | 91 (7,2) | 67 (6,7) | 0,86 |
| Extensión de la enfermedad coronaria | |||
| Enfermedad de 1 vaso | 789 (63,1) | 597 (60,1) | 0,003 |
| Enfermedad de 2 vasos | 301 (24,1) | 296 (29,8) | 0,003 |
| Enfermedad de 3 vasos | 161 (12,9) | 100 (10,1) | 0,003 |
| Acceso radial | 1.087 (88,7) | 910 (91,4) | 0,036 |
| Ubicación del vaso culpable | |||
| Tronco coronario izquierdo | 16 (1,2) | 15 (1,5) | 0,59 |
| Descendente anterior izquierda | 542 (41,5) | 454 (45,0) | 0,095 |
| Circunfleja izquierda | 198 (15,1) | 150 (14,9) | 0,84 |
| Coronaria derecha | 476 (36,5) | 388 (38,5) | 0,33 |
| Injerto de derivación | 9 (0,7) | 5 (0,5) | 0,55 |
| Flujo TIMI basal | |||
| 0 | 847 (68,9) | 724 (72,2) | 0,18 |
| 1 | 114 (9,3) | 75 (7,5) | 0,18 |
| 2 | 116 (9,4) | 99 (9,9) | 0,18 |
| 3 | 153 (12,4) | 105 (10,5) | 0,18 |
| Flujo TIMI final | |||
| 0 | 22 (1,8) | 17 (1,7) | 0,95 |
| 1 | 15 (1,2) | 11 (1,1) | 0,95 |
| 2 | 48 (3,9) | 43 (4,3) | 0,95 |
| 3 | 1.152 (93,1) | 925 (92,9) | 0,95 |
| Características de la ICP | |||
| Administración de inhibidor de la glucoproteína IIb/IIIa | 112 (8,6) | 150 (14,9) | <0,001 |
| Trombectomía mecánica | 337 (25,8) | 356 (35,3) | <0,001 |
| Angioplastia con balón | 428 (32,8) | 361 (35,8) | 0,13 |
| Implante de stent metálico | 97 (7,4) | 24 (2,4) | <0,001 |
| Implante de stent farmacoactivo | 1.066 (81,7) | 887 (87,9) | <0,001 |
| Decisión después de la coronariografía | |||
| ICPp | 1.209 (93,9) | 943 (94,7) | 0,74 |
| ICP de rescate | 29 (2,3) | 23 (2,3) | 0,74 |
| ICP temprana sistemática después de la fibrinolisis | 24 (1,9) | 14 (1,4) | 0,74 |
| Coronariografía sin ICP | 26 (2,0) | 16 (1,6) | 0,74 |
IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; ICPp: intervención coronaria percutánea primaria; TIMI: Thrombolysis in Myocardial Infarction.
Los valores expresan n (%).
Durante el brote de COVID-19, hubo un aumento del intervalo de tiempo entre el inicio de los síntomas y el primer contacto médico (105 [45-222] frente a 71 [30-180] min; p <0,001) y del intervalo entre el inicio de los síntomas y la reperfusión (233 [150-375] frente a 200 [140-332] min; p <0,001). En cambio, no se observaron diferencias en el tiempo entre el primer contacto médico y la reperfusión (110 [80-155] frente a 110 [81-151] min; p=0,54). En la tabla 3 y la figura 4 se presentan 5 intervalos diferentes entre el inicio de los síntomas y la reperfusión.
Intervalos de tiempo entre el inicio de los síntomas y la reperfusión
| Mediana [intervalo intercuartílico] | p | |
|---|---|---|
| Del inicio de los síntomas al primer contacto médico (min) | ||
| Antes de la COVID-19 (n=1.160) | 71 [30-180] | <0,001 |
| Durante la COVID-19 (n=901) | 105 [45-222] | <0,001 |
| Del inicio de los síntomas a la reperfusión (min) | ||
| Antes de la COVID-19 (n=895) | 200 [140-332] | <0,001 |
| Durante la COVID-19 (n=895) | 233 [150-375] | <0,001 |
| Del primer contacto médico a la reperfusión (min) | ||
| Antes de la COVID-19 (n=892) | 110 [81-151] | 0,54 |
| Durante la COVID-19 (n=892) | 110 [80-155] | 0,54 |
| Del primer contacto médico a la llegada al laboratorio de hemodinámica (min) | ||
| Antes de la COVID-19 (n=1.174) | 86 [59-125] | 0,089 |
| Durante la COVID-19 (n=904) | 83 [55-125] | 0,089 |
| De la llegada al laboratorio de hemodinámica a la reperfusión (min) | ||
| Antes de la COVID-19 (n=898) | 20 [15-30] | <0,001 |
| Durante la COVID-19 (n=906) | 24 [17-31] | <0,001 |
Las diferencias observadas entre las 2 cohortes en cuanto a los resultados hospitalarios se muestran en la tabla 4. La mortalidad por cualquier causa durante la COVID-19 fue del 7,5%, en comparación con el 5,1% en el grupo del periodo previo (OR sin ajustar = 1,50; IC95%, 1,07-2,11; p <0,001). Esta asociación se mantuvo de manera uniforme tras aplicar un ajuste por la edad, el sexo, la clase de Killip y la demora entre el inicio de los síntomas y la reperfusión (OR = 1,88; IC95%, 1,12-3,14; p=0,017), pero se atenuó tras aplicar un ajuste adicional por el diagnóstico confirmado de COVID-19 (OR = 1,56; IC95%, 0,91-2,67; p=0,108).
Desenlaces hospitalarios de los pacientes con diagnóstico de IAMCEST confirmado
| Antes de la COVID-19n=1.305 | Durante la COVID-19n=1.009 | p | |
|---|---|---|---|
| Mortalidad | 67 (5,1) | 75 (7,5) | 0,019 |
| Trombosis aguda del stent | 11 (0,8) | 11 (1,1) | 0,54 |
| Hemorragia mayor | 8 (0,6) | 11 (1,1) | 0,21 |
| Shock cardiogénico después de la ICP | 75 (5,7) | 48 (4,8) | 0,29 |
| Edema pulmonar después de la ICP | 30 (2,3) | 17 (1,7) | 0,30 |
| Ventilación mecánica después de la ICP | 31 (2,4) | 19 (1,9) | 0,42 |
| Complicación mecánica | 5 (0,4) | 9 (0,9) | 0,12 |
IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea.
Los valores expresan n (%).
La robustez de nuestros resultados se evaluó mediante 2 análisis de sensibilidad. Al excluir de los análisis principales a los pacientes con COVID-19, se eliminó su posible contribución al aumento de los resultados clínicos y se confirmó que el exceso de mortalidad se explicaba en parte por la propia COVID-19: pacientes de 2020, OR = 1,28 (IC95%, 0,77-1,83; p=0,173), y continuó siendo no significativa tras un ajuste por los factores de confusión: OR = 1,56 (IC95%, 0,90-2,68; p=0,11). Al emplear modelos de efectos aleatorios, se permitió cierta heterogeneidad aleatoria entre los distintos hospitales y se obtuvo una significación estadística similar (p=0,044) para la asociación entre la mortalidad hospitalaria y los pacientes incluidos durante el brote de COVID-19 en comparación con los reclutados 1 año antes: los pacientes con un IAMCEST durante el brote de COVID-19 presentaban un mayor riesgo de mortalidad hospitalaria tras un ajuste por los factores de confusión (p=0,033), pero esta asociación significativa desaparecía al introducir en el modelo el diagnóstico de COVID-19 (p=0,203), lo cual indica que la COVID-19 es el factor que motiva el aumento de mortalidad hospitalaria en la comparación de las 2 cohortes.
DISCUSIÓNEn nuestro estudio se evaluó la influencia del brote de COVID-19 en el tratamiento de los pacientes con IAMCEST atendidos en redes de asistencia específicas de toda España, uno de los países más afectados por la actual pandemia. Se compararon los datos de un registro nacional estableciendo 2 cohortes diferentes de pacientes de 30 días: antes del brote de COVID-19 (del 1 al 30 de abril de 2019) y durante el brote (del 16 de marzo al 14 de abril de 2020).
Menos pacientes con IAMCEST y mayores demoras hasta la reperfusiónUn estudio previo de nuestro grupo había revelado una disminución del 40% de los pacientes tratados por IAMCEST durante la primera semana del actual brote3. De modo análogo, un estudio de Estados Unidos ha indicado una reducción estimada del 38% en las activaciones del laboratorio de hemodinámica por IAMCEST en 9 centros de gran volumen durante la fase inicial de la pandemia de COVID-194. Nuestros resultados confirman una disminución uniforme del número de pacientes tratados por IAMCEST (en hasta un 87% de los centros), si bien de una magnitud inferior (22,7%) a la que se creía inicialmente3. Además, hubo una disminución significativa del número de pacientes tratados en las redes de IAMCEST cuyo diagnóstico final fue distinto del IAMCEST, lo cual respalda la creencia de que los pacientes evitaron acudir a los hospitales. Por otra parte, los tiempos hasta la reperfusión fueron más largos, debido en gran parte a que los pacientes contactaron más tarde con el sistema de salud, ya que no se observaron diferencias en cuanto al tiempo entre el primer contacto médico y la reperfusión. El tiempo de isquemia es un factor determinante en el tamaño del infarto de los pacientes con IAMCEST, y la identificación rápida y la aplicación temprana del tratamiento agudo del IAMCEST son cruciales para reducir la morbilidad y la mortalidad10–12. Tiene interés señalar que la cohorte de COVID-19 mostró una prevalencia superior de antecedentes de enfermedad coronaria y tenía con más frecuencia una enfermedad multivaso, lo cual indica que los pacientes con antecedentes de cardiopatía isquémica pudieron haber sido menos reacios a acudir al hospital. A pesar de las dificultades logísticas causadas por el brote de COVID-19, no se detectó una mayor demora entre el primer contacto médico y la reperfusión, lo cual indica una buena adaptación de las redes de IAMCEST a la presente crisis. En cambio, hubo un aumento del tiempo entre la llegada al laboratorio de hemodinámica y la reperfusión, probablemente por el tiempo empleado en la aplicación de las medidas de protección necesarias para las intervenciones13.
Las posibles explicaciones de estos resultados podrían estar en una combinación de la evitación de la asistencia médica a causa del distanciamiento social y la preocupación por contraer la COVID-19 en los hospitales. El brote epidémico que se está produciendo ha sido objeto de una cobertura masiva en los medios de comunicación, en los que se ha hecho especial énfasis en las formas más frecuentes de infección y los lugares en que el SARS-CoV-2 se propaga con mayor facilidad. El temor es un bien conocido factor determinante de la evitación de la asistencia médica14 y las pandemias se han relacionado con conductas de evitación de los hospitales15.
Estrategias de reperfusión y resultados angiográficos en el IAMCEST durante el brote de COVID-19Durante el brote de COVID-19, diversas sociedades científicas han elaborado recomendaciones sobre la estrategia de reperfusión que pueden ser contradictorias en función de las condiciones existentes en cada país. En China, el Peking Union Medical College Hospital recomienda la trombolisis como tratamiento de primera línea y recomienda la intervención coronaria solo una vez descartada la COVID-19 incluso para pacientes con contraindicación para la trombolisis16. El American College of Cardiology Interventional Council y la Society for Cardiovascular Angiography & Interventions afirman que cabe considerar la fibrinolisis para los pacientes con IAMCEST y COVID-19 activa relativamente estables, con objeto de evitar la exposición de los profesionales que los atienden17. En España, no ha habido cambios en la estrategia de reperfusión, de tal manera que más del 98% de los IAMCEST han sido tratados con ICPp y no se ha producido un aumento de las trombolisis, siguiendo las recomendaciones de la Asociación de Cardiología Intervencionista de España sobre el tratamiento del IAMCEST durante el brote de COVID-1918.
Dos series pequeñas de pacientes con COVID-19 y elevación del segmento ST recientemente publicadas han mostrado una gran prevalencia de enfermedad no obstructiva19,20. En términos generales, no se observa un aumento del número de pacientes sin lesiones obstructivas. Esto podría deberse a que: a) se analizó solo a los pacientes con diagnóstico de IAMCEST confirmado, por lo que se excluyeron otras causas de infarto de miocardio con arterias coronarias sin obstrucción, como la miocarditis, el síndrome de tako-tsubo, el infarto agudo de miocardio sin elevación del segmento ST y la embolia pulmonar, que representaron alrededor de un 10% de los pacientes de nuestra serie, o b) los datos publicados anteriormente probablemente fueran de pacientes no consecutivos y muy seleccionados.
Repercusiones del brote de COVID-19 en la mortalidad relacionada con IAMCESTUna observación de especial importancia en nuestro estudio es el preocupante aumento de la mortalidad hospitalaria durante el brote de COVID-19. Este aumento se mantuvo inalterada tras aplicar un ajuste los factores edad, sexo, clase de Killip y demora entre el inicio de los síntomas y la reperfusión.
Los datos epidemiológicos recientes indican un aumento significativo de la mortalidad durante este periodo que no puede explicarse por completo por los pacientes con COVID-19 solamente21. En la actual situación, los pacientes evitan acudir a los servicios de urgencias o van más tarde, y ello podría explicar el aumento de las paradas cardiacas extrahospitalarias que se ha descrito recientemente en Italia22. Aunque resulta difícil determinar la prevalencia real de la parada cardiaca extrahospitalaria en el contexto de un IAMCEST, no se observa un aumento de los casos de fibrilación ventricular o asistolia o que requirieran ventilación mecánica antes de la llegada al laboratorio de hemodinámica de los pacientes con un IAMCEST confirmado. Se calcula que hasta un 75% de las muertes se producen antes del contacto con el sistema de salud23 y la principal forma de prevenir la parada cardiaca extrahospitalaria es que los pacientes acudan al hospital lo antes posible tras la aparición de los síntomas de IAMCEST24. Así pues, es posible que un aumento de las paradas cardiacas extrahospitalarias no se haya reflejado en nuestro estudio.
La falta de acceso al tratamiento de reperfusión también implicaría un aumento de las complicaciones subagudas del IAMCEST, como la insuficiencia cardiaca y/o el shock cardiogénico, la formación de un trombo intraventricular y embolia periférica, y las complicaciones mecánicas25. Estos pacientes no están incluidos en el presente registro, puesto que no eran candidatos a una ICPp, pero contribuyen indudablemente al exceso de mortalidad relacionada con IAMCEST.
Por último, a largo plazo, una revascularización deficiente y un mayor tamaño del infarto aumentarán las complicaciones asociadas con un peor remodelado ventricular, como la insuficiencia cardiaca crónica y las arritmias ventriculares26.
LimitacionesEste estudio tiene las limitaciones inherentes al análisis de datos observacionales de carácter multicéntrico. Cada clínico-investigador evaluó los datos basales y de seguimiento de cada centro, sin una confirmación centralizada, y ello podría producir inexactitudes y errores de clasificación. No obstante, los datos de cardiología intervencionista están bastante estandarizados en todo el mundo y se diseñó un formulario de recogida de datos electrónico que pudieran rellenar intuitivamente todos los clínicos. Además, se aplicó un modelo de regresión mixto, incluyendo el hospital como variable aleatoria, para tener en cuenta las diferencias del hospital e interhospitalarias a lo largo del tiempo. En cualquier caso, la posible variabilidad entre los clínicos aproxima nuestros resultados a los de la práctica clínica real y mejora su generalizabilidad. Se abordó cualquier posible sesgo de selección mediante un ajuste de las regresiones logísticas por los posibles factores de confusión con consecuencias pronósticas, pero podría persistir algún factor de confusión residual (medido o no medido) en el modelo multivariante.
CONCLUSIONESEste estudio observacional de ámbito nacional muestra una disminución del número de pacientes con IAMCEST tratados durante el actual brote de COVID-19, con una prolongación del tiempo entre el inicio de los síntomas y la reperfusión y un incremento de la mortalidad hospitalaria al doble. No se detectaron cambios en la estrategia de reperfusión. La concomitancia de infección por el SARS-CoV-2 con IAMCEST fue poco frecuente, pero tuvo repercusión en la mortalidad hospitalaria.
- –
Algunos estudios preliminares han resaltado una disminución del número de pacientes con IAMCEST atendidos en los hospitales durante el actual brote de COVID-19.
- –
Hay poca información sobre la influencia del brote de COVID-19 en la asistencia del IAMCEST y los resultados en este grupo de pacientes.
- –
Se observa una disminución significativa del número de pacientes con IAMCEST tratados en las redes de asistencia específica en España durante la COVID-19.
- –
En comparación con una cohorte del año anterior, los pacientes tratados durante el brote de COVID-19 tuvieron más tiempo de isquemia y un aumento de la mortalidad, aunque no hubo diferencias en la estrategia de reperfusión utilizada.
A. Pérez de Prado ha recibido pagos personales de iVascular, Boston Scientific, Terumo, B. Braun y Abbott Laboratories. Á. Cequier ha recibido pagos personales de Ferrer International, Terumo, AstraZeneca y Biotronik. Todos los demás autores han indicado no tener relaciones relevantes que declarar en relación con el contenido de este artículo.
ANEXO. INVESTIGADORES DEL GRUPO DE TRABAJO SOBRE CÓDIGO INFARTO DE LA ASOCIACIÓN DE CARDIOLOGÍA INTERVENCIONISTA
Personal clave y centros de estudio participantes
Manuel Villa, Hospital Universitario Virgen del Rocío; Rafael Ruíz-Salmerón, Hospital Universitario Virgen Macarena; Francisco Molano, Hospital Universitario Virgen de Valme; Carlos Sánchez, Hospital Universitario General de Málaga; Erika Muñoz-García, Hospital Universitario Virgen de la Victoria; Luis Íñigo, Hospital Costa del Sol; Juan Herrador, Hospital Universitario de Jaén; Antonio Gómez-Menchero, Hospital Universitario Juan Ramón Jiménez; Eduardo Molina, Hospital Universitario Virgen de las Nieves; Juan Caballero, Hospital Universitario San Cecilio; Soledad Ojeda, Hospital Universitario Reina Sofía; Mérida Cárdenas, Hospital Punta de Europa; Livia Gheorghe, Hospital Universitario Puerta del Mar; Jesús Oneto, Hospital Universitario de Jerez de la Frontera; Francisco Morales, Hospital Universitario de Puerto Real; Félix Valencia, Hospital Universitario Torrecárdenas; José Ramón Ruiz, Hospital Clínico Universitario Lozano Blesa; José Antonio Diarte, Hospital Universitario Miguel Servet; Pablo Avanzas, Hospital Universitario Central de Asturias; Juan Rondán, Hospital Universitario de Cabueñes; Vicente Peral, Hospital Universitari Son Espases; Lucía Vera Pernasetti, Policlínica Nuestra Señora del Rosario; Julio Hernández, Hospital Universitario Nuestra Señora de Candelaria; Francisco Bosa, Hospital Universitario de Canarias; Pedro Luis Martín Lorenzo, Hospital Universitario de Gran Canaria Doctor Negrín; Francisco Jiménez, Hospital Insular de Gran Canaria; José M. de la Torre Hernández, Hospital Universitario Marqués de Valdecilla de Santander; Jesús Jiménez-Mazuecos, Hospital General Universitario de Albacete; Fernando Lozano, Hospital General Universitario de Ciudad Real; José Moreu, Complejo Hospitalario de Toledo; Enrique Novo, Hospital Universitario de Guadalajara; Javier Robles, Hospital Universitario de Burgos; Javier Martín Moreiras, Hospital Universitario de Salamanca; Felipe Fernández-Vázquez, Hospital de León; Ignacio J. Amat-Santos, Hospital Clínico Universitario de Valladolid, CIBERCV; Joan Antoni Gómez-Hospital, Hospital Universitari de Bellvitge; Joan García-Picart, Hospital de la Santa Creu i Sant Pau; Bruno García del Blanco, Hospital Universitari Vall d’Hebron; Ander Regueiro, Hospital Clínic de Barcelona; Xavier Carrillo-Suárez, Hospital Universitari Germans Trias i Pujol; Helena Tizón, Hospital del Mar; Mohsen Mohandes, Hospital Universitari Joan XXIII; Juan Casanova, Hospital Universitari Arnau de Vilanova; Víctor Agudelo-Montañez, Hospital Universitari de Girona Josep Trueta; Juan Francisco Muñoz, Hospital Universitari Mútua de Terrassa; Juan Franco, Hospital Universitario Fundación Jiménez Díaz; Roberto del Castillo, Hospital Universitario Fundación Alcorcón; Pablo Salinas, Hospital Clínico San Carlos y Hospital Príncipe de Asturias; Jaime Elízaga, Hospital General Universitario Gregorio Marañón; Fernando Sarnago, Hospital Universitario 12 de Octubre; Santiago Jiménez-Valero, Hospital Universitario La Paz; Fernando Rivero, Hospital Universitario de La Princesa; Juan Francisco Oteo, Hospital Universitario Puerta de Hierro Majadahonda; Eduardo Alegría-Barrero, Hospital Universitario de Torrejón-Universidad Francisco de Vitoria; Ángel Sánchez-Recalde, Hospital Ramón y Cajal; Valeriano Ruiz, Complejo Hospitalario de Navarra; Eduardo Pinar, Hospital Virgen de la Arrixaca; Luciano Consuegra-Sánchez, Hospital Universitario Santa Lucía de Cartagena; Ana Planas, Hospital General Universitario de Castellón; Bernabé López Ledesma, Hospital Universitario y Politécnico La Fe; Alberto Berenguer, Hospital General Universitario de Valencia; Agustín Fernández-Cisnal, Hospital Clínico Universitario de Valencia; Pablo Aguar, Hospital Universitario Dr. Peset; Francisco Pomar, Hospital Universitario de la Ribera; Miguel Jerez, Hospital de Manises; Francisco Torres, Hospitales de Torrevieja-Elche-Vinalopó; Ricardo García, Hospital General Universitario de Elche; Araceli Frutos, Hospital General Universitario de San Juan de Alicante; Juan Miguel Ruiz Nodar, Hospital General Universitario de Alicante; Koldobika García, Hospital Universitario de Cruces; Roberto Sáez, Hospital de Basurto; Alfonso Torres, Hospital Universitario Araba; Miren Tellería, Hospital Universitario Donostia; Mario Sadaba, Hospital de Galdakao-Usansolo; José Ramón López Mínguez, Complejo Hospitalario Universitario de Badajoz; Juan Carlos Rama Merchán, Hospital de Mérida; Javier Portales, Complejo Hospitalario Universitario de Cáceres; Ramiro Trillo Hospital Clínico Universitario Santiago de Compostela; Guillermo Aldama, Complejo Hospitalario Universitario de A Coruña; Saleta Fernández, Complejo Hospitalario Universitario de Vigo; Melisa Santás, Hospital Universitario Lucus Augusti, y María Pilar Portero Pérez, Hospital San Pedro de Logroño.