Estamos asistiendo a un incremento en el conocimiento sobre la amiloidosis cardiaca debida al depósito anómalo de la proteína transtirretina (ATTR), tanto en su forma herediataria como en la adquirida o senil. Datos actuales en España señalan a la ATTR como la forma más frecuente de amiloidosis cardiaca. La insuficiencia cardiaca (IC) es la presentación más frecuente y cerca del 35% de los pacientes tendrán deterioro de la fracción de eyección de ventrículo izquierdo (FEVI) y corta supervivencia1. Además, un número relevante de pacientes con ATTR presenta alteraciones del sistema de conducción (el 7%, bloqueo auriculoventricular avanzado) o disfunción sistólica del ventrículo izquierdo2. Estudios previos señalan un efecto deletéreo de la estimulación ventricular frecuente y un beneficio clínico de la resincronización cardiaca (TRC) en pacientes con ATTR seleccionados3. Recientemente la estimulación fisiológica de la rama izquierda (ERI) se ha posicionado como una alternativa factible y segura para quienes requieren tratamiento antibradicárdico o TRC4. Nuestro objetivo es estudiar la viabilidad técnica de la ERI en la ATTR y analizar sus efectos clínicos en una experiencia piloto. El estudio fue aprobado por el Comité Ético de Investigación Clínica de la provincia de Granada. Se obtuvo el consentimiento por escrito de los pacientes para la realización y la publicación de este estudio.
Se presentan 3 casos con ATTR, IC y disfunción sistólica del ventrículo izquierdo con necesidad de estimulación ventricular permanente; como seguían sintomáticos, se realizó ERI con el objetivo de optimizar la TRC o prevenir el deterioro de la FEVI como consecuencia de la estimulación permanente (tabla 1).
Características basales y evolución a los 3 meses de iniciarse el tratamiento con ERI
| Paciente 1 | Paciente 2 | Paciente 3 | ||||
|---|---|---|---|---|---|---|
| Sexo | Varón | Varón | Varón | |||
| Edad (años) | 83 | 72 | 84 | |||
| Tipo ATTR | Senil | Hereditaria (p.Val142Ile) | Senil | |||
| Síndrome de túnel carpiano | + | + | - | |||
| Polineuropatía | + | + | - | |||
| Hipertensión arterial | + | + | - | |||
| Hipertensión pulmonar | - | + | - | |||
| Filtrado glomerular < 45 ml/min/1,73 m2 | + | + | + | |||
| ACV | - | - | - | |||
| FA | Permanente | Paroxística | Paroxística | |||
| Indicación | ENS | BAVc | ENS | |||
| Tratamiento | ||||||
| ISRAA | No | Enalapril | Candesartán | |||
| Bloqueadores beta | No | No | Bisoprolol | |||
| ARM | Espironolactona | No | Espironolactona | |||
| Tafamidis | No | Sí | No | |||
| Diuréticos | Furosemida 120 mg | Furosemida 120 mg | Furosemida 80 mg | |||
| iSGLT2 | No | No | No | |||
| Ritmo | FA permanente | FA permanente | FA paroxística | |||
| Dispositivo previo | TRC-P (seno coronario inferolateral basal) | No | TRC-P (seno coronario inferolateral media) | |||
| Basal | 3 meses | Basal | 3 meses | Basal | 3 meses | |
| NYHA | III | II | IV | III | III | II |
| FEVI (%) | 37 | 37 | 43 | 57 | 30 | 49 |
| QRS (ms) | 156 | 128 | 186 | 138 | 248 | 148 |
| BNP (pg/ml) | 1.513 | 1.411 | 1.469 | 1.150 | 959 | 564 |
| Visitas a urgencias de causa cardiológica (6 meses) | 2 | 1 | 2 | 0 | 1 | 0 |
| Hospitalización por IC (1 año) | 1 | 0 | 1 | 0 | 0 | 0 |
| Parámetros eléctricos relativos a estimulación en rama izquierda | ||||||
| QRSd (ms) | 128 | 138 | 148 | |||
| LVAT (ms) | 88 | 92 | 96 | |||
| Umbral de captura de rama izquierda (V × 0,4 ms) | 0,75 | 0,75 | 1 | |||
| Programación | VVIR | DDD | DDDR | |||
| Porcentaje de estimulación ventricular | 97 | 99,6 | 99,9 | |||
ACV: accidente cerebrovascular; ARM: antagonistas del receptor de mineralocorticoides; ATTR: amiloidosis por transtirretina; BAVc: bloqueo auriculoventricular completo; BNP: péptido natriurético cerebral; ENS: enfermedad del nódulo sinusal; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2; ISRAA: inhibidores del eje renina-angiotensina-aldosterona; FA: fibrilación auricular; LVAT: tiempo de activación de ventrículo izquierdo; NYHA: clase funcional de la New York Heart Association; TRC-P: terapia de resincronización cardiaca.
El primer paciente es un varón de 83 años con ATTR adquirida que sufrió un síncope por enfermedad del nódulo sinusal (ENS) y escape nodular, con hipertrofia leve de paredes y FEVI ligeramente reducida. El paciente portaba un marcapasos bicameral, y 2 años más tarde, tras el diagnóstico etiológico, el desarrollo de bloqueo auriculoventricular y el deterioro de la FEVI con necesidad de estimulación permanente, se cambió a TRC convencional. La evolución desfavorable con paso a fibrilación auricular, deterioro de la clase funcional y hospitalizaciones por IC motivó la decisión de aplicar ERI.
El segundo caso es un varón de 72 años con ATTR hereditaria (variante p.Val142Ile) y fibrilación auricular paroxística con un gran deterioro de la clase funcional por IC tras el diagnóstico de la enfermedad (1 ingreso y 2 visitas a urgencias por IC). Posteriormente presentó bloqueo auriculoventricular, y se optó por ERI con el objetivo de evitar el deterioro de la FEVI.
El tercer caso es un varón de 84 años en seguimiento por hipertrofia ventricular de etiología no aclarada desde 4 años antes del diagnóstico. Durante el seguimiento presentó fibrilación auricular persistente de difícil control, bloqueo de rama izquierda y disfunción sistólica del ventrículo izquierdo progresiva. Tras la aparición de la enfermedad del nódulo sinusal sincopal, se implantó un dispositivo de TRC (QRSd, 160 ms). Finalmente, 1 año más tarde, tras considerárselo no respondedor y con clase funcional deteriorada, se decidió la ERI, y se obtuvo un QRSd de 140ms (figura 1).
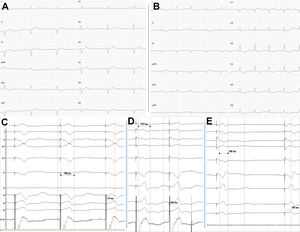
A: electrocardiograma basal con BAV de primer grado y bloqueo de rama derecha y eje izquierdo. B: ERI; típica morfología de rsr’ con eje normal. C: típica morfología de «W» en V1 antes de la penetración del electrodo en el SIV. D: penetración inicial en el SIV con acortamiento del intervalo QRS estimulado (212 ms) y del LVAT (162 ms). E: captura de rama izquierda con morfología rsr’ en V1, intervalo QRS más estrecho (148 ms) y LVAT más corto (108 ms). BAV: bloqueo auriculoventricular; ERI: estimulación de rama izquierda; SIV: septo interventricular; LVAT: tiempo de activación de ventrículo izquierdo.
En los 3 casos se usó una vaina para estimulación septal (C315 HIS, Medtronic Inc., Estados Unidos). Sobre ella se introdujo un electrodo (Select-Secure modelo 383069cm, Medtronic Inc., Estados Unidos) conectado al polígrafo para registro de señal intracavitaria. La vaina se colocó 2cm en dirección apical respecto al hisiograma y, mediante 6-8 giros en sentido horario, se penetró el electrodo en el septo interventricular hasta conseguir la captación de la rama izquierda. En los 3 casos se siguieron los siguientes 4 criterios para considerar ERI (figura 1)5:
- •
Acortamiento del intervalo espícula-onda R en V6.
- •
Morfología rsr’/rsR’en V1.
- •
Estrechamiento del complejo QRS tras penetración septal.
- •
Cambio de captura selectiva-no selectiva.
En nuestra experiencia, la tasa de éxito del implante fue del 100% y sin incidencias reseñables. En todos los casos se consiguió un QRS estimulado más estrecho que el previo.
A pesar de que los 3 pacientes presentaban una edad avanzada, fibrilación auricular (paroxística en 2 casos y permanente en 1), enfermedad renal crónica (estadio G3a) e IC avanzada (clase funcional de la New York Heart Association [NYHA] III-IV/IV), a los 3 meses del inicio de la ERI todos habían mejorado su clase funcional, con una leve disminución de la concentración de péptidos natriuréticos (tabla 1). En cuanto a la FEVI, en 2 pacientes se observó un incremento, pero no en el primero. Por último, sin que sean posibles inferencias estadísticas por el pequeño tamaño muestral, se observó una reducción del número de hospitalizaciones tras 1 año o visitas a urgencias por IC a los 6 meses de la ERI (tabla 1).
En conclusión, con las limitaciones del pequeño tamaño muestral, el carácter retrospectivo, la variabilidad de las mediciones ecocardiográficas y el corto tiempo de seguimiento, en nuestra pequeña cohorte inicial de pacientes con ATTR la ERI se mostró como una opción terapéutica viable y eficaz a corto plazo (3 meses) para la optimización de la TRC y que ofrece una mejoría de los síntomas de IC. Estudios más amplios y prospectivos deben confirmar esta hipótesis.
FINANCIACIÓNEste estudio no recibió ninguna subvención específica de organismos de financiación procedentes del sector público, comercial o sin ánimo de lucro.
CONTRIBUCIÓN DE LOS AUTORESF.J. Bermúdez-Jiménez recogió y analizó la información; escribió el manuscrito con la ayuda de los demás autores. M. Molina-Lerma y P. Sánchez-Millán realizaron y supervisaron los procedimientos técnicos. J. Jiménez-Jáimez y R. Macías-Ruiz concibieron la idea presentada. M. Álvarez supervisó todo el proceso. Todos los autores discutieron los resultados y contribuyeron al manuscrito final.
CONFLICTO DE INTERESESLos autores no tienen nada que declarar.