En pacientes con insuficiencia tricuspídea (IT), la reparación transcatéter de la válvula tricúspide (RTVT) mediante el uso de dispositivos «borde a borde» ha experimentado un creciente uso en todo el mundo. Recientemente se ha puesto a disposición un sistema dedicado de RTVT borde a borde. El presente artículo describe la experiencia inicial con este sistema en España.
MétodosEstudio multicéntrico prospectivo que incluyen los centros aceptados para el uso del novedoso sistema. Entre junio de 2020 y marzo de 2021 se incluyó a todos los pacientes sometidos a una RTVT con el sistema TriClip en España. El criterio de valoración principal fue la consecución de una reducción de la IT de al menos 1 grado al alta hospitalaria.
ResultadosSe incluyó a un total de 34 pacientes. La mayoría de ellos refería antecedentes de fibrilación auricular (91%). El objetivo primario se alcanzó en todos los pacientes. La mayoría requirieron uno (47%) o dos clips (44%), con un claro predominio del dispositivo XT (87%) sobre NT (13%). La localización del primer clip fue principalmente anteroseptal (> 90%). Solo un paciente presentó un desprendimiento parcial que pudo ser estabilizado con clips adicionales en el mismo procedimiento. Al alta, la gravedad de la IT fue de grado 2 en el 91% de los pacientes. A los 3 meses, no se detectó ninguna muerte. Al seguimiento, el 88% de los pacientes se encontraban en clase funcional New York Heart Association 2 y el 80% presentaban IT grado 2 residual.
ConclusionesLa RTVT borde a borde pareció ser eficaz y segura con una reducción sostenida de la IT a los 3 meses. Serán necesarios más estudios para confirmar estos resultados.
Palabras clave
La insuficiencia tricuspídea (IT) es una valvulopatía frecuente que está directamente relacionada con el aumento de la morbilidad y la mortalidad1,2. En general, los síntomas insidiosos y fluctuantes de la IT se traducen en retrasos sustanciales en la aplicación de estrategias correctoras invasivas3. Estos retrasos suelen tener repercusiones en una mayor comorbilidad en el momento de la corrección y, por consiguiente, una alta tasa de mortalidad, de hasta un 10% con las intervenciones quirúrgicas aisladas4,5. Las intervenciones percutáneas de la tricúspide vienen ofreciendo alternativas a la cirugía convencional para los pacientes en alto riesgo6,7. De entre ellas, la reparación percutánea de la válvula tricúspide (RPVT) borde a borde es la estrategia con mayor penetración en el mundo7. Al principio se propuso el empleo compasivo de dispositivos MitraClip (Abbott Medical, Estados Unidos) en posición tricuspídea, con unos resultados prometedores7,8. No obstante, las dificultades para alcanzar una altura adecuada del catéter o una coaxialidad óptima constituyeron limitaciones importantes para el uso del sistema mitral convencional9. El ensayo TRILUMINATE Pivotal fue el primero que evaluó los resultados de un sistema de RPVT borde a borde específico para este fin, denominado TriClip (Abbott Medical)10,11. A pesar de que se usaron únicamente dispositivos NT (de brazos cortos), el sistema TriClip mostró un elevado porcentaje de éxito de la intervención, con una incidencia de complicaciones muy baja. A 1 año, la IT se redujo a un grado moderado o menor en el 71% de los participantes y la mayoría (83%) estaban en clase funcional de la New York Heart Association (NYHA) ≤ II11. El nuevo sistema TriClip se comercializó en Europa en junio de 2020 en 2 tamaños: XT y NT. Este artículo describe la experiencia inicial con el sistema en España.
MÉTODOSDiseño y población del estudioSe hizo un análisis retrospectivo multicéntrico con los datos individuales de 4 centros de España con acceso inicial a la distribución limitada del sistema TriClip comercializado para la RPVT borde a borde en la IT sintomática. Se obtuvieron prospectivamente los datos relativos a parámetros demográficos, características iniciales y de la intervención y resultados clínicos y ecocardiográficos en el seguimiento para elaborar una base de datos común prospectiva y específica para este fin en cada uno de los centros participantes. Un equipo formado por cardiólogos intervencionistas, especialistas en insuficiencia cardiaca, cardiólogos expertos en exploraciones de imagen y cirujanos cardiacos evaluó a los pacientes. Todas las intervenciones se llevaron a cabo con anestesia general y guiados por ecocardiografía transesofágica y fluoroscopia. Se registraron las complicaciones periintervención durante la hospitalización de calificación para el estudio («índice»). El estudio se llevó a cabo de acuerdo con lo indicado por el comité de ética de investigación de cada centro participante y todos los pacientes firmaron su consentimiento informado para la intervención.
Objetivos del estudio y definicionesSe utilizaron definiciones estandarizadas de todas las variables relacionadas con los pacientes, los diagnósticos clínicos, las complicaciones hospitalarias y los criterios de valoración utilizados. La IT se evaluó con métodos estándares de Doppler color bidimensional y se usó una clasificación en 5 grados: leve, moderada, grave, masiva o torrencial12. Las brechas de coaptación se evaluaron en la proyección transgástrica de eje corto. El éxito del implante se definió como la aplicación e implante satisfactorios como mínimo de 1 clip y que se lograra la aproximación de los velos tratados y la retirada del catéter de implante. El objetivo principal fue una reducción de la IT ≥ 1 grado, evaluada mediante una ecocardiografía transtorácica al alta. Los eventos adversos mayores en la intervención y durante la hospitalización fueron muerte, taponamiento cardiaco, cirugía de urgencia inmediata, complicaciones vasculares, hemorragia mayor, ictus e infarto de miocardio. Se llevó a cabo un seguimiento clínico y ecocardiográfico a los 3 meses. El estado clínico se evaluó con la clase funcional de la NYHA.
Análisis estadísticoLas variables cualitativas se presentan mediante frecuencias (porcentajes) y las diferencias se evalúan mediante la prueba de la χ2 o la prueba de Fisher en caso necesario. Las variables continuas se presentan en forma de media ± desviación estándar o mediana [intervalo intercuartílico]. Se aplicó la prueba de Kolmogorov-Smirnov para verificar la normalidad de la distribución. Se utilizaron pruebas de la t para datos emparejados para el análisis de los cambios observados en las variables continuas entre la situación inicial y las visitas de seguimiento y se aplicó la prueba de Friedman para los datos nominales emparejados. El seguimiento se consideró finalizado en la fecha de la última visita de seguimiento. Los análisis se llevaron a cabo con el programa informático STATA (V 14.0, StataCorp LP, Estados Unidos).
RESULTADOSEntre junio de 2020 y marzo de 2021, se trató mediante RPVT borde a borde con el sistema TriClip a un total de 34 pacientes. Las características basales de los pacientes se muestran en la tabla 1. Es de destacar que la mayoría de los pacientes referían antecedentes de fibrilación auricular y que solo 1 era portador de un marcapasos permanente. La ecocardiografía reveló una IT grave (47%) o masiva (44%) e IT funcional como mecanismo subyacente (79%) en la mayoría de los pacientes (tabla 2). Además, la mayoría de los chorros de IT eran centrales (91%) y estaban situados en la línea anteroseptal de la coaptación de la válvula (59%). Tenían una insuficiencia mitral mayor que moderada 2 pacientes: en 1 se llevó a cabo simultáneamente la reparación percutánea de la válvula mitral, y en el otro la válvula mitral no era apta para la reparación percutánea. Ninguno de los pacientes tenían hipertensión pulmonar.
Características clínicas basales
| Variable | n=34 |
|---|---|
| Edad (años) | 75,5 [69-79] |
| Mujeres | 25 (74) |
| IMC | 26,8±4,86 |
| Hipertensión | 19 (56) |
| Diabetes mellitus | 7 (20) |
| Fibrilación auricular | 31 (91) |
| EPOC | 5 (15) |
| EC | 2 (6) |
| Ictus/AIT | 6 (18) |
| ERC | 14 (41) |
| TFGe (ml/min) | 57,8±21,7 |
| MPP/DAI | 1 (3) |
| Cirugía valvular previa | |
| Mitral | 9 (27) |
| Tricúspide | 1 (3) [Anuloplastia de DeVega] |
| MitraClip previo | 2 (6) |
| EuroSCORE II | 4,04 [2,31-5,68] |
| STS | 3,73 [2,76-5,44] |
| NYHA | |
| I | 0 |
| II | 8 (24) |
| III | 22 (67) |
| IV | 3 (9) |
| Edema periférico | 29 (85) |
| Ascitis | 15 (44) |
| Tratamiento médico | |
| Bloqueadores beta | 16 (47) |
| IECA/ARA-II | 12 (34) |
| Antagonistas de la aldosterona | 19 (56) |
| Sacubitrilo-valsartán | 0 |
| AVK | 25 (74) |
| NACO | 4 (12) |
| Nitratos | 1 (3) |
| Hidralazina | 1 (3) |
| Furosemida | 31 (92) |
| Dosis diaria media (mg/día) | 60±7,23 |
| Tiacida | 10 (29) |
AIT: accidente isquémico transitorio; ARA-II: antagonistas del receptor de la angiotensina II; AVK: antagonistas de la vitamina K; DAI: desfibrilador automático implantable; EC: enfermedad coronaria; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; IECA: inhibidores de la enzima de conversión de la angiotensina; IMC: índice de masa corporal; MPP: marcapasos permanente; NACO: nuevos anticoagulantes orales; NYHA: clase funcional de la New York Heart Association; STS: Society of Thoracic Surgeons; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico]
Variables basales ecocardiográficas y del cateterismo cardiaco derecho
| Variables ecocardiográficas (n=34) | |
| FEVI (%) | 57,5 [55-61] |
| VTDVI (ml/m2) | 72 [53-80] |
| VTSVI (ml/m2) | 29 [22,8-38] |
| Volumen de la AI (ml/m2) | 87 [52,6-114] |
| Gravedad de la insuficiencia mitral | |
| Inexistente | 8 (24) |
| Leve | 20 (61) |
| Moderada | 3 (9) |
| Moderada-grave | 1 (3) |
| Grave | 1 (3) |
| Gravedad de la IT | |
| Inexistente | 0 |
| Leve | 0 |
| Moderada | 0 |
| Grave | 16 (47) |
| Masiva | 15 (44) |
| Torrencial | 3 (9) |
| Mecanismo de la IT | |
| Funcional | 27 (79) |
| Degenerativa | 1 (3) |
| Mixta | 6 (18) |
| IT inducida por electrodo | 1 (3) |
| Vena contracta (cm) | 1,32 [0,9-12] |
| Localización central | 31 (91) |
| Brecha máxima (mm) | 4,98±2,64 |
| Localización principal del chorro | |
| Anteroseptal | 20 (59) |
| Posteroseptal | 5 (15) |
| Anteroposterior | 9 (27) |
| Cambio del área fraccional del VD | 40 [35-47] |
| Área TDVD (cm2) | 21,6 [19-28] |
| Área de la AD (cm2) | 28 [22,7-35] |
| DSPAT (cm) | 18 [15-20] |
| PAPs en la ecocardiografía (mmHg) | 40 [35-47] |
| Colapso de la VCI > 50% | 6 (19) |
| Diámetro máximo de la VCI (mm) | 23 (20-27) |
| Cateterismo cardiaco derecho (n=16) | |
| PAPs (mmHg) | 29 [21-34,5] |
| Máxima en VD (mmHg) | 27 [23-35,5] |
| Máxima en AD (mmHg) | 8 [5,5-15,5] |
AD: aurícula derecha; AI: aurícula izquierda; DSPAT: desplazamiento sistólico del plano del anillo tricuspídeo; FEVI: fracción de eyección del ventrículo izquierdo; IT: insuficiencia tricuspídea; PAP: presión de la arteria pulmonar; PAPs: presión de la arteria pulmonar sistólica; TDVD: telediastólico del ventrículo derecho; VCI: vena cava inferior; VD: ventrículo derecho; VTDVI: volumen telediastólico del ventrículo izquierdo; VTSVI: volumen telesistólico del ventrículo izquierdo.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalointercuartílico].
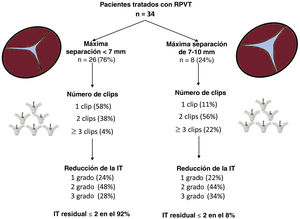
La información sobre la intervención se presenta en la tabla 3. Se alcanzó una reducción aguda de la IT ≥ 1 grado en todos los pacientes. La mayoría de los pacientes necesitaron 1 (47%) o 2 clips (44%), con un claro predominio de implantes de XT (87%) sobre los NT (13%). La ubicación del primer clip fue anteroseptal en más del 90% de los casos. Solo 1 paciente presentó un desprendimiento parcial, que pudo estabilizarse con un 1 clip adicional. La reducción de la IT fue similar en los pacientes con un gap de la valva < 7 mm o de 7-10 mm (figura 1). Se alcanzó el objetivo primario (reducción de la IT ≥ 1 grado al alta) en todos los pacientes. La gravedad de la IT tras la intervención y antes del alta fueron de grado ≤ 2 en el 97 y el 91% de los pacientes. La mediana de estancia hospitalaria fue de 2 [1-3] días.
Datos de la intervención
| Variable | n=34 |
|---|---|
| Número de clips por paciente | |
| 1 | 16 (47) |
| 2 | 15 (44) |
| 3 | 2 (6) |
| > 3 | 1 (3) |
| Tipo de clip | |
| NT | 6 (13) |
| XT | 40 (87) |
| Ubicación del primer clip | |
| Anteroseptal | 31 (91) |
| Posteroseptal | 3 (9) |
| Anteroposterior | 0 |
| Ubicación del segundo clip | |
| Anteroseptal | 14 (74) |
| Posteroseptal | 5 (26) |
| Anteroposterior | 0 |
| Gradiente final medio de la VT (mmHg) | 1,4 [1-2] |
| Duración de la intervención (min) | 130 [100-173] |
| Tiempo de fluoroscopia (min) | 30 [21,75-43,6] |
| Gravedad final de la IT en laboratorio | |
| Inexistente | 0 |
| Leve | 23 (68) |
| Moderada | 10 (29) |
| Grave | 1 (3) |
| Masiva | 0 |
| Torrencial | 0 |
| Complicaciones técnicas | |
| Ninguna | 33 (97) |
| Desprendimiento parcial | 1 (3) |
| Desprendimiento total | 0 |
| Perforación de valva | 0 |
| Rotura de cuerdas tendinosas | 0 |
| Complicaciones clínicas | |
| Ninguna | 32 (94) |
| Muerte | 0 |
| Taponamiento cardiaco | 0 |
| Cirugía de urgencia | 0 |
| Complicaciones vasculares | 0 |
| Hemorragia mayor | 0 |
| Ictus | 0 |
| Infarto de miocardio | 0 |
| Días de ingreso | 2 [1-3] |
| Gravedad de la IT antes del alta | |
| Inexistente | 0 |
| Leve | 17 (50) |
| Moderada | 14 (41) |
| Grave | 3 (9) |
| Masiva | 0 |
| Torrencial | 0 |
| Estrategia antitrombótica al alta | |
| Ninguna | 1 (3) |
| TAPU | 3 (9) |
| TAPD | 1 (3) |
| AVK | 23 (68) |
| NACO | 6 (17) |
AVK: antagonistas de la vitamina K; IT: insuficiencia tricuspídea; NACO: nuevos anticoagulantes orales; TAPD: tratamiento antiagregante plaquetario doble; TAPU: tratamiento antiagregante plaquetario único; VT: válvula tricúspide.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
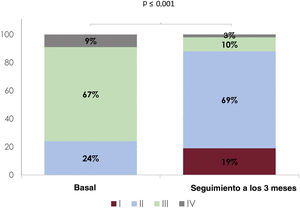
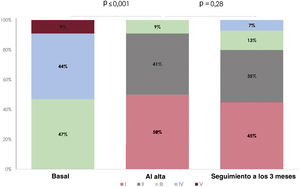
Se dispuso de un seguimiento clínico y ecocardiográfico de todos los pacientes (tabla 4). A los 3 meses, no se había registrado mortalidad. En total, el 88% de los pacientes se encontraban en clase funcional de la NYHA ≤ 2 y solo 3 (9%) requirieron ingreso por insuficiencia cardiaca (figura 2). A 1 paciente (3%) con una IT residual grave se le practicó una nueva intervención 1 mes después de la primera. En el seguimiento a los 3 meses se redujo la dosis de diuréticos a más de la mitad de los pacientes. La IT residual fue de grado ≤ 2 en el 80% de los pacientes (figura 3). Es importante señalar que los parámetros ecocardiográficos —área telediastólica del ventrículo derecho (TDVD), vena contracta de IT y diámetro máximo de la vena cava inferior (VCI)— mejoraron en comparación con el valor basal (tabla 5).
Seguimiento clínico y ecocardiográfico a los 3 meses
| Seguimiento clínico a los 3 meses | |
| Mortalidad | 0 |
| Mortalidad CV | 0 |
| Ingresos por IC | 3 (10) |
| NYHA | |
| I | 6 (19) |
| II | 22 (69) |
| III | 3 (10) |
| IV | 1 (3) |
| Edema periférico | 10 (29) |
| Ascitis | 3 (10) |
| Modificación de dosis de diurético | |
| No | 13 (41) |
| Sí, reducción | 17 (53) |
| Sí, aumento | 2 (6) |
| Dosis diaria de furosemida, media (mg/día) | 45±7,5 |
| Ecocardiografía transtorácica a los 3 meses | |
| Gravedad de la IT | |
| Inexistente | 0 |
| Leve | 14 (45) |
| Moderada | 11 (35) |
| Grave | 4 (13) |
| Masiva | 2 (7) |
| Torrencial | 0 |
| Área de la AD (cm2) | 28,1 [22-36] |
| Área TDVD (cm2) | 18,8 [16,8-24,8] |
| Cambio del área fraccional del VD | 38,5 [33-47] |
| DSPAT (cm) | 1,8 [1,4-1,9] |
| Vena contracta (cm) | 0,6 [0,3-0,9] |
| Colapso de la VCI > 50% | 13 (54) |
| Diámetro máximo de la VCI (mm) | 18 [16-23] |
AD: aurícula derecha; CV: cardiovascular; DSPAT: desplazamiento sistólico del plano del anillo tricuspídeo; IC: insuficiencia cardiaca; IT: insuficiencia tricuspídea; NYHA: clase funcional de la New York Heart Association; TDVD: telediastólico del ventrículo derecho; VCI: vena cava inferior; VD: ventrículo derecho.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
Variables ecocardiográficas basales y en el seguimiento a los 3 meses
| Variable | Basal | Seguimiento a los 3 mes | Cambio | p |
|---|---|---|---|---|
| Área de la AD | 28 [22,7-35] | 28,1 [22-36] | –0,7 [–6 a 4] | 0,31 |
| Área TDVD | 21,6 [19-28] | 18,8 [16,8-24,8] | –2,1 [–4,9 a 0] | 0,021 |
| Cambio del área fraccional del VD | 40 [35-47] | 38,5 [33-47] | 0 [–8 a 6] | 0,818 |
| DSPAT | 18 [15-20] | 18 [15-20] | –0,3 [–6 a 0,4] | 0,10 |
| Vena contracta | 1,32 [0,9-12] | 0,6 [0,3-0,9] | –0,6 [–0,87 a –0,27)] | 0,018 |
| Diámetro máximo de la VCI | 23 [20-27] | 18 [16-23] | –4 (–5,5 a –1) | 0,013 |
AD: aurícula derecha; DSPAT: desplazamiento sistólico del plano del anillo tricuspídeo; TDVD: telediastólico del ventrículo derecho; VCI: vena cava inferior; VD: ventrículo derecho.
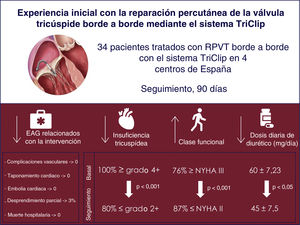
Los resultados principales son que la RPVT borde a borde con el sistema TriClip: a) fue factible y segura, con un alto porcentaje de éxito de la intervención y baja incidencia de complicaciones; b) resultó eficaz según lo indicado por la reducción de la IT de como mínimo 1 grado en todos los pacientes y por una IT residual ≤ 2 en el 91 y el 80% de los pacientes al alta y a los 3 meses respectivamente; c) fue clínicamente trascendente, ya que la mayoría de los pacientes estaban en NYHA ≤ 2 (88%) a los 3 meses; d) se tradujo en una mejora de los parámetros ecocardiográficos (del área TDVD, la vena contracta de IT y el diámetro máximo de la VCI) a los 3 meses, y e) se asoció con más dispositivos XT (87%) que NT (13%).
De entre los demás resultados, la reducción de la IT observada, con ausencia de complicaciones clínicas importantes, probablemente sea el hallazgo más importante del estudio. La disponibilidad de una técnica de RPVT que es sumamente eficaz para la reducción de la IT, pero al mismo tiempo resulta muy segura, representa una importante ventaja del dispositivo y de la técnica. Tal como se muestra en la tabla 3, ningún paciente sufrió una complicación clínica trascendente que pudiera estar relacionada con la intervención. Antes de que se desarrollara el sistema TriClip, la RPVT se llevaba a cabo principalmente con dispositivos borde a borde tricuspídeos inespecíficos, como el sistema MitraClip. El sistema TriClip se basa en la misma tecnología que el MitraClip, pero el nuevo catéter-guía se ha diseñado específicamente para abordar la válvula tricúspide, adaptado al lado derecho del corazón y, por consiguiente, mejorando la seguridad y la eficacia de la intervención6. El registro más grande de pacientes en los que se ha utilizado la RPVT borde a borde antes de la introducción del sistema TriClip mostró un éxito agudo de la reparación de la válvula tricúspide en un 83% de los pacientes en comparación con nuestro 100% de éxitos agudos o el 87% de éxitos a los 30 días en el ensayo TRILUMINATE1–13.
Por otro lado, los resultados observados fueron mejores aún que los del ensayo TRILUMINATE, en el que, a pesar de que el 87% de los pacientes mostraron una mejora de la IT de al menos 1 grado, solo el 60% de ellos tenían IT ≤ 2 a los 30 días10,11. Tiene interés señalar que el 60% descrito a los 30 días aumentó hasta el 70% a 1 año, como resultado del remodelado inverso de las cámaras cardiacas derechas11. Nuestra serie reveló una reducción de la IT de 1 grado como mínimo en todos los pacientes y una IT residual ≤ 2 en el 80% de los pacientes a los 3 meses. La mejora de los resultados puede responder a varios factores, pero es probable que la experiencia creciente de los operadores y la disponibilidad no solo de dispositivos NT (de brazos cortos), sino también de dispositivos XT (de brazos largos), sean los factores más importantes que explicarían estos resultados prometedores. En la presente serie, el sistema XT se utilizó en el 87% de los clips implantados. Es probable que la disponibilidad del clip XT tuviera un papel muy importante en los resultados de la intervención al facilitar el proceso de sujeción en cualquier anatomía, pero en especial en las válvulas con una brecha de coaptación grande. El clip NT se reservó generalmente para la sujeción más comisural, en la que los operadores podían prever un mayor riesgo de atrapamiento con el aparato subvalvular. La mayoría de los pacientes (91%) presentaron chorros centrales y a muchos se los trató con un solo clip (47%). De manera similar a lo indicado por experiencias previas11,13,14, el primer clip se implantó anteroseptal en el 91% de los casos. Fue necesario un segundo clip en el 44%. Este segundo clip se implantó también anteroseptal en el 75% de los pacientes y posteroseptal en el 26%. En 2 pacientes (6%) se necesitaron 3 clips y 1 (3%) requirió 5. El paciente con 5 clips presentó un desprendimiento parcial que se detectó durante la intervención y se fijó con clips adicionales en la misma intervención. A los 3 meses, no se había detectado ningún otro caso de desprendimiento parcial o total. A diferencia de lo indicado en publicaciones anteriores13, no parece que un gap ≥ 7 mm limite la efectividad del tratamiento, ya que el grado de reducción de la IT fue similar en los pacientes con brechas < 7 y de 7-10 mm. De nuevo, los resultados presentados podrían explicarse por la experiencia creciente y por la disponibilidad actual del dispositivo XT. Además, tal como se muestra en la figura 1, los pacientes con brechas ≥ 7 mm necesitaron mayor número de clips. En cualquier caso, es importante reconocer que el gap máximo tratado en esta serie fue de 10mm, por lo que los resultados en los casos > 10 mm son inciertos.
En la presente serie no se incluyó ningún caso en el que se usara el dispositivo de última generación TriClip G4. El sistema G4 se ha comercializado ya y aporta algunas características adicionales que podrían mejorar los resultados de la intervención. El dispositivo TriClip G4, al igual que el MitraClip G4, está disponible en 4 tamaños: los dispositivos regulares NT y XT y también las versiones anchas: NTW y XTW15. El sistema TriClip G4 permite también la sujeción independiente de la línea de sujeción; esta es una característica novedosa que podría ser muy útil en la aplicación tricuspídea por 2 razones. Primero, podría facilitar el tratamiento de brechas de coaptación amplias y, segundo, puede mejorar la visualización del proceso de sujeción en los casos en que la ventana de la ecocardiografía transesofágica sea difícil, ya que el foco de la ecocardiografía puede centrarse individualmente en una u otra valva. Además, si la sujeción de la válvula es deficiente, la línea de sujeción independiente puede ser útil para optimizar la inserción en la valva en un solo lado sin perder la valva del otro.
A pesar del corto seguimiento, la mayoría de los pacientes presentaron mejoría clínica según lo indicado por la clase funcional de la NYHA ≤ 2 a los 3 meses en el 87% de los pacientes (figura 4). Los presentes resultados son coherentes con los observados en el ensayo TRILUMINATE, en el que el 82 y el 83% de los pacientes estaban en NYHA ≤ 2 a los 30 días y a 1 año respectivamente11. Por otro lado, solo 3 tuvieron que ser rehospitalizados por insuficiencia cardiaca en el seguimiento a los 3 meses. Dos de estos pacientes tenían una IT torrencial antes de la RPVT, que se redujo a grave después de esta. En el ensayo TRILUMINATE, la persistencia de una IT grave o superior después de la RPVT se asoció con un aumento de la mortalidad y las hospitalizaciones por insuficiencia cardiaca a 1 año, con un aumento de cerca de 3 veces en el número de participantes con una IT grave o superior en comparación con los que tenían una IT moderada o inferior después de la RPVT11 (el 24,5 frente al 8,8%). Este hecho resalta los efectos de la reducción de la IT en los resultados clínicos de los pacientes sometidos a RPVT: cuanto mayor sea la reducción de la IT, mayores son los beneficios clínicos obtenidos. En nuestra serie, se pudo reducir la dosis de los diuréticos a más de la mitad de los pacientes (53%) y solo para el 6% fue necesario un aumento. La modificación de la dosis de los diuréticos es objeto de controversia en la actualidad. Algunos médicos defienden mantener las dosis de durante 3 meses para fomentar un remodelado inverso de las cámaras cardiacas derechas manteniendo una IT residual lo más baja posible. Es probable que el remodelado inverso de las cámaras cardiacas derechas sea una de las razones que expliquen por qué los efectos beneficiosos tanto clínicos como electrocardiográficos parecen aumentar más en el seguimiento10,11. Tal como se muestra en la tabla 5, a pesar del escaso número de pacientes, el área TDVD se redujo a los 3 meses, lo cual indica cierto grado de remodelado inverso. Parece que el remodelado inverso se produce pronto tras la operación10. En el ensayo TRILUMINATE, se observaron reducciones tempranas (a los 30 días) y persistentes (a 1 año) de los volúmenes de la AD y el VD10,11. También se apreció una mejora más progresiva del desplazamiento sistólico del plano del anillo tricuspídeo (DSPAT) en el primer año11. En nuestro estudio, la ausencia de diferencias significativas en el DSPAT puede responder al seguimiento corto y al hecho de que el DSPAT basal fuera grande (1,8 cm), lo cual indica el estado basal relativamente conservado de la función del VD de la mayoría de los pacientes.
El presente estudio tiene varias limitaciones. Es un registro observacional de pequeño tamaño, lo cual implica un sesgo de selección inherente. Además, resulta difícil captar y controlar todos los posibles factores de confusión cuando se usan los datos de un registro. Además, es posible que el tamaño muestral no proporcione la potencia estadística necesaria para detectar factores predictivos de la mejora de la clase funcional de la NYHA, las variables ecocardiográficas o la predicción del fallo de la intervención. Tanto los datos clínicos como los ecocardiográficos fueron notificados por los propios centros, de manera que no hubo una validación («adjudicación») independiente de los eventos clínicos ni un laboratorio central para los análisis ecocardiográficos. Nuestra cohorte presentó una puntuación Euroscore II inferior a la de la cohorte del estudio TRILUMINATE. Esto podría explicarse por el hecho de que la contraindicación principal a la cirugía cardiaca en nuestra cohorte fue la presencia de fragilidad, una característica clínica que se ha asociado con peor pronóstico tras cirugía cardiaca16 y que no se evalúa en la puntuación Euroscore II. El cateterismo cardiaco derecho es el patrón de referencia para la evaluación de la gravedad de la hipertensión pulmonar. En nuestra cohorte, solo en 16 pacientes se llevó a cabo un cateterismo cardiaco derecho antes de la RPVT. La razón principal de que no se realizara un cateterismo cardiaco derecho a estos pacientes fue la ausencia de cardiopatía izquierda y los signos ecocardiográficos indirectos de hipertensión pulmonar. El cuestionario de calidad de vida relacionada con la salud y la prueba de los 6 min de marcha realizadas antes y después de la RPVT podrían ayudar a comprender mejor las repercusiones de este tratamiento prometedor.
CONCLUSIONESSe presenta la experiencia inicial con el sistema TriClip para la RPVT borde a borde después de su distribución limitada a algunos centros con experiencia. El dispositivo parece ser eficaz y seguro, con unos resultados prometedores por lo que respecta a la reducción de la IT, no solo aguda sino también a los 3 meses de seguimiento. Serán necesarios nuevos estudios con una muestra más grande y un seguimiento más largo para confirmar nuestros resultados.
- –
La insuficiencia tricuspídea ha generado un interés creciente en los últimos años, principalmente por su asociación con un aumento del riesgo de morbilidad y mortalidad.
- –
Recientemente han surgido las técnicas de reparación percutánea de la válvula tricúspide como alternativa para el tratamiento de la insuficiencia tricuspídea grave en los pacientes que no son aptos para la cirugía.
- –
La reparación percutánea de la válvula tricúspide borde a borde con el sistema TriClip es la estrategia con una mayor penetración en el mundo.
- –
Se describe la experiencia inicial con el sistema TriClip para la reparación percutánea de la válvula tricúspide borde a borde después de una distribución limitada a algunos centros con experiencia.
- –
La reparación percutánea de la válvula tricúspide borde a borde con el sistema TriClip resultó factible y segura, con un elevado porcentaje de éxito de la intervención y una baja incidencia de complicaciones.
- –
Se logró una insuficiencia tricuspídea residual ≤ 2 en el 91 y el 80% de la cohorte al alta y a los 3 meses respectivamente.
Sin financiación.
CONTRIBUCIÓN DE LOS AUTORESX. Freixa, D. Arzamendi, R. Estévez-Loureiro y J. Goicolea concibieron y diseñaron el análisis. M. del Trigo, P. Li, L. Sanchis y Manuel Barreiro obtuvieron los datos. X. Freixa y P. L. Cepas-Guillén llevaron a cabo el análisis. A. Regueiro, J.A. Baz, L. Asmarats, F. Calvo, V. Moñivas, I. Meduiña y M. Sitges revisaron y corrigieron el manuscrito.
CONFLICTO DE INTERESESX. Freixa, L. Sanchis, D. Arzamendi, R. Estévez-Loureiro y M. Sitges han sido mentores de Abbott. R. Estévez-Loureiro declara pagos por conferencias de Abbott, Boston Edwards Lifesciences y P&F. L. Sanchis es editor asociado de Rev Esp Cardiol. Se ha seguido el procedimiento editorial establecido por la Revista para garantizar un tratamiento imparcial del manuscrito.