Asistimos a un avance imparable en los procedimientos percutáneos para el tratamiento de las cardiopatías congénitas1. Los cirujanos debemos estar familiarizados con la evolución de dicha tecnología por 2 motivos:
- •
Ha cambiado la manera de abordar determinadas cardiopatías, fundamentalmente complejas, que precisan intervención percutánea y cirugía en serie.
- •
Encontrarnos stents en quirófano y, por lo tanto, tenemos que aprender a manejarlos y establecer patrones o algoritmos de actuación.
Se presenta una serie de 105 pacientes incluidos durante 7 años consecutivos (2013-2019) en los que se manipularon los stents previamente implantados. En un trabajo previo2 se revisaron las escasas publicaciones referentes a stents en Fallot3, ductus4 o ramas pulmonares5.
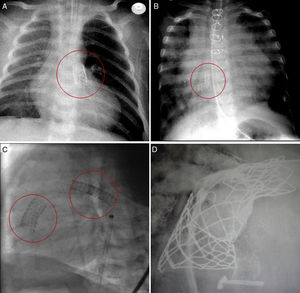
En total, se manipularon 131 stents (tabla 1) en las siguientes posiciones: 18 en ductus, 34 en el tracto de salida del ventrículo derecho, 11 en comunicación interauricular, 14 en la arteria pulmonar derecha (APD), 36 en la arteria pulmonar izquierda, 7 en la vena cava superior, 7 en la vena cava inferior, 2 en la aorta ascendente y 2 en la aurícula izquierda (figura 1). Los procedimientos quirúrgicos realizados en los 105 pacientes (tabla 1) fueron: 25 trasplantes, 13 Fontan, 7 Glenn, 2 comprehensive repair (Norwood+Glenn), 2 Glenn take-down, 23 recambios de conducto (entre el ventrículo derecho y las ramas pulmonares), 11 Fallot, 6 Rastelli, 1 Ross-Konno, 1 Yasui (Norwood+Rastelli) y otros (14). Como dato adicional, 47 de los pacientes presentaban fisiología univentricular.
Localizaciones de los stents y procedimientos quirúrgicos
| Localizaciones de los stents | n = 131 |
| Rama pulmonar izquierda | 36 |
| Tracto de salida del ventrículo derecho | 34 |
| Ductus | 18 |
| Rama pulmonar derecha | 14 |
| Tabique interauricular | 11 |
| Vena cava superior | 7 |
| Vena cava inferior | 7 |
| Aorta ascendente | 2 |
| Aurícula izquierda | 2 |
| Intervenciones realizadas | n = 105 |
| Trasplante | 25 |
| Recambio de conducto | 23 |
| Fontan | 13 |
| Fallot | 11 |
| Glenn bidireccional | 7 |
| Rastelli | 6 |
| Glenn take-down | 2 |
| Norwood-Glenn (comprehensive) | 2 |
| Ross-Konno | 1 |
| Norwood-Rastelli (Yasui) | 1 |
| Otros | 14 |
En función de la localización anatómica, los stents se ligaron externamente (clip ductal) y se retiraron de manera parcial (apertura longitudinal y/o recorte del borde) o total (tras la disección roma de la estructura subyacente). El criterio para efectuar una retirada parcial o total se basó en la fragilidad/consistencia del vaso en el que se apoya el stent (ramas pulmonares, ventrículo derecho) y el juicio del cirujano (a medida que se adquiría experiencia). Además, las maniobras imprevistas inicialmente, como el uso de hipotermia profunda con parada circulatoria (que prolonga el tiempo de cirugía e incrementa la morbilidad), también se registraron.
Las localizaciones anatómicas donde más frecuentemente se encontraban los stents son la rama pulmonar izquierda y el tracto de salida del ventrículo derecho. Juntos suman 2 tercios del total (66%). Trasplantes, recambios de conducto y cirugía univentricular en conjunto suponen un 80% de los diagnósticos principales. No es de extrañar que todos ellos fueran reintervenciones (en ocasiones, múltiples) y en niños tratados con cirugías y procedimientos percutáneos en secuencia. Es precisamente en los trasplantes donde se han encontrado más dobles (o triples) stents (rama pulmonar izquierda más cava superior o inferior, habitualmente).
La posición del dispositivo no necesariamente tiene relación con su retirada total o parcial. Paradójicamente, un stent de rama pulmonar izquierda en un Glenn se puede recortar para acomodar la sutura de un Fontan extracardiaco (retirada parcial, fácil), mientras que el mismo paciente precisa una extracción completa del stent en idéntica posición (más ampliación de las ramas con parche de pericardio) para realizar un trasplante (retirada completa, difícil).
En el caso de stent ductal se debe diferenciar 2 grupos: los 10 pacientes que terminan en cirugía de Fallot o Rastelli (clip externo, procedimiento sencillo) y los 8 restantes con procedimiento híbrido6 y evolución posterior a cirugía compleja (Norwood-Glenn, Ross-Konno, Yasui, trasplante).
Casi la mitad de los pacientes intervenidos en nuestra serie corresponden a cirugía univentricular, en diversos estadios. Como paradigma, los trasplantes son el perfecto ejemplo (reintervenciones, cateterismos previos, fisiología univentricular, etc.). La planificación quirúrgica permite anticipar periodos de hipotermia profunda y parada circulatoria si hay 1 o más stents en varias posiciones.
Los hemodinamistas y los cirujanos debemos ampliar los horizontes. Los retos que nos presentan los pacientes más complejos (multioperados, pluricateterizados) nos ofrecen la oportunidad de modificar los tiempos, indicando cirugía o hemodinámica de manera alternativa o incluso simultánea (procedimientos híbridos). Una reflexión de este trabajo es que los cirujanos aprendemos a manejar los stents previamente implantados, y podemos anticipar la estrategia quirúrgica en función de su localización y el diagnóstico. Así, un stent en el ductus es fácil de retirar en el caso de un Fallot y difícil en un procedimiento híbrido; un dispositivo en una rama pulmonar izquierda en sencillo de manejar si se precisa un recambio de conducto y complejo en un Fontan para un trasplante. Los datos analizados en este trabajo nos enseñan que las cardiopatías complejas (reintervenciones, corazón univentricular, trasplante, etc.) presentan stents intracardiacos con frecuencia. A medida que los cirujanos adquirimos experiencia en su manejo durante las cirugías posteriores, los hemodinamistas se animan a seguir implantándolos en futuros pacientes, de manera individual o junto con cirugía (procedimientos híbridos). La evolución de ambas especialidades (hemodinámica y cirugía) nos anima a revisar continuamente nuestros procesos.