El Registro Español del Síndrome Aórtico Agudo (RESA) se inició en 2005 para valorar las características del síndrome aórtico agudo (SAA) en nuestro país. El objetivo es analizar las diferencias en las características, el abordaje y el tratamiento y la mortalidad observadas entre las 3 ediciones del RESA.
MétodosSe analizaron los datos de los pacientes con SAA incluidos prospectivamente por 24-30 hospitales terciarios en las 3 ediciones: RESA I (2005-2006), RESA II (2012-2013) y RESA III (2018-2019).
ResultadosSe incluyó a 1.902 pacientes (el 74% varones; media de edad, 60,7± 12,5 años), 1.329 (69,9%) tipo A y 573 (30,1%) tipo B. Comparando los RESAS, la tomografía computarizada aumentó como técnica diagnóstica (el 77,1, el 77,9 y el 84,2% respectivamente; p=0,001). El tratamiento quirúrgico del SAA tipo A aumentó (el 79,6, el 78,7 y el 84,5%; p=0,045) y la mortalidad total disminuyó (el 41,2, el 34,5 y el 31,2%; p=0,002), coincidiendo con una reducción de la mortalidad quirúrgica (el 33,4, el 25,1 y el 23,9%; p=0,003). En el tipo B, el tratamiento endovascular aumentó (el 22,8, el 32,8 y el 38,7%; p=0,006). La mortalidad total del SAA tipo B disminuyó (el 21,6, el 16,1 y el 12,0%; p=0,005) como consecuencia de la reducción de la mortalidad de los tratamientos médico (el 16,8, el 13,8 y el 8,8%; p=0,030) y endovascular (el 27,0, el 18,0 y el 9,2%; p=0,009).
ConclusionesEl RESA evidencia una disminución de la mortalidad del SAA tipo A coincidiendo con un incremento del tratamiento quirúrgico y una reducción de su mortalidad. En el SAA tipo B, el tratamiento endovascular se asocia con un aumento de la supervivencia, ya que permite una mejor estrategia terapéutica para los pacientes con complicaciones.
Palabras clave
Vídeo del artículo

El síndrome aórtico agudo (SAA) es una emergencia cardiovascular que se asocia con grandes morbilidad y mortalidad1. Estudios recientes han demostrado que la frecuencia del SAA es de 110-170 casos/millón de habitantes/año2,3, bastante superior a lo que se consideraba previamente, y que aproximadamente la mitad de los pacientes con SAA fallecen antes de llegar al hospital4. A pesar de los avances en el diagnóstico y el tratamiento del SAA, la mortalidad hospitalaria (20-35%)1 sigue siendo alta. Para mejorar la supervivencia del SAA, es fundamental una gran sospecha clínica, una estrategia diagnóstica definida y un equipo médico-quirúrgico con adecuada experiencia.
Desde el inicio del registro IRAD5, el conocimiento del SAA en su presentación clínica, sus complicaciones y su tratamiento ha mejorado de modo considerable. No obstante, el IRAD es un registro internacional de centros de excelencia que no permite extrapolar los resultados a los de la práctica clínica general. En los últimos años, varios registros nacionales6–9 han reproducido el análisis del IRAD con enfoques y sesgos diferentes y resultados que no representan la realidad de nuestro país. El objetivo del Registro Español del Síndrome Aórtico (RESA) es analizar los resultados en diagnóstico, tratamiento y mortalidad del SAA en nuestro país y determinar su evolución a lo largo de los años. El RESA I10 se llevó a cabo en 2005-2006; el RESA II11, en 2012-2013 y el RESA III, en 2018-2019; la mayoría de los hospitales terciarios del país participan en el registro. El avance de las técnicas de imagen combinado con el progreso en las técnicas quirúrgicas y endovasculares ha modificado el diagnóstico y el tratamiento de la enfermedad durante este periodo12.
El presente estudio aporta los resultados del RESA III y los compara con la serie completa de los estudios RESA con el propósito de analizar los cambios en el diagnóstico y el abordaje del SAA a lo largo de estos 15 años en nuestro país y las implicaciones que han podido tener en la mortalidad del SAA.
MÉTODOSSe trata de un registro prospectivo, protocolizado, observacional y descriptivo en hospitales de tercer nivel con disponibilidad ininterrumpida de técnicas de imagen cardiovascular, hemodinámica y cirugía cardiaca. En total, 24 hospitales terciarios de los 34 propuestos aceptaron participar en el RESA I10. Aceptaron participar 2 más en el RESA II11 (n=26) y otros 6 en el RESA III (n=30). Los centros participantes se comprometieron a incluir prospectivamente a todos los pacientes con SAA consecutivos, ya fueran referidos de otros centros o diagnosticados en el propio hospital durante los 2 años que duraba cada fase del registro. Los periodos de inclusión fueron del 1 de enero de 2005 al 31 de diciembre de 2006 en el RESA I, del 1 de enero del 2012 al 31 de diciembre del 2013 en el RESA II y del 1 de enero del 2018 al 31 de diciembre del 2019 en el RESA III. El RESA I incluyó a 519 pacientes6; el RESA II, a 62911 y el RESA-III, a 754. Por lo tanto, la serie analizada incluye a 1.902 pacientes, 1.328 (69,9%) con SAA tipo A y 574 (30,1%) con SAA tipo B.
Recogida de datosEl método para la recogida de datos estaba preespecificado10. En resumen, se solicitó a cada centro que nombrara un coordinador responsable de la recolección y validación de los datos de los pacientes diagnosticados de SAA. Los pacientes fueron identificados en el servicio de urgencias, los departamentos de imagen o los informes de alta hospitalarios. La hoja de recogida de datos incluyó 140 variables con información demográfica, historia clínica, examen físico, técnicas de imagen, tratamiento, mortalidad y complicaciones hospitalarias. Se diseñó una base de datos para la recolección de la información con el programa REDCap (Research Electronic Data Capture Vanderbilt University). El protocolo del estudio se ajustó a las pautas éticas de la Declaración de Helsinki de 1975 y fue aprobado por los comités de investigación ética del Hospital Universitario Vall d’Hebron y los demás hospitales participantes, y se obtuvo consentimiento informado de los pacientes incluidos. Las variables se definieron en concordancia con el Registro IRAD (International Registry of Aortic Dissection)1 para facilitar una posible comparación posterior. El IRAD es un registro internacional que se inició en 1996 con la participación de 24 centros de diferentes países de Europa, Estados Unidos y Japón; en la actualidad participan más de 60 centros. Se consideró el antecedente de arterioesclerosis si el paciente ya había tenido diagnóstico de cardiopatía isquémica, arteriopatía obliterante o accidente cerebrovascular. Se definió shock si la presión arterial sistólica era <80mmHg y alteración de la función renal si la creatinina era >1,5mg/100ml o el filtrado glomerular era <30/min/1,73 m2. De los pacientes con información incompleta, se utilizaron los datos disponibles, pero siempre se incluyó el caso. Cualquier duda se solucionó comunicando telefónicamente con el responsable de cada hospital. No se incluyó en el estudio a los pacientes con disección aórtica crónica o de causa postraumática o iatrogénica.
Análisis de datosLos datos se analizaron mediante el paquete estadístico STATA versión 15.1 (StataCorp, Estados Unidos). Se analizaron los datos demográficos, la primera técnica diagnóstica, las complicaciones, el abordaje terapéutico y la mortalidad en la fase aguda. Las variables cuantitativas se expresaron como media±desviación estándar y las cualitativas, en porcentaje. La comparación de variables cuantitativas entre grupos se realizó mediante test de ANOVA y entre variables cualitativas, mediante el test de la χ2 o el exacto de Fisher. Se hizo una prueba no paramétrica de tendencias. Un valor de p <0,05 se consideró significativo.
RESULTADOSEn las 3 ediciones del RESA se incluyó a 1.902 pacientes con SAA (el 74% varones; media de edad, 60,7±12,5 años). Los datos demográficos y los antecedentes clínicos se presentan en la tabla 1. A lo largo de los 3 periodos, se ha observado un incremento de la frecuencia del diagnóstico de SAA en las mujeres (el 22,5, el 27,0 y el 29,6% respectivamente; p=0,006) y la frecuencia de los antecedentes de aneurisma aórtico y valvulopatía aórtica, particularmente en el RESA III.
Datos demográficos en los estudios RESA
| Variable | Total (n=1.902) | RESA I (n=519) | RESA II (n=629) | RESA III (n=754) | p | Tendencia, p |
|---|---|---|---|---|---|---|
| Edad (años) | 63,6±13,1 | 60,9±13,3 | 64,7±14,0 | 65,6±11,7 | 0,001 | 0,001 |
| Edad> 70 años | 590 (29,4) | 154 (29,7) | 238 (38,8) | 167 (37,7) | 0,001 | 0,036 |
| Varones | 1.392 (73,2) | 402 (77,5) | 459 (73,0) | 531 (70,4) | 0,020 | 0,006 |
| Hipertensión | 1.335 (70,2) | 369 (71,1) | 410 (65,2) | 556 (73,7) | 0,061 | 0,172 |
| Fumadores | 820 (43,1) | 233 (44,9) | 259 (41,2) | 328 (43,5) | 0,123 | 0,269 |
| Dislipemia | 537 (28,2) | 116 (22,4) | 190 (30,2) | 231 (30,6) | 0,009 | 0,088 |
| Diabetes mellitus | 178 (9,4) | 43 (8,3) | 56 (8,9) | 79 (10,5) | 0,489 | 0,275 |
| Cardiopatía isquémica | 173 (9,1) | 44 (8,5) | 53 (8,4) | 76 (10,1) | 0,545 | 0,413 |
| Ateroesclerosis | 303 (15,9) | 97 (18,7) | 127 (20,2) | 79 (17,8) | 0,818 | 0,817 |
| Síndrome de Marfan | 65 (3,4) | 33 (6,4) | 14 (2,2) | 18 (2,4) | 0,001 | 0,001 |
| Aneurisma aórtico | 406 (21,3) | 89 (17,1) | 118 (18,8) | 199 (26,4) | 0,001 | 0,001 |
| Valvulopatía aórtica | 188 (9,9) | 46 (8,9) | 50 (7,9) | 92 (12,2) | 0,026 | 0,056 |
| Cirugía cardiaca | 120 (6,3) | 34 (6,6) | 39 (6,2) | 47 (6,2) | 0,322 | 0,139 |
Los valores expresan n (%) o media±desviación estándar.
La tomografía computarizada es la primera técnica de imagen en el diagnóstico del SAA, con un uso creciente a lo largo de las 3 ediciones (el 77,1, el 77,9 y el 84,2%; p=0,001). EL SAA se clasificó como tipo A en 1.328 casos (69,9%) y tipo B en 574 (30,1%), con frecuencias de hematoma intramural y úlcera penetrante similares en las 3 ediciones. El intervalo entre el inicio de los síntomas y el diagnóstico del SAA disminuyó significativamente a lo largo de las 3 ediciones del RESA, <24 h en el 70,3, el 84,0 y el 86,5% de los casos (p=0,012). No hubo diferencias significativas en las demoras de los diagnósticos realizados en las primeras 24 h.
Las complicaciones del SAA diagnosticadas al ingreso hospitalario antes del tratamiento quirúrgico o endovascular fueron similares en los 3 periodos, aunque en el RESA III hubo una mayor frecuencia de coma e isquemia periférica y menor de isquemia mesentérica (tabla 2).
Diagnóstico por técnicas de imagen y complicaciones en los estudios RESA
| Total (n=1.902) | RESA-I (n=519) | RESA-II (n=629) | RESA-III (n=754) | p | Tendencia, p | |
|---|---|---|---|---|---|---|
| Primera técnica de imagen diagnóstica | ||||||
| TC | 1.527 (80,3) | 400 (77,1) | 490 (77,9) | 637 (84,2) | 0,001 | 0,001 |
| ETE | 52 (2,7) | 7 (13,5) | 19 (3,0) | 26 (3,4) | 0,001 | 0,001 |
| ETT | 197 (10,4) | 24 (4,6) | 92 (14,6) | 81 (10,7) | 0,003 | 0,003 |
| RMC | 38 (1,9) | 2 (0,4) | 26 (4,1) | 10 (1,3) | 0,487 | 0,092 |
| Angiografía | 25 (1,3) | 15 (2,9) | 2 (0,3) | 8 (1,1) | 0,745 | 0,345 |
| Demora diagnóstica | ||||||
| <24 h | 70,3 | 84,0 | 86,5 | 0,042 | 0,012 | |
| Mediana de diagnóstico en las primeras 24 h (h) | 5 [3-10] | 5 [3-15] | 5 [3-11] | 0,874 | 0,748 | |
| Tipo de SAA | ||||||
| Tipo A | 1.329 (69,8) | 357 (68,8) | 443 (70,4) | 529 (70,3) | 0,731 | 0,630 |
| Tipo B | 573 (30,2) | 162 (31,2) | 186 (29,6) | 225 (29,7) | ||
| Disección | 1.537 (80,8) | 430 (82,5) | 495 (78,9) | 612 (81,2) | 0,195 | 0,569 |
| Hematoma | 249 (13,1) | 64 (12,3) | 83 (13,1) | 102 (13,5) | 0,089 | 0,865 |
| Úlcera penetrante | 116 (6,1) | 25 (4,8) | 51 (8,1) | 40 (5,3) | 0,514 | 0,379 |
| Complicaciones | ||||||
| Shock | 301 (15,9) | 97 (18,7) | 90 (14,3) | 114 (15,3) | 0,192 | 0,138 |
| Coma | 66 (3,5) | 15 (2,9) | 20 (3,2) | 31 (4,2) | 0,416 | 0,205 |
| Taponamiento | 196 (10,3) | 59 (11,4) | 53 (8,4) | 84 (11,1) | 0,161 | 0,959 |
| Isquemia visceral | 108 (5,7) | 33 (6,4) | 38 (6,0) | 37 (4,9) | 0,040 | 0,360 |
| Isquemia periférica | 202 (10,6) | 46 (8,9) | 64 (10,1) | 92 (12,2) | 0,018 | 0,084 |
| Hematoma periaórtico | 469 (27,7) | 111 (31,4) | 169 (26,9) | 189 (25,6) | 0,120 | 0,063 |
| Insuficiencia renal | 379 (19,9) | 94 (18,2) | 146 (19,1) | 139 (18,4) | 0,321 | 0,673 |
ETE: ecocardiograma transesofágico; ETT: ecocardiograma transtorácico; RMC: resonancia magnética cardiaca; SAA: síndrome aórtico agudo; TC: tomografía computarizada.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
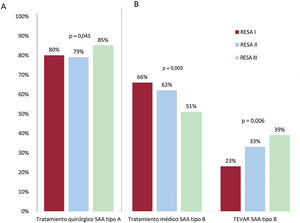
En el SAA tipo A se observó aumento del tratamiento quirúrgico (el 79,6, el 78,7 y el 84,5%; p=0,045) (figura 1A). La edad de los pacientes intervenidos aumentó significativamente con los RESA (58,6±12,6, 61,1±13,3 y 62,5±10,9 años; p=0,001). En el 94,4% de los SAA tipo A tratados con cirugía, antes se realizó una tomografía computarizada. En el RESA III los motivos de que no hubiera tratamiento quirúrgico fueron: fallecimiento en urgencias o previa al trasladado del paciente al quirófano (32,7%), comorbilidades (30,1%), edad> 80 años (22,6%), hematoma intramural (8,7%) y rechazo del paciente (6,7%). En el SAA tipo B se observó una disminución progresiva del tratamiento exclusivamente médico, sobre todo en el RESA III (el 66,0, el 62,3 y el 50,7%; p=0,003); esta disminución coincidió con un aumento progresivo del tratamiento endovascular en las 3 ediciones del RESA (el 22,8, el 32,8 y el 38,7%; p=0,006) (figura 1B). Por el contrario, no hubo diferencias significativas en la indicación del tratamiento quirúrgico del SAA tipo B (el 11,2, el 4,8 y el 10,6%; p=0,474). En el RESA III, las indicaciones de tratamiento endovascular o quirúrgico abierto en el SAA tipo B fueron: signos de rotura aórtica contenida (21%), inestabilidad hemodinámica (20%), hipertensión arterial no controlable (17%), dilatación aórtica grave (11%), isquemia visceral o periférica (10%), extensión de la disección (6%) y persistencia del dolor (4%).
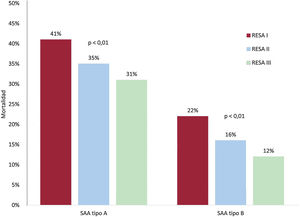
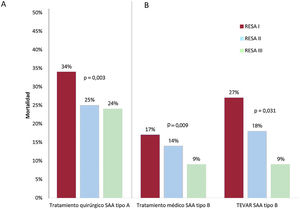
MortalidadLa mortalidad hospitalaria total del SAA tipo A disminuyó a lo largo de los 3 RESAS (el 41,2, el 34,5 y el 31,2%; p=0,002) (tabla 3 y figura 2), coincidiendo con una reducción de la mortalidad del tratamiento quirúrgico (el 33,4, el 25,1 y el 23,9%; p=0,002) (figura 3A). La mortalidad total del SAA tipo B también disminuyó en los 3 registros (el 22,8, el 16,1 y el 12,0%; p=0,005) (figura 2), como consecuencia de la disminución de la mortalidad en el grupo solo con tratamiento médico (el 16,8, el 13,8 y el 8,8%; p=0,030) y también en el grupo con TEVAR (el 27,0, el 18,0 y el 9,2%; p=0,009) (figura 3B). El análisis de la mortalidad del SAA tipos A y B en cada uno de los RESAS, ajustado por edad y complicaciones, mostró la asociación entre la disminución de la mortalidad en el SAA tipos y B y en los subgrupos de tratamiento con los RESAS II y III (tabla 1 del material adicional).
Tratamiento y mortalidad del síndrome aórtico agudo en los estudios RESA
| Tipo A | Tipo B | ||||||
|---|---|---|---|---|---|---|---|
| Total | Cirugía | Médico | Total | Médico | TEVAR | Cirugía | |
| Tratamiento | |||||||
| RESA I | 357 | 286 (79,6) | 71 (20,4) | 162 | 106 (65,4) | 41(25,3) | 15(9,3) |
| RESA II | 443 | 347(78,7) | 96 (21,3) | 186 | 116 (62,4) | 62 (33,3) | 8 (4,3) |
| RESA III | 529 | 447 (84,5) | 82 (15,5) | 225 | 114 (50,7) | 87 (38,7) | 24 (10,6) |
| Total | 1.329 | 1.080 (81,3) | 249 (18,7) | 573 | 336 (58,6) | 190 (33,2) | 47 (8,2) |
| p | — | 0,039 | — | — | 0,009 | 0,022 | 0,756 |
| Tendencia, p | — | 0,045 | — | — | 0,003 | 0,006 | 0,474 |
| Mortalidad | |||||||
| RESA I | 147 (41,2) | 95 (33,4) | 52 (71,2) | 37 (22,8) | 18 (16,8) | 10 (27,0) | 9 (50,0) |
| RESA II | 153 (34,5) | 87 (25,1) | 66 (68,7) | 30 (16,1) | 16 (13,8) | 11 (18,0) | 3 (33,3) |
| RESA III | 165 (31,2) | 107 (23,9) | 58 (70,3) | 27 (12,0) | 10 (8,8) | 8 (9,2) | 9 (37,5) |
| p | 0,007 | 0,003 | 0,913 | 0,018 | 0,094 | 0,031 | — |
| Tendencia, p | 0,002 | 0,002 | 0,675 | 0,005 | 0,030 | 0,009 | — |
TEVAR: reparación endovascular de la aorta torácica.
Salvo otra indicación, los valores expresan n (%).
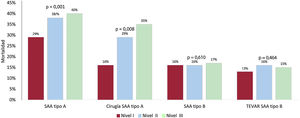
El número de SAA atendidos en cada centro se asoció con la mortalidad del SAA tipo A pero no con la del tipo B. Solo 7 centros trataron ≥ 12 SAA tipo A por año (nivel de actividad I A), con una la mortalidad total del 28,8%, mientras que la mortalidad en 13 centros que trataron entre 6 y 11 casos al año (nivel de actividad II A) fue del 38,1% y en los 14 centros que trataron menos de 6 casos al año (nivel de actividad III A), la mortalidad fue del 40,4% (p=0,001). De modo similar, la mortalidad quirúrgica del SAA tipo A en los centros de actividad de nivel I A fue del 16,6%; en los de actividad II A, del 28,7% y en los de actividad III A, del 34,9% (p=0,008). Por el contrario, en el SAA tipo B no se evidenciaron diferencias entre los centros que trataron a más de 6 pacientes por año (I B), con una mortalidad del 16,1%, los que trataron 3-6 casos por año (II B), con una mortalidad del 15,6%, y los que trataron menos de 3 casos por año (III B), con una mortalidad del 16,9% (p=0,610). En el tratamiento con TEVAR, tampoco hubo diferencias de mortalidad entre los centros que realizaron al menos 6, entre 3 y 5 o menos de 3 TEVAR al año por SAA (el 13,4, el 16,0 y el 15,1%; p=0,464) (figura 4).
Mortalidad en relación con la actividad asistencial de los centros en el síndrome aórtico agudo (SAA). Niveles de actividad en el SAA tipo A total y con tratamiento quirúrgico: nivel 1: ≥ 12/año; nivel 2: 6-11/año y nivel 3: <6/año. Niveles de actividad en el SAA tipo B: nivel 1: ≥ 6/año; nivel 2: 3-5/año y nivel 3: <3/año. Niveles de actividad en el SAA tipo B tratados con reparación endovascular de la aorta torácica (TEVAR): nivel 1: ≥ 6/año, nivel 2: 3-5/año y nivel 3: <3/año.
Los resultados del RESA han evidenciado en estos 15 años una significativa disminución en la mortalidad de los SAA tipo A y tipo B, coincidiendo con un aumento en el abordaje quirúrgico del SAA tipo A y el tratamiento endovascular del SAA tipo B. Tanto el tratamiento quirúrgico del SAA tipo A como el TEVAR y el tratamiento médico del SAA tipo B han disminuido su mortalidad (figura 5). A lo largo de las ediciones del RESA han aumentado la edad de los pacientes y la frecuencia de mujeres diagnosticadas de SAA. Estudios poblacionales recientes evidencian resultados similares13. A lo largo de estos 3 lustros ha disminuido la frecuencia de pacientes diagnosticados de SAA con un intervalo> 24 h desde el inicio de los síntomas, pasando del 29,7% en el RESA I al 13,5% en el RESA III. Aunque la demora en el diagnóstico no se menciona en la mayoría de las series publicadas, la precocidad del diagnóstico puede condicionar la inclusión en el registro de pacientes más inestables o con más complicaciones14,15. Nuestros resultados son muy parecidos a los del IRAD, con un tiempo de síntomas a diagnóstico de 4,3 (1,5-24) h1. Probablemente es difícil mejorar estos datos en un registro nacional con población a diversas distancias de los centros hospitalarios. Hace 15 años se recomendaba una tomografía computarizada o un ecocardiograma transesofágico, indistintamente16, para los pacientes con sospecha de SAA; el ecocardiograma transesofágico es la primera técnica diagnóstica en el 13,5% de los casos del RESA I, mientras que en el RESA III solo lo fue en el 3,4%. La tomografía computarizada se ha consolidado como la técnica más utilizada para el diagnóstico del SAA y ha aumentado del 77,1 al 84,2%. Sus principales ventajas son su exactitud diagnóstica, la capacidad de valorar toda la aorta, su rapidez y su disponibilidad. Las guías de práctica clínica de la Sociedad Europea de Cardiología17,18 recomiendan la ecocardiografía transtorácica como técnica de elección en urgencias porque a menudo permite visualizar el tabique miointimal en algunos segmentos como la raíz de la aorta, el cayado o la aorta abdominal y obtener información relevante como posibles derrame pericárdico, insuficiencia aórtica y disfunción ventricular. En este registro se observa que la ecocardiografía transtorácica aumentó la frecuencia de diagnóstico inicial de SAA, que pasó del 4,6 al 10,7% de los casos. Es previsible que esta cifra siga aumentando por el mayor uso en urgencias de la ecocardiografía transtorácica, incluida la ecoscopia.
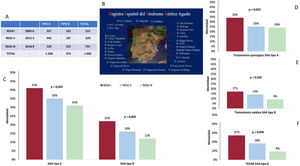
Figura central. A: número de pacientes incluidos por síndrome aórtico agudo (SAA) tipo A o B en cada una de las ediciones del RESA. B: centros participantes ubicados en España. C: evolución de la mortalidad total del SAA tipo A y tipo B. D: evolución de la mortalidad de los pacientes con SAA tipo A sometidos a tratamiento quirúrgico. E: evolución de la mortalidad de los pacientes con SAA tipo B en tratamiento médico. F: evolución de la mortalidad de los pacientes sometidos a tratamiento endovascular. TEVAR: reparación endovascular de la aorta torácica.
Uno de los aspectos más relevantes del RESA I es la alta mortalidad hospitalaria en el SAA tanto de tipo A como de tipo B. En el RESA I la mortalidad total del SAA tipo A fue del 41% y en el RESA III, del 31%. Esta significativa disminución de la mortalidad puede deberse a varios factores, como el incremento del tratamiento quirúrgico del 79,6 al 84,5% y la disminución de la mortalidad quirúrgica del 33,4 al 23,9%. Sin duda, el abordaje y el tratamiento de esta enfermedad han ganado relevancia en nuestros centros, se ha protocolizado la asistencia del paciente crítico y los cirujanos han adquirido más experiencia. En el IRAD, la mortalidad de SAA tipo A tratado con cirugía en un periodo análogo al de los RESA disminuyó del 25 al 18%. Hay que considerar que en el IRAD solo se incluyen centros de referencia con alto volumen de cirugía de aorta, y no se incluyen centros con poco volumen de actividad en esta enfermedad. Otros registros nacionales reportan mortalidades quirúrgicas del 23,1 y el 17,0%6,19. En el primer registro de disección de aorta en China (Sino-RAD)8, la mortalidad total del SAA tipo A fue del 18,1% y con tratamiento quirúrgico, solo del 5,1%. No obstante, en el Sino-RAD participaron solo 15 grandes centros que incluyeron a 1.002 pacientes con SAA tipo A en 2 años, con una media de edad de 51 años, 12 años inferior que en el RESA, por lo que se sospecharía un sesgo de inclusión. Por último, se ha publicado recientemente el registro nacional japonés (JRAD)9, que incluye la gran mayoría de centros hospitalarios del país, en el que se reporta una mortalidad del SAA tipo A tratado con cirugía del 11,8%, pero se rechazó para cirugía al 25% de los casos.
Es bien conocido que el SAA tipo B tiene menos mortalidad que el tipo A, y es de elección el tratamiento médico, excepto para los pacientes con complicaciones graves. La mortalidad total del SAA tipo B en el RESA I fue llamativamente alta (21%) comparada con la del IRAD (15%). Sin embargo, en el RESA III la mortalidad del SAA tipo B es similar a la del IRAD (12%)1. Una posible explicación para esta mejora de la supervivencia sería el incremento de la TEVAR, que pasó del 23 al 39%, y que la mortalidad por este tratamiento ha disminuido del 27 al 9%. Esta marcada disminución en la mortalidad puede explicarse porque en el RESA I la implantación de la TEVAR era muy reciente y la experiencia, muy inicial. Por otra parte, aunque la indicación de TEVAR está establecida para pacientes con complicaciones, como signos de inminente rotura de la aorta, grave inestabilidad hemodinámica o isquemia visceral-periférica, en el RESA III se ha observado la inclusión de indicaciones más laxas, como la dilatación aórtica> 45 mm y el difícil control del dolor o la presión arterial. En contraposición, el tratamiento exclusivamente médico en el SAA tipo B disminuyó del 66 al 51% y se acompañó de una disminución de su mortalidad del 17 al 9%. Centros seleccionados del IRAD evidenciaron que la mortalidad de la TEVAR en la SAA tipo B complicado era del 11%20. Ciertamente, una parte importante de los tratamientos quirúrgicos para el tipo B se han desplazado a la TEVAR21. En concordancia con otros estudios publicados8,19,22, en el RESA se observó que la mortalidad del SAA tipo A tratado mediante cirugía se asoció con el volumen de estas intervenciones en los centros, y resulta significativamente menor en los centros con 12 o más cirugías/año. Llama la atención que no se demuestren estas diferencias en relación con el SAA tipo B o el número de casos tratados con TEVAR, lo que probablemente indique que la TEVAR precisa una experiencia e infraestructura más asequibles que la cirugía abierta.
Asumiendo las limitaciones inherentes a todo registro, los resultados del presente estudio son especialmente importantes porque se obtienen de una amplia cohorte de hospitales terciarios de nuestro país. Los resultados indican que la disminución de la mortalidad hospitalaria a lo largo de los RESAS no parece relacionada con el cambio del perfil de los pacientes. Probablemente el aumento en la sospecha clínica, la protocolización de la estrategia diagnóstica y el tratamiento médico, junto con la mayor experiencia de los cirujanos tanto en cirugía abierta como en TEVAR, han podido influir en la mejora del pronóstico del SAA. En este sentido, nuevas aportaciones como la creación del Código Aorta pueden incrementar el diagnóstico de la enfermedad aórtica aguda, reducir el tiempo de traslado de los pacientes al centro de referencia y ofrecer la mayor experiencia con la concentración de las intervenciones en un reducido grupo de profesionales23.
LimitacionesLos resultados del RESA están sujetos a un inherente sesgo por la inclusión únicamente de hospitales terciarios, por lo que los resultados no pueden extrapolarse a la realidad general de esta enfermedad. En la comparación de los resultados en un periodo de 15 años, se podría argumentar que la mejora de la supervivencia pudiera deberse a un mejor perfil de los pacientes o una menor incidencia de complicaciones graves. Como puede observarse por nuestros resultados, en el RESA III hubo menos pacientes con isquemia visceral que en el RESA I, pero más casos con isquemia periférica y coma, sin diferencias en las demás complicaciones. En el RESA III se incluyeron 6 nuevos centros respecto al RESA I. No obstante, el análisis de los datos excluyendo estos nuevos centros no mostró diferencias significativas. Por la naturaleza de la recogida de los datos del registro, se disponía de la información demográfica y los antecedentes de enfermedad cardiovascular de los pacientes, pero no de otros antecedentes que pudieran influir en su pronóstico, como enfermedad pulmonar crónica, insuficiencia renal crónica o procesos oncológicos. Por último, el estudio no permitió definir con exactitud la demora en el diagnóstico del SAA de los pacientes transferidos desde hospitales no RESA cuando el intervalo era> 24 h.
CONCLUSIONESEl RESA evidencia que en estos últimos 15 años la mortalidad hospitalaria del SAA tipo A ha disminuido significativamente coincidiendo con el incremento del tratamiento quirúrgico y la disminución de la mortalidad de este. Asimismo el SAA tipo B ha disminuido su mortalidad, probablemente en relación con el aumento del tratamiento endovascular, que ha evitado la cirugía abierta, y una disminución del tratamiento exclusivamente médico para los pacientes sufren complicaciones pero sin indicación de cirugía por su complejidad y alto riesgo.
Los avances en la estrategia diagnóstica, el abordaje terapéutico y el tratamiento con cirugía abierta o endovascular se han asociado con una disminución significativa de la mortalidad del SAA en nuestro país. No obstante, estamos aún lejos de ofrecer resultados óptimos y es importante perseverar en el esfuerzo de mejorar el tratamiento de esta enfermedad y mantener registros como el RESA, que muestra el camino que queda por recorrer.
FINANCIACIÓNEste registro se ha financiado en parte por la Sociedad Española de Cardiología y Medtronic, específicamente para el desarrollo y el mantenimiento de la base de datos y los costes de publicación.
CONTRIBUCIÓN DE LOS AUTORESA. Evangelista Masip ha participado en el diseño y la redacción; A. López-Sainz en la redacción y la edición; A.J. Barros Membrilla, en la inclusión de pacientes y la revisión del manuscrito, al igual que F. Calvo Iglesias, J. López Ayerbe, M. Azqueta Molluna, V.X. Mosquera Rodríguez, F Arregui Montoya, R. Tarrío Fernández, A. Revilla Orodea, V. Sánchez Sánchez, E.M. Cantero Pérez, C. Ferrera, D. Toral Sepúlveda, F. Nistal y C. Fernández Golfín. A. Sao ha colaborado con el análisis estadístico y J. Rodríguez-Palomares, en la revisión del manuscrito y el análisis estadístico.
CONFLICTO DE INTERESESNinguno.
- –
El síndrome aórtico agudo (SAA) es un proceso agudo de la pared aórtica que se asocia con grandes morbilidad y mortalidad, por lo que se requiere un alto grado de sospecha clínica y una adecuada estrategia diagnóstica y terapéutica.
- –
El avance de las técnicas de imagen, combinado con el progreso en las técnicas quirúrgicas y endovasculares, ha modificado el diagnóstico y el tratamiento de esta enfermedad en los últimos años.
- –
Aunque diversos registros nacionales e internacionales han aportado importante conocimiento sobre el SAA, la inclusión únicamente de centros de excelencia o la diferente estructura sanitaria hacen difícil aplicar los resultados a nuestro entorno.
- –
Al comparar las 3 ediciones del Registro Español del Síndrome Aórtico (RESA), se observa un incremento de la edad y de las mujeres diagnosticadas de SAA. El diagnóstico en las primeras 24 h ha aumentado a lo largo del registro.
- –
El RESA evidencia que en estos últimos 15 años la mortalidad del SAA tipo A ha disminuido significativamente coincidiendo con una mayor frecuencia del tratamiento quirúrgico y la disminución de la mortalidad de la cirugía.
- –
El SAA tipo B ha disminuido su mortalidad probablemente por el incremento del tratamiento endovascular, que ha reducido la necesidad del tratamiento complejo con cirugía abierta, y como consecuencia de una mejor selección del tratamiento solo médico.
A los servicios de urgencias, radiología, cirugía cardiaca y cirugía vascular de cada centro, por haber brindado una excelente colaboración durante todos los años en que se ha realizado el registro.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.recesp.2022.01.014.
Los centros participantes, coordinadores y colaboradores de los centros RESA se pueden consultar en el material adicional.