Se presentan las características clínicas, los resultados y las complicaciones de todos los pacientes a los que se implantó un dispositivo de asistencia circulatoria mecánica de larga duración en España entre 2007 y 2020.
MétodosAnálisis a partir del Registro español de asistencia ventricular de larga duración (REGALAD) en el que participaron los centros españoles con programa de asistencia ventricular mecánica.
ResultadosEn este periodo se implantaron 263 dispositivos de asistencia ventricular de larga duración en 22 hospitales. En 182 pacientes (69%) la asistencia fue ventricular izquierda de flujo continuo; en 79 (30%), de flujo pulsátil (58 izquierdas y 21 biventriculares), y en 2 (1%) se implantó un corazón artificial total. El objetivo de la asistencia fue el puente al trasplante en 78 pacientes (30%), puente a la candidatura en 110 (42%), puente a la recuperación en 3 (1%) y la terapia de destino en 72 (27%). La supervivencia total a 6, 12 y 24 meses fue del 79, el 74 y el 69% respectivamente, y la mejor se consiguió con las asistencias izquierdas de flujo continuo (el 84, el 80 y el 75%). Las principales complicaciones asociadas fueron: infecciones (el 37% de los pacientes), hemorragias (35%), neurológicas (29%) y disfunción de la asistencia (17%).
ConclusionesLas asistencias ventriculares de larga duración han irrumpido en España como un tratamiento útil en la insuficiencia cardiaca avanzada. Como en otros registros internacionales, se tiende a utilizar dispositivos izquierdos intracorpóreos de flujo continuo, que se asocian con mejores resultados. Las complicaciones relacionadas siguen siendo frecuentes y graves.
Palabras clave
A pesar de los avances de los últimos años en el tratamiento de la insuficiencia cardiaca (IC), un número no despreciable de estos pacientes progresa hasta una situación de IC avanzada en la que el tratamiento médico no es suficiente para evitar el deterioro funcional, la afectación de otros órganos, los reingresos frecuentes o la muerte1.
El trasplante cardiaco (TxC) sigue siendo el tratamiento de elección en estos casos. Sin embargo, la escasez de donantes y las eventuales contraindicaciones o comorbilidades hacen que muchos pacientes no puedan acceder a este tratamiento2,3.
Los dispositivos de asistencia ventricular de larga duración (AVLD) han experimentado un rápido desarrollo en los últimos años4. Su función es dar soporte circulatorio a los pacientes con IC avanzada en lista de espera para trasplante (puente al trasplante [PT]) hasta que se resuelva una contraindicación potencialmente reversible para el trasplante (puente a la candidatura), el corazón se recupere (puente a la recuperación) o como tratamiento definitivo para pacientes no candidatos a TxC (terapia de destino).
Se presenta el primer análisis del Registro español de asistencia ventricular de larga duración (REGALAD). Este registro se constituye como una actividad delegada por la Asociación de Insuficiencia Cardiaca de la Sociedad Española de Cardiología con la colaboración de la Sociedad Española de Cirugía Cardiovascular y Endovascular, y tiene como objetivos la recogida y el análisis de las características y resultados de los procedimientos de AVLD realizados en España.
MÉTODOSRegistroEl REGALAD es un registro observacional y multicéntrico que incluye de manera retrospectiva todos los procedimientos de AVLD realizados en España desde 2007 hasta la fecha de inicio de actividad del registro (30 de noviembre de 2018) y prospectivamente a partir de entonces.
De la gestión técnica del registro se ocupa una empresa externa que actúa por delegación de la dirección del registro. Los procedimientos empleados en la recogida, el tratamiento y la comunicación de los datos se atienen a lo establecido en la Ley de Protección de Datos, incluido un consentimiento informado en los términos que establece dicha ley. Este protocolo fue aprobado por el Comité de Ética de los centros participantes.
Hospitales participantesTodos los hospitales españoles que realizan implantes de AVLD participan en este registro. En cada centro hay un responsable local médico y otro quirúrgico, que se comprometen a introducir en la base de datos online todos los procedimientos de AVLD al menos una vez al año, incluyendo los casos nuevos y actualizando la situación y las complicaciones principales de los casos antiguos. Los colaboradores del registro se detallan en el .
Dispositivos de asistencia ventricularEl REGALAD se restringe al estudio de los dispositivos conocidos como de larga duración. Se entienden por tales todos los que eventualmente permiten la autonomía y el alta hospitalaria del paciente.
Según el tipo de flujo que proporciona la bomba, se ha utilizado un modelo de AVLD de flujo pulsátil de localización paracorpórea, con posibilidad de proporcionar asistencia izquierda o biventricular, EXCOR (Berlin Heart GmbH, Alemania), y varios modelos de AVLD de flujo continuo de localización intracorpórea, para asistencia solo del ventrículo izquierdo: INCOR (Berlin Heart GmbH, Alemania), HeartMate II (Abbott, Estados Unidos) y Jarvik 2000 (Jarvik Heart Inc., Estados Unidos) proporcionan un flujo axial y HeartWare HVAD (Medtronic, Estados Unidos) y Heartmate 3 (Abbott, Estados Unidos), bombas de última generación que proporcionan un flujo continuo centrífugo. Existe también un modelo de corazón artificial total que genera flujos pulsátiles en ambos circuitos (sistémico y pulmonar): SynCardia t-TAH (Syncardia Systems LLC, Estados Unidos).
PacientesLos pacientes analizados en este trabajo son todos los adultos con IC avanzada sometidos al implante de un dispositivo de AVLD en España entre 2007 y 2020.
El REGALAD incluye la mayoría de las variables de los registros IMACS (International Society for Heart and Lung Transplantation Registry for Mechanically Assisted Circulatory Support) y EUROMACS (European Registry for Patients with Mechanical Circulatory Support), además de otras adicionales que los creadores del registro consideraron de interés. Entre estas variables figuran características demográficas, clínicas, analíticas, ecocardiográficas y hemodinámicas de los pacientes, datos del implante y datos de seguimiento a los 3 meses, al año y de cada año tras el implante. Se recogen específicamente los eventos adversos relacionados con la asistencia. En el se incluye una definición de todos estos eventos adversos.
La gravedad de la IC en el momento del implante se gradúa según la escala propuesta por INTERMACS (Interagency Registry for Mechanically Assisted Circulatory Support)5 ().
Análisis estadísticoLas variables numéricas se describen mediante media±desviación estándar o mediana [intervalo intercuartílico] según cumplieran o no la presunción de normalidad. Las variables categóricas se expresan como frecuencia absoluta y relativa. La supervivencia total se ha estimado mediante el método de Kaplan-Meier. Se siguió a los pacientes hasta su muerte o hasta el cierre del análisis el 31 de diciembre de 2020. Para este análisis de supervivencia, los pacientes fueron censurados en el momento del trasplante o el explante de la AVLD. La evolución de los pacientes se ha examinado también utilizando el análisis de riesgos competitivos de Fine y Gray, en el que se rastrean múltiples resultados mutuamente excluyentes (vivo con la asistencia, muerte, trasplante o explante). En cualquier momento, la suma de la proporción (porcentaje) de pacientes en cada categoría de resultado es igual al 100%. Con el fin de comparar la evolución en las características de los implantes y los resultados, se ha dividido el tiempo de estudio en 3 periodos (2007-2010, 2011-2015 y 2016-2020). Todos los test se realizaron a 2 colas y se consideró estadísticamente significativo un valor de p <0,05. Para los análisis se utilizaron los programas IMB SPSS Statistics 24.0 y R 4.1.2. El análisis de supervivencia y riesgos competitivos se realizó con las librerías «survival» y «cmprsk» disponibles en R.
RESULTADOSHospitales participantesLos 22 hospitales españoles con implantes de AVLD entre 2007 y 2020 participaron en el registro; de ellos, 15 tenían programa de TxC. El número de dispositivos por hospital fue muy irregular y destacaron sobre los demás 4 hospitales con más de 20 implantes por centro; estos 4 centros sumaban más de la mitad del total de la actividad realizada. La tabla 1 muestra los hospitales participantes y el número de AVLD implantadas en cada centro.
Dispositivos de asistencia ventricular implantados en España, ordenados por comunidad autónoma, provincia y hospital (2007-2020)
| Comunidad | Hospital | Dispositivos (n=263) |
|---|---|---|
| Andalucía | ||
| Córdoba | Hospital Universitario Reina Sofía de Córdoba | 1 |
| Granada | Hospital Universitario Virgen de las Nieves | 2 |
| Sevilla | Hospital Universitario Virgen del Rocío | 14 |
| Principado de Asturias | Hospital Universitario Central de Asturias | 14 |
| Islas Baleares | Hospital Universitari Son Espases | 1 |
| Cantabria | Hospital Universitario Marqués de Valdecilla | 3 |
| Castilla y León | ||
| Salamanca | Hospital Clínico Universitario de Salamanca | 8 |
| Valladolid | Hospital Clínico Universitario de Valladolid | 11 |
| Cataluña | ||
| Barcelona | Hospital Clínic i Provincial de Barcelona | 7 |
| Hospital Universitari de Bellvitge | 46 | |
| Hospital de la Santa Creu i Sant Pau | 6 | |
| Hospital Germans Trias i Pujol | 2 | |
| Comunidad Valenciana | ||
| Valencia | Hospital Universitario La Fe | 12 |
| Galicia | ||
| A Coruña | Complejo Hospitalario Universitario A Coruña | 15 |
| Pontevedra | Hospital Álvaro Cunqueiro | 4 |
| Comunidad de Madrid | Hospital Universitario 12 de Octubre | 24 |
| Hospital General Universitario Gregorio Marañón | 25 | |
| Hospital Universitario La Paz | 2 | |
| Hospital Universitario Puerta de Hierro | 48 | |
| Hospital Universitario Ramón y Cajal | 3 | |
| Región de Murcia | Hospital Clínico Universitario Virgen de la Arrixaca | 3 |
| Comunidad Foral de Navarra | Clínica Universidad de Navarra | 12 |
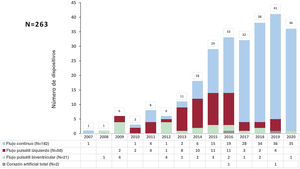
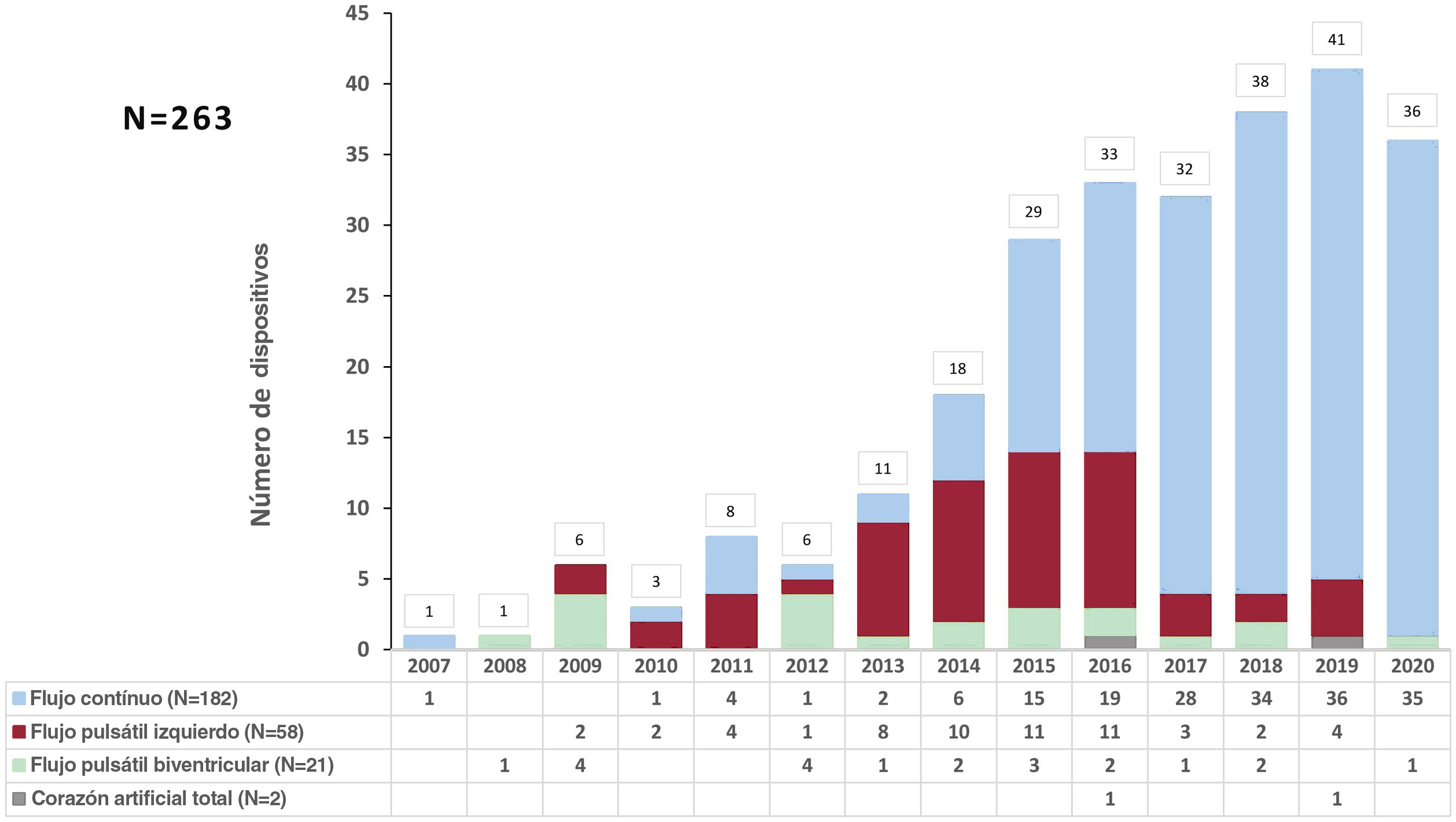
Entre 2007 y 2020 se implantaron en España 263 AVLD. En 182 pacientes (69%), la asistencia fue ventricular izquierda de flujo continuo; en 79 (30%), de flujo pulsátil (58 izquierdas, 21 biventriculares), y en 2 (1%) se implantó un corazón artificial total (figura 1). La tabla 2 muestra los diferentes modelos de AVLD utilizados, divididos por periodos.
Modelo de asistencia ventricular según periodo del implante
| 2007-2010 (n=11) | 2011-2015 (n=72) | 2016-2020 (n=180) | Total (n=263) | |
|---|---|---|---|---|
| Flujo pulsátil | ||||
| EXCOR izquierdo | 4 | 34 | 20 | 58 |
| EXCOR biventricular | 5 | 10 | 6 | 21 |
| Flujo continuo | ||||
| INCOR | 2 | 3 | 5 | |
| HeartMate II | 5 | 1 | 6 | |
| Heartware HVAD | 20 | 55 | 75 | |
| HeartMate 3 | 95 | 95 | ||
| Jarvik 2000 | 1 | 1 | ||
| Corazón artificial total | ||||
| SynCardia | 2 | 2 | ||
Las características basales de los pacientes asistidos se resumen en la tabla 3.
Características basales clínicas, ecocardiográficas y hemodinámicas de los pacientes asistidos (n=263)
| Edad (años) | 58±12 |
| Varones | 220 (84) |
| Área de superficie corporal (m2) | 1,9±0,2 |
| HTA | 141 (54) |
| Diabetes mellitus | 88 (34) |
| ACV previo | 27 (10) |
| Cirugía cardiaca previa | 29 (11) |
| Tipo de cardiopatía | |
| Cardiopatía isquémica | 134 (51) |
| Miocardiopatía dilatada no isquémica | 91 (35) |
| Miocardiopatía hipertrófica | 9 (3) |
| Miocarditis | 8 (3) |
| Miocardiopatía por tóxicos | 7 (3) |
| Valvulopatía | 5 (2) |
| Otras | 9 (3) |
| Tiempo desde el diagnóstico de IC | |
| <1 mes | 15 (6) |
| 1 mes-1 año | 26 (10) |
| >1 año | 220 (84) |
| Necesidad de inotrópicos ambulatorios | 69 (26) |
| Portador de DAI | 207 (79) |
| Portador de TRC | 78 (31) |
| Objetivo inicial de la asistencia | |
| Puente al trasplante | 78 (30) |
| Puente a la candidatura | 110 (42) |
| Puente a la recuperación | 3 (1) |
| Terapia de destino | 72 (27) |
| Tratamiento en las 48 h previas al implante | |
| Infusión de inotrópicos | 176 (68) |
| Balón de contrapulsación intraaórtico | 38 (14) |
| Otra asistencia circulatoria | 22 (8) |
| Respirador | 15 (6) |
| Diálisis/ultrafiltración | 3 (1) |
| Parámetros analíticos en las 24 h previas al implante | |
| Creatinina (mg/dl) | 1,3±0,5 |
| GOT/AST (U/l) | 35±48 |
| Bilirrubina (mg/dl) | 1,2±0,9 |
| Albúmina (mg/dl) | 3,8±0,6 |
| NT-proBNP (pg/ml) | 4.567 (2.587-8.286) |
| Plaquetas (×10/μl) | 201±74 |
| INR | 1,3±0,4 |
| Parámetros ecocardiográficos | |
| DTDVI (cm) | 6,8±1,0 |
| FEVI (%) | 23±7 |
| TAPSE (mm) | 15±4 |
| Disfunción del VD moderada o grave | 88 (34) |
| Insuficiencia mitral moderada o grave | 172 (65) |
| Insuficiencia tricuspídea moderada o grave | 106 (40) |
| Insuficiencia aórtica moderada o grave | 14 (5) |
| Parámetros hemodinámicos | |
| PVC (mmHg) | 11±6 |
| PAPs (mmHg) | 55±18 |
| PAPm (mmHg) | 36±12 |
| PCP (mmHg) | 23±8 |
| GTP (mmHg) | 13±8 |
| GC (l/min/m2) | 4,1±1,1 |
| IxC (l/min/m2) | 2,2±0,6 |
| RVP (UW) | 3,3±2,3 |
| ITVD (mmHg/ml/m2) | 774±456 |
| INTERMACS en el momento del implante | |
| 1 | 15 (6) |
| 2 | 41 (15) |
| 3 | 116 (44) |
| 4 | 70 (27) |
| > 4 | 20 (8) |
ACV: accidente cerebrovascular; AST: aspartato aminotransferasa; DAI: desfibrilador automático implantable; DTDVI: diámetro telediastólico del ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo; GC: gasto cardiaco; GOT: transaminasa glutámico-oxalacética; GTP: gradiente transpulmonar; HTA: hipertensión arterial; IC: insuficiencia cardiaca; INR: razón internacional normalizada; INTERMACS: Registro Interinstitucional de Dispositivos de Asistencia Circulatoria Mecánica; ITVD: índice de trabajo del ventrículo derecho; IxC: índice cardiaco; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; PAPm: presión arterial pulmonar media; PAPs: presión arterial pulmonar sistólica; PCP: presión capilar pulmonar; PVC: presión venosa central; RVP: resistencia vascular pulmonar; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo; TRC: terapia de resincronización cardiaca; VD: ventrículo derecho.
Los valores continuos se expresan como n (%) y los categóricos, como media±desviación estándar o mediana [intervalo intercuartílico].
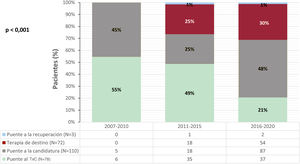
El objetivo inicial de la AVLD fue el PT en 78 pacientes (30%), con una mediana de tiempo en lista de espera de 61 [21-228] días antes del implante de la asistencia. En 110 pacientes (42%) la AVLD se implantó como puente a la candidatura; en ellos la hipertensión pulmonar (61 pacientes, 55%) y el antecedente de cáncer reciente (11 pacientes, 10%) fueron las principales contraindicaciones para el TxC. En los 72 pacientes (27%) cuyo objetivo de la AVLD fue el terapia de destino, las contraindicaciones más señaladas fueron la edad avanzada (47 pacientes, 65%) y la insuficiencia renal (22 pacientes, 31%). Solo en 3 pacientes (1%) la asistencia se implantó como puente a la recuperación. La evolución del objetivo inicial según la época del implante se muestra en la figura 2.
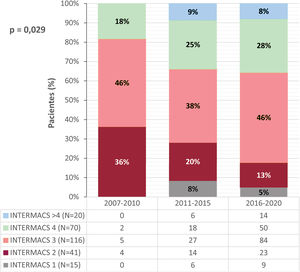
Todos los pacientes cumplían criterios de IC avanzada y la mayoría tenían perfiles de riesgo INTERMACS 3 (44%) o 4 (27%) en el momento del implante. La evolución del perfil de riesgo según la época del implante se muestra en la figura 3.
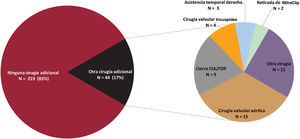
Características de la cirugía de implante de la asistenciaEn 250 pacientes (95%) la cirugía se hizo con circulación extracorpórea. El acceso quirúrgico fue la esternotomía media en el 93% de los casos, toracotomía izquierda en el 2% y cirugía mínimamente invasiva en el 5%. En 44 pacientes (17%) se asoció alguna otra cirugía cardiaca; la más frecuente fue la cirugía valvular aórtica (figura 4).
Evolución de los pacientes durante la hospitalización del implante de la asistenciaDe los 263 pacientes asistidos, 190 (72%) recibieron el alta tras una mediana de 36 [20-64] días, 44 (17%) fallecieron y 27 (10%) recibieron un TxC durante la hospitalización tras 77 [33-121] días. En 23 (85%) de los 27 casos trasplantados, las asistencias eran bombas pulsátiles con eventos u otros condicionantes que «obligaron» a mantener al paciente hospitalizado hasta el TxC. En 2 casos (1%) aparecieron complicaciones derivadas de la AVLD que hicieron necesario explantar la bomba.
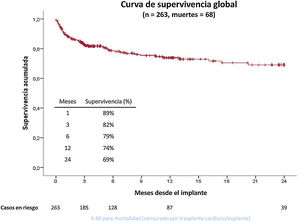
Supervivencia de los pacientesLa supervivencia total de los pacientes tras un seguimiento medio de 358 —mediana, 173 [83-430]— días fue del 89, el 82, el 79, el 74 y el 69% a 1, 3, 6, 12 y 24 meses (figura 5).
La figura 6 muestra la supervivencia en función del tipo de asistencia y del objetivo inicial del implante. La mejor supervivencia se consiguió con las asistencias izquierdas de flujo continuo (el 92, el 87, el 84, el 80 y el 75% a 1, 3, 6, 12 y 24 meses) frente a las izquierdas de flujo pulsátil (el 82, el 74, el 62 y el 31% a 1, 3, 6 y 12 meses) y frente a las biventriculares/corazón artificial total (el 91, el 71 y el 56% a 1, 3 y 6 meses).
Complicaciones de los pacientesDurante el seguimiento se registraron 611 complicaciones mayores (2,3 eventos/paciente) relacionadas con la asistencia ventricular (tabla 4).
Complicaciones mayores relacionadas con la asistencia ventricular
| Eventos | Pacientes, n | Pacientes, % | Incidencia (cada 100 pacientes-mes) | |
|---|---|---|---|---|
| Hemorragia mayor | 151 | 91 | 35 | 6,05 |
| Mediastino-tórax | 60 | |||
| Digestivo | 57 | |||
| Pleural-pulmonar | 14 | |||
| ORL-dental | 6 | |||
| Intraabdominal | 4 | |||
| Urinario | 3 | |||
| Otros | 7 | |||
| Infección mayor | 139 | 98 | 37 | 5,74 |
| Específica de la asistencia | 60 | |||
| Relacionada con la asistencia | 14 | |||
| No relacionada con la asistencia | 65 | |||
| Disfunción neurológica | 113 | 76 | 29 | 4,30 |
| AIT | 37 | |||
| Ictus isquémico | 47 | |||
| Ictus hemorrágico | 21 | |||
| Otras | 8 | |||
| Disfunción de la asistencia | 56 | 45 | 17 | 2,0 |
| Disfunción de la bomba | 45 | |||
| Trombosis de la bomba es un subtipo de disfunción de la bomba | 26 | |||
| Disfunción del cable de conducción percutáneo | 3 | |||
| Disfunción de otro componente | 8 | |||
| Insuficiencia cardiaca derecha | 52 | 49 | 19 | 1,88 |
| IC leve | 23 | |||
| IC moderada | 23 | |||
| IC grave | 6 | |||
| Insuficiencia respiratoria | 15 | 14 | 5 | 0,50 |
| Desarrollo de anticuerpos anti-HLA | 6 | 6 | 2 | 0,20 |
| Tromboembolia arterial sin afección del SNC | 2 | 2 | 1 | 0,07 |
| Otro tipo de evento | 77 | 55 | 21 | 2,89 |
AIT: accidente isquémico transitorio; IC: insuficiencia cardiaca; HLA: antígeno leucocitario humano; ORL: otorrinolaringológico; SNC: sistema nervioso central.
La complicación más referida fue la hemorragia mayor. En la primera semana tras el implante, los sangrados más frecuentes fueron los relacionados con la propia cirugía, y más tarde, las hemorragias digestivas.
La segunda complicación más señalada fue la infección mayor. El 47% de las infecciones no tuvieron relación directa con la asistencia, la mayoría fueron respiratorias o urinarias. Un 43% fueron infecciones específicas de la asistencia, sobre todo infecciones del cable de conducción percutáneo que conecta la bomba intracorpórea con el controlador externo o de las cánulas percutáneas en el caso de las bombas paracorpóreas. El 10% restante de las infecciones estaban relacionadas con la asistencia, aunque no eran específicas de esta (mediastinitis, bacteriemias y endocarditis bacterianas).
Otras complicaciones menos frecuentes, pero más graves, fueron las neurológicas, que hasta en 26 pacientes (el 34% de los casos) resultaron fatales: 12 pacientes fallecieron como consecuencia de un ictus isquémico tras una mediana de 15 [5-66] días y 12 pacientes, por un ictus hemorrágico tras 162 [33-236] días. En otros 10 pacientes (13%) la complicación neurológica dejó secuelas graves.
La disfunción de la AVLD más repetida fue la trombosis de la bomba, que se presentó en 26 ocasiones y afectó al 5% de los pacientes con asistencias de flujo continuo y al 11% de las asistencias pulsátiles. En la mayoría de los casos se solucionó intensificando el tratamiento antitrombótico o cambiando los ventrículos paracorpóreos, aunque en 3 pacientes con trombosis graves y/o repetidas se llegó a explantar la bomba y conectar al paciente a una asistencia circulatoria temporal como puente a un TxC urgente. El 21% de todas las disfunciones de asistencia fueron motivo para poner al paciente en lista urgente de TxC.
Tras el implante de la asistencia, 49 pacientes (19%) presentaron algún grado de IC derecha. La mayoría se controló con tratamiento médico, aunque 6 pacientes necesitaron asistencia circulatoria derecha temporal y 2 de ellos acabaron falleciendo por este motivo.
Cuando se comparan las tasas de complicaciones según el tipo de AVLD (izquierda continua frente a izquierda pulsátil y frente a biventricular/corazón artificial), se observa que —excepto en el caso de la IC derecha, que obviamente ya se previene con las asistencias biventriculares— los demás eventos fueron menos frecuentes en el primer grupo de pacientes (tabla 5).
Complicaciones mayores según el tipo de asistencia ventricular (incidencia cada 100 pacientes-mes)
| Izquierda continua (n=182) | Izquierda pulsátil (n=58) | Biventricular/corazón artificial total (n=23) | p | |
|---|---|---|---|---|
| Hemorragia mayor | 5,15 | 13,89 | 26,72 | <0,001 |
| Infección mayor | 4,82 | 15,58 | 16,70 | <0,001 |
| Disfunción neurológica | 2,54 | 30,55 | 7,92 | <0,001 |
| Disfunción de la asistencia | 1,13 | 13,06 | 9,53 | <0,001 |
| Trombosis de la bomba | 0,51 | 6,53 | 4,08 | <0,001 |
| Insuficiencia cardiaca derecha | 1,74 | 5,24 | 0 | 0,01 |
| Insuficiencia respiratoria | 0,40 | 0,60 | 3,73 | 0,01 |
| Desarrollo de anticuerpos anti-HLA | 0,07 | 1,18 | 2,52 | 0,01 |
| Otro tipo de evento | 2,72 | 4,52 | 5,11 | — |
HLA: antígeno leucocitario humano.
El 31 de diciembre de 2020, de los 263 pacientes incluidos en el registro, 101 (38%) habían recibido un TxC tras una mediana de 159 [105-321] días, 90 (34%) seguían vivos con la asistencia tras 173 [83-430] días, 68 (26%) habían fallecido tras 51 [18-178] días y en 4 pacientes (2%) se había explantado la asistencia (3 por disfunción de la bomba y 1 por haberse recuperado de la cardiopatía).
Cabe señalar que, del subgrupo de 110 pacientes asistidos inicialmente como puente a la candidatura, 58 (53%) acabaron trasplantados, 23 (21%) fallecieron y 29 (26%) seguían vivos con la asistencia al final del seguimiento, 15 (14%) de estos en lista de espera de TxC.
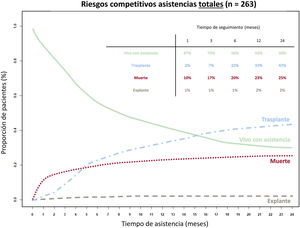
La figura 7 representa la evolución de los pacientes durante los primeros 2 años tras el implante. En la se muestra la evolución de los pacientes según el tipo de asistencia implantada.
La principal causa de fallecimiento fue la complicación neurológica (el 38% de las muertes). El resto de causas de fallecimiento se resumen en la tabla 6.
Causa primaria de fallecimiento de los pacientes asistidos
| Causa primaria del fallecimiento | n (%) |
|---|---|
| Disfunción neurológica | 26 (38) |
| Fracaso multiorgánico | 9 (13) |
| Hemorragia | 7 (10) |
| Insuficiencia cardiaca refractaria | 6 (9) |
| Infección mayor | 4 (6) |
| Insuficiencia respiratoria | 4 (6) |
| Disfunción de la asistencia | 3 (4) |
| Cáncer | 2 (3) |
| Otras | 7 (10) |
| Total | 68 (100) |
Este trabajo es el primer informe del REGALAD y recoge la información completa de todas las AVLD implantadas en España entre 2007 y 2020.
Al igual que en otros registros internacionales, el número de dispositivos implantados ha ido aumentando progresivamente desde su inicio hasta el año 2020, en el que hubo un pequeño retroceso en probable relación con la pandemia de COVID-19. Por otro lado, nuestros números anuales son significativamente inferiores a los de otros países. Como ejemplo, basándonos en los datos del registro INTERMACS6, sabemos que en 2019 se implantaron en Estados Unidos 9,7 dispositivos de AVLD por millón de habitantes frente a 0,8 en España. Es posible que esta enorme diferencia esté condicionada por la relativa facilidad para acceder en poco tiempo a un TxC en España. Esto, junto con el alto porcentaje de pacientes a los que se trasplanta de manera urgente con asistencia circulatoria de corta duración7, explicaría sobre todo el escaso número de AVLD como PT de nuestro registro. Sin embargo, esta estrategia es muy discutida con base en sus dudosos resultados8,9. El cambio reciente de la normativa para la priorización de los receptores en Estados Unidos ha tenido este mismo efecto controvertido de facilitar los TxC urgentes con asistencia circulatoria temporal y reducir el número de implantes de AVLD como PT, pero a expensas de un aumento de la mortalidad tras el TxC10.
Otra de las razones para el escaso crecimiento de las AVLD en España es el desconocimiento que aún existe en nuestro medio sobre este tratamiento y sus resultados, lo cual hace que muchos de los pacientes que podrían beneficiarse no sean derivados a centros especializados. Esto, unido a la falta de unos resultados de coste-efectividad favorables, puede influir considerablemente en la lenta incorporación de este tratamiento al sistema público español, sobre todo como terapia de destino.
En cuanto al momento del implante de la AVLD, llama la atención la escasa indicación en perfiles INTERMACS graves 1 o 2 (solo el 21% de los casos en nuestra serie) frente al registro estadounidense (51%)6. Quizás esto tenga que ver con la dificultad logística y el «respeto» que aún existe en la mayoría de los centros españoles a la hora de implantar de urgencia una AVLD, que clásicamente se ha acompañado de peores resultados11. Para estos pacientes críticos, muchos optan por instaurar inicialmente una asistencia circulatoria de corta duración como puente a una AVLD (estrategia bridge to bridge); de hecho, 22 pacientes (8%) de nuestra serie tenían una asistencia mecánica temporal (8 ECMO, 6 Impellas y 8 Centrimag) en el momento del implante de la AVLD. Estos pacientes no tuvieron más eventos ni peor supervivencia que el resto de los pacientes del registro.
También en el REGALAD se confirma que el sexo masculino (84%) predomina entre la población con IC tratada con terapias avanzadas, al igual que ocurre en otros registros de AVLD como INTERMACS (79%)6 o EUROMACS (82%)12 y de TxC como el propio Registro Español de Trasplante Cardiaco (75%)7.
Los dispositivos paracorpóreos pulsátiles utilizados antiguamente han dado paso a los intracorpóreos de flujo continuo, más pequeños, con menor consumo de energía y más duraderos, por lo que pueden utilizarse como tratamiento definitivo. Estos dispositivos acarrean menor tasa de complicaciones, pero tienen la limitación de su mayor coste y la dificultad para asistir al ventrículo derecho. El dispositivo que predomina en los últimos 3 años es el HeartMate 3, lo que probablemente será la tónica en el futuro próximo, ya que el otro modelo similar que estaba en el mercado (HVAD, Heartware) detuvo su venta y distribución en junio 2021 por una mayor tasa de eventos adversos13. Nuestra experiencia con los corazones artificiales totales es anecdótica, debido a que aún conllevan gran complejidad en el implante, poca durabilidad y múltiples complicaciones14.
Los resultados de los pacientes incluidos en el REGALAD están lastrados por un alto porcentaje de dispositivos de flujo pulsátil y asistencias biventriculares, así como por la participación de centros con implantes muy irregulares y esporádicos, con escasa experiencia y falta de curva de entrenamiento. Aun así, la supervivencia general (el 74 y el 69% a 1 y 2 años) no es peor que la mostrada en otros registros internacionales similares, como por ejemplo el registro EUROMACS, que recoge 2.268 pacientes y muestra supervivencias del 69% al año y el 55% a los 2 años12. Si nos restringimos al subgrupo de pacientes con AVLD izquierda aislada de flujo continuo, nuestros resultados (supervivencia del 80% a 1 año y el 75% a 2 años) tampoco tienen nada que envidiar a los de otros registros internacionales como el INTERMACS, que recoge 25.551 AVLD izquierdas de flujo continuo, implantadas entre 2010-2019, y muestra supervivencias del 82% al año y el 73% a los 2 años6.
Podría llamar la atención que en nuestra serie no se observen diferencias significativas en la supervivencia cuando se comparan los diferentes objetivos por los que se implantó la asistencia, como sí ocurre en otros registros6,12. En general, es lógico pensar que los pacientes con AVLD como PT o como puente a la candidatura, que son más jóvenes y tienen menos comorbilidades, deberían conseguir mejores supervivencias que los que reciben la asistencia como terapia de destino. Es probable que la explicación esté precisamente en que la gran mayoría de las asistencias de flujo pulsátil y biventriculares, que son las que muestran peores resultados, se implantaron con este objetivo de asistir a los pacientes hasta el TxC15.
Las complicaciones ocurridas a estos pacientes siguen siendo frecuentes y graves, algunas pueden causar la muerte o una discapacidad permanente, a menudo requieren hospitalizaciones, empeoran la percepción de la calidad de vida y son hoy por hoy el principal obstáculo para que este tratamiento se expanda.
El ictus, tanto isquémico como hemorrágico, es la complicación más temida por sus secuelas y por ser la principal causa de muerte de estos pacientes (hasta el 38% de las muertes de nuestra serie). Por fortuna, con la identificación de sus factores de riesgo y las medidas de prevención como el control estricto de la presión arterial y, por supuesto, con la aparición de nuevas AVLD más hemocompatibles, esta complicación se ha reducido muy significativamente.
También nuestro registro muestra una disminución progresiva de la disfunción de la asistencia. De estas disfunciones, la más característica y grave es la trombosis de la bomba, que ocurrió en el 7% de nuestros pacientes, sobre todo con las bombas pulsátiles paracorpóreas, y obliga a su sustitución en más de la mitad de los casos.
Precisamente para prevenir las complicaciones tromboembólicas, la mayoría de estos pacientes reciben tratamiento antitrombótico doble, lo que a su vez favorece la aparición de eventos hemorrágicos. Especialmente típicas a largo plazo son las hemorragias digestivas, que afectaron hasta al 19% de los pacientes de nuestra serie. Los resultados del estudio ARIES HM3 mostrará si es posible prescindir de la antiagregación en pacientes con bajo riesgo trombótico seleccionados16.
Las infecciones son la otra complicación más frecuente; muchas son similares a las de cualquier posoperatorio de cirugía cardiaca, pero algo específico de estos pacientes son las infecciones de las cánulas que salen a través de la piel en las bombas paracorpóreas y del cable de conducción en las asistencias intracorpóreas. Estas infecciones, una vez que aparecen, son difíciles de suprimir, obligan a mantener tratamientos antibióticos prolongados y empeoran la calidad de vida17. Como el resto de complicaciones, también estas muestran una tendencia a reducirse con los dispositivos de última generación.
La colaboración entre la tecnología y la medicina en los últimos años ha hecho que se estén desarrollando dispositivos mecánicos cada vez más eficaces y seguros para proporcionar asistencia circulatoria duradera a los pacientes con IC avanzada. Necesitamos seguir avanzando hacia dispositivos más sencillos, que puedan usarse en fases tempranas de la IC para facilitar la recuperación, dispositivos fabricados con materiales hemocompatibles para disminuir la necesidad de anticoagulación, que puedan prescindir de cables percutáneos y tengan la capacidad de adaptarse a las necesidades fisiológicas de los pacientes.
El presente registro demuestra que las AVLD son ya una realidad y, aunque aún existe mucho desconocimiento acerca de su utilidad y sus indicaciones, su uso se está generalizando. Estos dispositivos aún distan mucho de la perfección y de convertirse en la solución definitiva para los pacientes con IC avanzada.
LimitacionesLas principales limitaciones de este registro, si se compara con otros registros internacionales, son el reducido número de pacientes que incluye y el seguimiento relativamente corto. Sin embargo, es un registro exhaustivo, ya que contiene todos los procedimientos consecutivos practicados desde que se empezaron a implantar estos dispositivos en España.
CONCLUSIONESLas AVLD se han establecido en España en los últimos años como tratamiento útil para pacientes seleccionados con IC avanzada. Como en otros registros internacionales, se tiende hacia el uso de dispositivos izquierdos intracorpóreos de flujo continuo, que son los que logran los mejores resultados. Las complicaciones siguen siendo frecuentes y graves, y muchas están relacionadas con la hemocompatibilidad de los dispositivos.
FINANCIACIÓNNinguno.
CONTRIBUCIÓN DE LOS AUTORESTodos los autores han contribuido por igual en la recolección de datos para este trabajo y en la revisión del manuscrito final.
CONFLICTO DE INTERESESM. Gómez-Bueno ha recibido honorarios por charlas y consultoría de Abbott; M.D. García-Cosío ha recibido becas para gastos de inscripción y viajes a congresos de Epycardio; E. Barge-Caballero ha recibido honorarios por charlas y consultoría de Abbott; D. Rangel ha recibido becas para gastos de inscripción y viajes a congresos de Abbott y Medtronic; A. Uribarri ha recibido honorarios por consultoría de Abbott; M.A. Castel ha recibido becas para gastos de inscripción y viajes a congresos de Epycardio y Abbott; P. Codina ha recibido pagos por charlas de Abbott; J. González-Costello ha recibido honorarios por charlas y consultoría de Abbott. El resto de los autores no tienen conflictos de intereses en relación con este trabajo.
- –
Las asistencias ventriculares de larga duración son parte del tratamiento actual de la insuficiencia cardiaca avanzada y se utilizan con el objetivo de proporcionar asistencia circulatoria hasta el trasplante cardiaco o como tratamiento definitivo para pacientes con contraindicaciones para el trasplante.
- –
Se presentan las características y los resultados de todos y cada uno de los procedimientos de asistencia ventricular realizados en España desde que se comenzó a implantar este tipo de dispositivos.
- –
Como en otros registros internacionales, se confirma que en los últimos años se ha ido evolucionando hacia dispositivos intracorpóreos de flujo continuo, que son más duraderos, generan menores tasas de complicaciones y logran las mejores supervivencias.