El implante percutáneo de la válvula aórtica se ha consolidado como tratamiento de la estenosis aórtica grave inoperable o de alto riesgo quirúrgico. Recientemente las indicaciones se han ampliado a riesgo intermedio y bajo. Nuestro objetivo es evaluar la eficiencia de SAPIEN 3 frente al tratamiento médico conservador (TMC) o el reemplazo quirúrgico de válvula aórtica (RVA) en pacientes sintomáticos inoperables con riesgo alto e intermedio.
MétodosAnálisis de coste-efectividad de SAPIEN 3 frente a RVA/TMC mediante un modelo de Markov (ciclos mensuales) adaptado con 8 estados definidos por la New York Hearth Association y resultados a 15 años, incluidos las complicaciones mayores y el tratamiento tras el alta hospitalaria, desde la perspectiva del Sistema Nacional de Salud. Los parámetros de efectividad se basan en los estudios PARTNER. Se incluyeron costes sanitarios (en euros de 2019) derivados del procedimiento, hospitalización, complicaciones clínicas y seguimiento. Se aplicó una tasa de descuento anual del 3% en costes y beneficios. El análisis de sensibilidad fue determinístico y probabilístico (Monte Carlo).
ResultadosEn comparación con el RVA (riesgo alto e intermedio) y el TMC (inoperables), el SAPIEN 3 implicó mejores resultados en las 3 poblaciones y menor estancia. Las tasas de coste-utilidad incremental fueron 5.471 (riesgo alto), 8.119 (riesgo intermedio) y 9.948 (inoperables) euros/años de vida ajustados por calidad ganados. En el análisis probabilístico, el SAPIEN 3 resultó coste-efectivo por encima del 75% de las simulaciones en los 3 perfiles.
ConclusionesEn nuestro medio, el SAPIEN 3 permite un tratamiento eficiente de la estenosis aórtica grave tanto en pacientes inoperables como en riesgo alto e intermedio.
Palabras clave
La estenosis aórtica (EA) es la enfermedad valvular más frecuente en Europa (41,2%), de origen degenerativo en su mayoría, reumático o congénito1–4. Al principio los pacientes permanecen asintomáticos, pero el incremento de su gravedad causa síntomas e incluso muerte súbita5. Además, la morbimortalidad puede aumentar en los asintomáticos con velocidades de flujo aórtico> 4 m/s6 o con enfermedades asociadas7–10.
En España, un 7% de los mayores de 85 años padece EA11 y la tasa anual de prevalencia es del 4,4% en los mayores de 65. De estos, un 68% podría necesitar cirugía o implante percutáneo de válvula aórtica (TAVI)12, por lo que tiene un impacto creciente en la salud pública.
La evaluación de las tecnologías sanitarias es un pilar básico para la toma de decisiones en la asignación de recursos que garantice la calidad de la provisión de los servicios y la sostenibilidad del sistema13. A tal fin, el análisis de coste-efectividad es en una herramienta útil en la toma de decisiones13. El análisis de coste-utilidad, una forma de análisis de coste-efectividad que utiliza años de vida ajustados por calidad (AVAC) como una medida de efectividad, tiene en cuenta el valor que las personas asignan a los estados de salud14. Se llevan a cabo normalmente a través de una modelización de la realidad clínica, a partir de la perspectiva de interés en el análisis15.
En los últimos años, el TAVI se ha convertido en el tratamiento de elección para pacientes con EA grave y sintomática que son inoperables o presentan un alto riesgo quirúrgico, y ha mejorado la supervivencia y la capacidad funcional según las clases de la New York Heart Association (NYHA). Además, es un procedimiento menos invasivo que la cirugía valvular. Asimismo, el empleo de las últimas innovaciones, como el dispositivo SAPIEN 3 (S3) (Edwards Lifesciences, Estados Unidos), se está considerando para pacientes con riesgo quirúrgico intermedio e incluso bajo por los resultados de recientes estudios16–18.
Debido al interés que profesionales sanitarios y pacientes muestran por el TAVI, esta tecnología viene siendo objeto de evaluaciones que persiguen potenciar su uso eficiente19–21. Nuestro objetivo es realizar una evaluación económica completa del S3 en pacientes inoperables (PI) y con riesgo alto (PRA) e intermedio (PRI) en comparación con la alternativa de tratamiento en cada caso (tratamiento médico conservador [TMC] o reemplazo quirúrgico de la válvula aórtica [RVA]), incorporando las evidencias clínicas recientes y los costes sanitarios de nuestro país.
MÉTODOSSe parte de un modelo matemático de Markov que permite el análisis comparativo en las 3 poblaciones de interés: PI, PRA y PRI. El comparador en cada caso fue el TMC (farmacológico) en los PI y el RVA en los PRI o PRA.
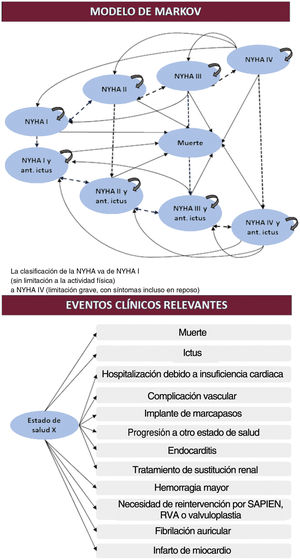
El modelo, descrito en publicaciones recientes22,23, considera las características de las cohortes de pacientes equivalente a la de los ensayos clínicos PARTNER24, PARTNER 125 y PARTNER 216,26,27, y se nutre de sus resultados. Estos hallazgos se emplearon para definir la progresión en el tiempo, con 4 niveles de estado funcional a partir del instrumento NYHA y la ocurrencia de ictus. Así, los pacientes podían localizarse en cualquiera de 9 estados excluyentes, que podían cambiar en ciclos mensuales, salvo en caso de fallecimiento (figura 1).
El horizonte temporal de 15 años considera toda la vida de los pacientes candidatos a TAVI, con una media de edad> 65 años12,18,25,28. No obstante, el modelo permite análisis anuales, siempre siguiendo la perspectiva del Sistema Nacional de Salud. Se tuvieron en cuenta los recursos relacionados con la intervención (actuaciones previas y procedimiento percutáneo o su alternativa terapéutica), además del tratamiento durante el seguimiento según clase NYHA y el abordaje de potenciales eventos adversos.
Para cada alternativa comparada, se estimaron los costes sanitarios, los años de vida ganados (AVG) y los AVG ajustados por calidad (AVAC). De esta forma, se estimaron las variables de resultado de la evaluación económica: el cociente de coste-efectividad incremental y el de coste-utilidad incremental (CCUI) en cada población. El cálculo de estos cocientes es como sigue:
Cociente de coste-efectividad incremental(poblaciónx)=(Coste S3(poblaciónx) – Coste alternativa(poblaciónx)) / (AVG S3(poblaciónx) – AVG alternativa(poblaciónx)), expresado en euros/AVG.
CCUI(poblaciónx)=(Coste S3(poblaciónx) – Coste alternativa(poblaciónx)) / (AVAC S3(poblaciónx) – AVAC alternativa(poblaciónx)), expresado en euros/AVAC.
Los resultados expresan el coste incremental que implicaría la S3 para conseguir una unidad adicional de beneficio (AVG o AVAC) frente a su comparador, en cada población (PRI, PRA, PI).
Se considera que una tecnología es coste-efectiva cuando el resultado se sitúa por debajo de los umbrales definidos (máximo de 30.000 euros/AVAC).
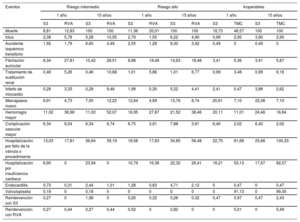
Parámetros y probabilidades de transiciónEl modelo considera durante el seguimiento el riesgo de muerte y de una serie de eventos o complicaciones recogidos en trabajos previos19–21. El riesgo se definió a partir de los ensayos PARTNER, siguiendo los criterios VARC-229: mortalidad, accidente cerebrovascular, infarto de miocardio, accidente isquémico transitorio, fibrilación auricular, tratamiento de sustitución renal, necesidad de marcapasos, hemorragia mayor, complicación vascular, hospitalización por insuficiencia cardiaca y reintervención (tabla 1).
Resultados clínicos por perfil de riesgo y alternativa de intervención
| Eventos | Riesgo intermedio | Riesgo alto | Inoperables | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 año | 15 años | 1 año | 15 años | 1 año | 15 años | |||||||
| S3 | RVA | S3 | RVA | S3 | RVA | S3 | RVA | S3 | TMC | S3 | TMC | |
| Muerte | 8,81 | 12,83 | 100 | 100 | 11,36 | 20,01 | 100 | 100 | 18,73 | 46,57 | 100 | 100 |
| Ictus | 2,38 | 5,78 | 5,28 | 10,55 | 2,79 | 1,55 | 6,22 | 4,90 | 0,99 | 2,95 | 3,90 | 2,95 |
| Accidente isquémico transitorio | 1,92 | 1,79 | 6,60 | 4,49 | 2,55 | 1,28 | 8,30 | 3,92 | 0,49 | 0 | 0,49 | 0 |
| Fibrilación auricular | 6,34 | 27,81 | 10,42 | 28,51 | 8,88 | 18,48 | 14,63 | 18,48 | 3,41 | 5,36 | 3,41 | 5,87 |
| Tratamiento de sustitución renal | 0,46 | 5,26 | 0,46 | 10,68 | 1,01 | 5,86 | 1,01 | 6,77 | 0,99 | 3,48 | 0,99 | 6,16 |
| Infarto de miocardio | 0,28 | 3,33 | 0,28 | 9,46 | 1,99 | 0,30 | 5,22 | 4,41 | 2,41 | 0,47 | 3,86 | 2,62 |
| Marcapasos nuevo | 6,91 | 4,73 | 7,50 | 12,22 | 12,64 | 4,69 | 13,76 | 8,74 | 20,61 | 7,10 | 22,06 | 7,10 |
| Hemorragia mayor | 11,02 | 36,98 | 11,02 | 52,07 | 16,95 | 27,87 | 21,52 | 38,46 | 20,11 | 11,01 | 24,46 | 16,64 |
| Complicación vascular mayor | 6,34 | 6,04 | 6,34 | 6,74 | 6,75 | 3,91 | 7,88 | 3,91 | 6,40 | 2,02 | 6,40 | 2,02 |
| Hospitalización por fallo de la válvula o procedimiento | 13,03 | 17,81 | 36,64 | 39,19 | 18,58 | 17,83 | 34,85 | 56,48 | 22,75 | 61,68 | 25,66 | 100,33 |
| Hospitalización por insuficiencia cardiaca | 6,90 | 0 | 23,94 | 0 | 10,79 | 16,38 | 22,32 | 26,41 | 16,21 | 53,13 | 17,67 | 82,07 |
| Endocarditis | 0,73 | 0,31 | 2,44 | 1,01 | 1,28 | 0,63 | 4,71 | 2,12 | 0 | 0,47 | 0 | 0,47 |
| Valvuloplastia | 0,18 | 0 | 0,18 | 0 | 0 | 0 | 0 | 0 | 0 | 91,13 | 0 | 99,30 |
| Reintervención con S3 | 0,27 | 0 | 1,98 | 0 | 0,26 | 0,32 | 0,26 | 0,32 | 0,47 | 0,97 | 0,47 | 2,43 |
| Reintervención con RVA | 0,27 | 0,44 | 0,27 | 0,44 | 0,52 | 0 | 2,82 | 0 | 0 | 5,01 | 0 | 5,49 |
RVA: reemplazo quirúrgico válvula aórtica; S3: SAPIEN 3; TMC: tratamiento médico conservador.
Los valores expresan porcentaje.
Las probabilidades de transición para S3 se definieron con los datos clínicos disponibles de hasta 12 meses de seguimiento. Por su parte, para el RVA se dispuso de información a 2 años de los PRI y 5 años para los PRA. Con esta base, las proyecciones de mortalidad se realizaron (hasta una supervivencia del 0% en cada alternativa) siguiendo una función log lineal y distribución de Weibull de los PRI y PRA respectivamente. La elección de las funciones se basó en pruebas de bondad de ajuste (criterio de Akaike y de información Bayesiano), y de la comparación de las predicciones con la mortalidad general30. En el caso de las complicaciones potenciales, el modelo reproduce los resultados de los ensayos y se basa en los últimos valores observados durante el seguimiento para extrapolar su ocurrencia a lo largo de 15 años.
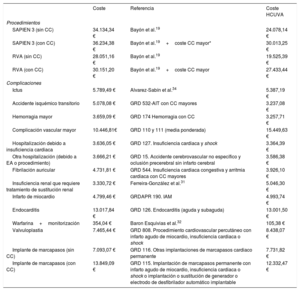
Costes y utilidadesSe tuvieron en cuenta costes (en euros de 2019) relacionados con el procedimiento, la hospitalización y las complicaciones tras la intervención y durante el seguimiento. Se imputaron de forma desagregada a partir de datos publicados19,31,32 y de la información aportada por el servicio de contabilidad analítica del Hospital Clínico Universitario Virgen de la Arrixaca (HCUVA). Para los costes por procedimiento se comprobaron también los grupos relacionados de diagnóstico33 (tabla 2 y tabla 3). Por su parte, los costes asociados con el seguimiento se estimaron en función de la clase funcional de la NYHA (con/sin ictus)34,35. Se asumió que los pacientes con ictus previo tendrían un coste adicional (tabla 4)36.
Costes incluidos en el modelo: procedimiento y complicaciones
| Coste | Referencia | Coste HCUVA | |
|---|---|---|---|
| Procedimientos | |||
| SAPIEN 3 (sin CC) | 34.134,34 € | Bayón et al.19 | 24.078,14 € |
| SAPIEN 3 (con CC) | 36.234,38 € | Bayón et al.19+coste CC mayor* | 30.013,25 € |
| RVA (sin CC) | 28.051,16 € | Bayón et al.19 | 19.525,39 € |
| RVA (con CC) | 30.151,20 € | Bayón et al.19+coste CC mayor | 27.433,44 € |
| Complicaciones | |||
| Ictus | 5.789,49 € | Alvarez-Sabín et al.34 | 5.387,19 € |
| Accidente isquémico transitorio | 5.078,08 € | GRD 532-AIT con CC mayores | 3.237,08 € |
| Hemorragia mayor | 3.659,09 € | GRD 174 Hemorragia con CC | 3.257,71 € |
| Complicación vascular mayor | 10.446,81€ | GRD 110 y 111 (media ponderada) | 15.449,63 € |
| Hospitalización debido a insuficiencia cardiaca | 3.636,05 € | GRD 127. Insuficiencia cardiaca y shock | 3.364,39 € |
| Otra hospitalización (debido a EA o procedimiento) | 3.666,21 € | GRD 15. Accidente cerebrovascular no específico y oclusión precerebral sin infarto cerebral | 3.586,38 € |
| Fibrilación auricular | 4.731,81 € | GRD 544. Insuficiencia cardiaca congestiva y arritmia cardiaca con CC mayores | 3.926,10 € |
| Insuficiencia renal que requiere tratamiento de sustitución renal | 3.330,72 € | Ferreira-González et al.31 | 5.046,30 € |
| Infarto de miocardio | 4.799,46 € | GRDAPR 190. IAM | 4.993,74 € |
| Endocarditis | 13.017,84 € | GRD 126. Endocarditis (aguda y subaguda) | 13.001,50 € |
| Warfarina+monitorización | 354,04 € | Baron Esquivias et al.32 | 105,38 € |
| Valvuloplastia | 7.465,44 € | GRD 808. Procedimiento cardiovascular percutáneo con infarto agudo de miocardio, insuficiencia cardiaca o shock | 8.438,07 € |
| Implante de marcapasos (sin CC) | 7.093,07 € | GRD 116. Otras implantaciones de marcapasos cardiaco permanente | 7.731,82 € |
| Implante de marcapasos (con CC) | 13.849,09 € | GRD 115. Implantación de marcapasos permanente con infarto agudo de miocardio, insuficiencia cardiaca o shock o implantación o sustitución de generador o electrodo de desfibrilador automático implantable | 12.332,47 € |
APR: all-patient refined; CC: complicaciones; EA: estenosis aórtica; GRD: grupo relacionado de diagnóstico; HCUVA: Hospital Clínico Universitario Virgen de la Arrixaca; IAM: infarto agudo de miocardio; RVA: reemplazo de quirúrgico válvula aórtica.
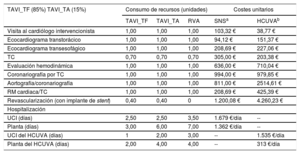
Consumos de recursos para la preparación del procedimiento y hospitalización
| TAVI_TF (85%) TAVI_TA (15%) | Consumo de recursos (unidades) | Costes unitarios | |||
|---|---|---|---|---|---|
| TAVI_TF | TAVI_TA | RVA | SNSa | HCUVAb | |
| Visita al cardiólogo intervencionista | 1,00 | 1,00 | 1,00 | 103,32 € | 38,77 € |
| Ecocardiograma transtorácico | 1,00 | 1,00 | 1,00 | 94,12 € | 151,37 € |
| Ecocardiograma transesofágico | 1,00 | 1,00 | 1,00 | 208,69 € | 227,06 € |
| TC | 0,70 | 0,70 | 0,70 | 305,00 € | 203,38 € |
| Evaluación hemodinámica | 1,00 | 1,00 | 1,00 | 636,00 € | 710,04 € |
| Coronariografía por TC | 1,00 | 1,00 | 1,00 | 994,00 € | 979,85 € |
| Aortografía/coronariografía | 1,00 | 1,00 | 1,00 | 811,00 € | 2514,61 € |
| RM cardiaca/TC | 1,00 | 1,00 | 1,00 | 208,69 € | 425,39 € |
| Revascularización (con implante de stent) | 0,40 | 0,40 | 0 | 1.200,08 € | 4.260,23 € |
| Hospitalización | |||||
| UCI (días) | 2,50 | 2,50 | 3,50 | 1.679 €/día | -- |
| Planta (días) | 3,00 | 6,00 | 7,00 | 1.362 €/día | -- |
| UCI del HCUVA (días) | 1 | 2,00 | 3,00 | -- | 1.535 €/día |
| Planta del HCUVA (días) | 2,00 | 4,00 | 4,00 | -- | 313 €/día |
HCUVA: Hospital Clínico Universitario Virgen de la Arrixaca; RM: resonancia magnética; RVA: reemplazo quirúrgico válvula aórtica; SNS: Sistema Nacional de Salud; TAVI_TA: implante percutáneo de válvula aórtica vía transapical; TAVI_TF: implante percutáneo de válvula aórtica vía transfemoral; TC: tomografía computarizada; UCI: unidad de cuidados intensivos.
Costes del tratamiento clínico durante el seguimiento de los pacientes en el horizonte de 15 años
| Costes anuales (euros, enero de 2019) | Fuente | |
|---|---|---|
| Clase NYHA sin ictus | ||
| Clase I | 116,00 | Presunción confirmada por experto (1 visita especialista+ECG) |
| Clase II | 4.115,18 | Delgado et al.35 |
| Clase III | 7.419,75 | Delgado et al.35 |
| Clase IV | 7.419,75 | Delgado et al.35 |
| Clase NYHA con ictus | ||
| Clase I | 759,00 | Mar et al.36 |
| Clase II | 4.432,18 | Delgado et al.35 |
| Clase III | 7.475,75 | Delgado et al.35 |
| Clase IV | 7.475,75 | Delgado et al.35 |
ECG: electrocardiograma; NYHA: New York Heath Association (clase funcional).
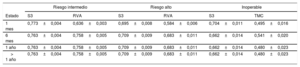
Las utilidades asignadas a cada estado de salud se extrajeron del ensayo PARTNER 2 mediante el instrumento EQ-5D37,38. Se realizaron los ajustes necesarios con los pesos de la población española (tabla 5)14. No se emplearon descuentos adicionales en utilidades debido a que se aplicaron los valores extraídos de los ensayos a lo largo del seguimiento que ya recogían el impacto de la aparición de cada evento. Así, se evitó duplicar su impacto, ya que beneficiaría a la alternativa con menor tasa de ocurrencia (S3).
Utilidades en cada perfil de riesgo evaluado a lo largo del seguimiento
| Riesgo intermedio | Riesgo alto | Inoperable | ||||
|---|---|---|---|---|---|---|
| Estado | S3 | RVA | S3 | RVA | S3 | TMC |
| 1 mes | 0,773±0,004 | 0,636±0,003 | 0,695±0,008 | 0,584±0,006 | 0,704±0,011 | 0,495±0,016 |
| 6 mes | 0,763±0,004 | 0,758±0,005 | 0,709±0,009 | 0,683±0,011 | 0,662±0,014 | 0,541±0,020 |
| 1 año | 0,763±0,004 | 0,758±0,005 | 0,709±0,009 | 0,683±0,011 | 0,662±0,014 | 0,480±0,023 |
| > 1 año | 0,763±0,004 | 0,758±0,005 | 0,709±0,009 | 0,683±0,011 | 0,662±0,014 | 0,480±0,023 |
RVA: reemplazo quirúrgico de válvula aórtica
S3: SAPIEN 3; TMC: tratamiento médico conservador.
Los valores expresan media±desviación estándar. Fuente: PARTNER37,38.
Se aplicó una tasa de descuento anual del 3% a costes y beneficios39.
Incertidumbre y análisis de sensibilidadSiendo los modelos de Markov una representación matemática de la realidad, es inherente cierto grado de incertidumbre, que se debe tratar. Para ello, se siguieron distintos análisis comenzando por la revisión del modelo por expertos médicos, que confirmaron su validez estructural. También la robustez de los resultados se testó con un análisis de sensibilidad probabilístico con 1.000 simulaciones de Monte Carlo del CCUI. A tal fin, además de las distribuciones en los parámetros clínicos ya comentadas, se asumió una distribución Gamma en costes y Beta en utilidades, dado su mejor ajuste a los datos observados. Mediante este análisis, se realizan otras tantas estimaciones del CCUI modificando a la vez los parámetros de costes y efectividad en toda su amplitud, con el fin de estimar la probabilidad de que los CCUI se sitúen por debajo de los umbrales normalmente definidos. Esto se complementó con un análisis de escenarios considerando distintos porcentajes de uso de las vías transfemoral y transapical. Esta última suele asociarse con peores resultados31,40 y en nuestro país el porcentaje de implantes por esta vía suele ser menor.
Por último, se repitió el análisis considerando los consumos de recursos sanitarios registrados en un estudio prospectivo llevado a cabo en el HCUVA que, debido a su alta experiencia y sus protocolos definidos, resulta interesante para conocer la perspectiva de un centro con alta actividad en TAVI. Se recogió información de 76 casos consecutivos con implante de S3 durante 1 año de seguimiento. La media de edad de los pacientes fue 82,5 años, con un score medio de la Society of Thoracic Surgeons (STS) de 5,33±3,37, y el 81,6% mostraba limitaciones graves, con NYHA III/IV. Con estos datos, se analizaron los resultados a 15 años y también tras el primer año desde la intervención para aportar una visión cercana a la gestión del servicio.
Comité de éticaLa información relativa al análisis de escenario con datos propios del HCUVA se recogió a partir de un estudio prospectivo aprobado por el Comité de Ética en Investigación Clínica del Hospital Clínico Universitario Virgen de la Arrixaca el 24 de julio de 2017 (código CEIC 2017-6-5-HCUVA).
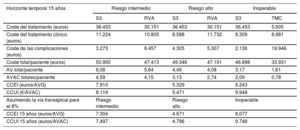
RESULTADOSA 15 años, el S3 resultó superior a las alternativas en los grupos analizados. Así, en los PI, los AVG por paciente asociados con el S3 fueron de 3,17 años, casi el doble que con el TMC (1,61 años). Frente al RVA, el S3 implicó también una mayor esperanza de vida para los PRA (4,49 AVG con S3 frente a 4,08 con RVA) y los PRI (6,08 con S3 frente a 5,64 con RVA). Cuando se ajustaron por calidad (utilidades), las diferencias en efectividad se mantuvieron en el caso de la alternativa RVA y fueron proporcionalmente mayores en el caso de los PI (2,09 AVAC con S3 frente a 0,78 con TMC). En todos los casos el S3 implicó un menor consumo de recursos por estancias hospitalarias asociadas con el procedimiento y el seguimiento por una menor tasa de complicaciones (tabla 1 y tabla 6).
Resultados de evaluación económica de SAPIEN 3: caso base con perspectiva nacional
| Horizonte temporal 15 años | Riesgo intermedio | Riesgo alto | Inoperable | |||
|---|---|---|---|---|---|---|
| S3 | RVA | S3 | RVA | S3 | TMC | |
| Coste del tratamiento (euros) | 36.453 | 30.151 | 36.453 | 30.151 | 36.453 | 5.005 |
| Coste del tratamiento clínico (euros) | 11.224 | 10.805 | 8.588 | 11.732 | 8.309 | 8.981 |
| Coste de las complicaciones (euros) | 3.273 | 6.457 | 4.305 | 5.307 | 2.136 | 19.946 |
| Coste total/paciente (euros) | 50.950 | 47.413 | 49.346 | 47.191 | 46.898 | 33.931 |
| AV total/paciente | 6,08 | 5,64 | 4,49 | 4,08 | 3,17 | 1,61 |
| AVAC totales/paciente | 4,59 | 4,15 | 3,13 | 2,74 | 2,09 | 0,78 |
| CCEI (euros/AVG) | 7.910 | 5.329 | 8.243 | |||
| CCUI (€/AVAC) | 8.119 | 5.471 | 9.948 | |||
| Asumiendo la vía transapical para el 8% | Riesgo intermedio | Riesgo alto | Inoperable | |||
| CCEI 15 años (euros/AVG) | 7.304 | 4.671 | 8.077 | |||
| CCUI 15 años (euros/AVAC) | 7.497 | 4.796 | 9.748 | |||
AV: años de vida; AVAC: años de vida ajustados por calidad; AVG: años de vida ganados; CCEI: cociente de coste-efectividad incremental; CCUI: cociente de coste-utilidad incremental; RVA: reemplazo quirúrgico de la válvula aórtica; S3: SAPIEN 3; TMC: tratamiento médico conservador.
A partir de estos datos, el S3 se mostró como una medida coste-efectiva en las 3 poblaciones con CCUI por debajo de los umbrales normalmente asumidos de 30.000 euros/AVAC (tabla 6, figura 2). Si bien el coste de adquisición de la tecnología y la intervención es superior al de la cirugía convencional y, por supuesto, el tratamiento farmacológico, los ahorros por un menor consumo de recursos sanitarios asociado con el tratamiento de las complicaciones y la menor hospitalización requerida (2,5 días de estancia en unidad de cuidados intensivos frente a 3,5 días en RVA y 3-6 días, dependiendo del abordaje vascular, en planta frente a 7 días en RVA) compensaron en gran parte las diferencias anteriores. Con estos datos, las CCUI fueron de 9.948 euros/AVAC en población con riesgo inasumible, 5.471 euros/AVAC en los PRA y 8.119 euros/AVAC en los PRI (tabla 6).
Análisis de sensibilidad probabilístico de Monte Carlo con 1.000 simulaciones del cálculo del cociente de coste-utilidad incremental de SAPIEN 3. AVAC: años de vida ajustados por calidad; HCUVA: Hospital Clínico Universitario Virgen de la Arrixaca; IC95%: intervalo de confianza del 95%; IC99%: intervalo de confianza del 99%; RVA: reemplazo quirúrgico de la válvula aórtica; TMC: tratamiento médico conservador.
En el análisis de sensibilidad probabilístico, el S3 resultó una opción coste-efectiva en más del 95% de las simulaciones con PI, el 87,8% con PRA y el 74,9% con PRI (figura 2).
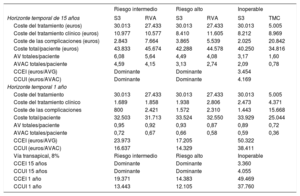
En el análisis de escenarios con la información de consumos y costes del HCUVA, los resultados fueron favorables al S3 (tabla 7, figura 2) y poco sensibles a cambios en parámetros relevantes como el horizonte temporal definido en el análisis. El S3 resultó coste-efectivo considerando solo el primer año frente al RVA en PRI y PRA (tabla 7). No así respecto al TMC en PI, ya que el coste del tratamiento médico es menor y el marco temporal no permite recoger las complicaciones asociadas ni el consumo de recursos a partir de ese periodo.
Resultados de la evaluación económica de SAPIEN 3: análisis de sensibilidad con perspectiva del Hospital Clínico Universitario Virgen de la Arrixaca (centro con alto volumen de implantes percutáneos)
| Riesgo intermedio | Riesgo alto | Inoperable | ||||
|---|---|---|---|---|---|---|
| Horizonte temporal de 15 años | S3 | RVA | S3 | RVA | S3 | TMC |
| Coste del tratamiento (euros) | 30.013 | 27.433 | 30.013 | 27.433 | 30.013 | 5.005 |
| Coste del tratamiento clínico (euros) | 10.977 | 10.577 | 8.410 | 11.605 | 8.212 | 8.969 |
| Coste de las complicaciones (euros) | 2.843 | 7.664 | 3.865 | 5.539 | 2.025 | 20.842 |
| Coste total/paciente (euros) | 43.833 | 45.674 | 42.288 | 44.578 | 40.250 | 34.816 |
| AV totales/paciente | 6,08 | 5,64 | 4,49 | 4,08 | 3,17 | 1,60 |
| AVAC totales/paciente | 4,59 | 4,15 | 3,13 | 2,74 | 2,09 | 0,78 |
| CCEI (euros/AVG) | Dominante | Dominante | 3.454 | |||
| CCUI (euros/AVAC) | Dominante | Dominante | 4.169 | |||
| Horizonte temporal 1 año | ||||||
| Coste del tratamiento | 30.013 | 27.433 | 30.013 | 27.433 | 30.013 | 5.005 |
| Coste del tratamiento clínico | 1.689 | 1.858 | 1.938 | 2.806 | 2.473 | 4.371 |
| Coste de las complicaciones | 800 | 2.421 | 1.572 | 2.310 | 1.443 | 15.668 |
| Coste total/paciente | 32.503 | 31.713 | 33.524 | 32.550 | 33.929 | 25.044 |
| AV totales/paciente | 0,95 | 0,92 | 0,93 | 0,87 | 0,89 | 0,72 |
| AVAC totales/paciente | 0,72 | 0,67 | 0,66 | 0,58 | 0,59 | 0,36 |
| CCEI (euros/AVG) | 23.973 | 17.205 | 50.322 | |||
| CCUI (euros/AVAC) | 16.637 | 14.329 | 38.411 | |||
| Vía transapical, 8% | Riesgo intermedio | Riesgo alto | Inoperable | |||
| CCEI 15 años | Dominante | Dominante | 3.360 | |||
| CCUI 15 años | Dominante | Dominante | 4.055 | |||
| CCEI 1 año | 19.371 | 14.383 | 49.469 | |||
| CCUI 1 año | 13.443 | 12.105 | 37.760 | |||
AV: años de vida; AVAC: años de vida ajustados por calidad; AVG: años de vida ganados; CCEI: cociente de coste-efectividad incremental; CCUI: cociente de coste-utilidad incremental; RVA: reemplazo quirúrgico de la válvula aórtica; S3: SAPIEN 3; TMC: tratamiento médico conservador.
El TAVI ha revolucionado el tratamiento de la EA41, y se lo considera la primera opción en casos con riesgo alto o inoperables. La válvula S3ha recibido aprobación para pacientes con bajo riesgo tras el estudio PARTNER S3i17. Anteriormente ya se había considerado junto con la EVOLUT (Medtronic, Estados Unidos) como la prótesis indicada en casos de riesgo intermedio (STS 4-8%)21. Esta expansión requiere una evaluación en términos de coste-beneficio, especialmente cuando el coste de adquisición para el TAVI es mayor que su alternativa.
En el presente análisis, el implante de S3 resulta una opción coste-efectiva o incluso dominante en el tratamiento de la EA en PRI, PRA y PI. Los CCUI en todas las indicaciones se situaron por debajo de los umbrales estimados en nuestro país42,43, mostrando además cocientes de coste-utilidad favorables en comparación con las de otros dispositivos o fármacos aceptados44–47.
Este trabajo coincide con evaluaciones económicas publicadas en Francia23, Canadá22 y Estados Unidos, donde la válvula S3 incluso se mostró dominante respecto al RVA48 en PRI. Respecto a España, no hay precedentes que tengan en cuenta las características de la última generación de la prótesis. Nuestros resultados son similares a los publicados en 2013 por Ferreira et al., sobre pacientes con alto riesgo en un horizonte temporal de 3 años31. En un informe previo de evaluación con horizonte temporal comparable19, el TAVI no parecía coste-efectivo. Pero un aspecto de incertidumbre señalado por sus autores fue la escasa información sobre efectividad que permitiera compensar su coste de adquisición. En nuestro estudio, se incluye información de ensayos posteriores y se consideran costes de seguimiento en función de la clase funcional de los pacientes, más ajustados a su realidad, lo que podría explicar las diferencias en los hallazgos.
En otra publicación con datos de práctica clínica entre 2011 y 201328, se indicaba que el TAVI podría resultar eficiente si el coste del implante se reducía un 30% y dependiendo de los costes asociados con la hospitalización y las características de los pacientes. En nuestro análisis, se consideran estancias hospitalarias más cortas y cercanas a la realidad actual, en planta y en unidad de cuidados intensivos.
En esta línea, el análisis con datos económicos del HCUVA muestra que la optimización del implante y la recuperación posterior redundan en la mayor eficiencia del dispositivo, que consigue resultados ya en el primer año muy favorables. Además, el implante de S3 implicaría una reducción importante de las complicaciones relacionadas con la intervención22,23.
La principal limitación del trabajo se debe precisamente a que la información del beneficio procede de estudios en situaciones más o menos controladas18,37. Se debe incorporar evidencia de práctica clínica real para obtener una estimación más precisa a escala nacional.
Además, en los PRI consideramos datos del PARTNER 2 sobre RVA (STS, 4-8%) y se compara con SAPIEN siguiendo el análisis ajustado de riesgos26. No obstante, debe tenerse en cuenta que la S3ha mostrado mejores resultados que la anterior prótesis (SAPIEN XT) en un reciente metanálisis49. Otra limitación es que los resultados solo se pueden aplicar al S3, y puede haber diferencias entre prótesis percutáneas, por lo que estos análisis deben individualizarse50,51. Tampoco se ha tenido en cuenta la durabilidad de la prótesis, factor que puede ser determinante en la eficiencia, aunque la tasa de deterioro parece ser baja (el 4% grave a 5 años en el registro FRANCE 252). Finalmente, también se podría estudiar en pacientes con otras afecciones que empeoran el pronóstico (insuficiencia renal, neumopatía crónica…)53.
CONCLUSIONESEl tratamiento de pacientes con EA mediante TAVI con S3 es una opción efectiva tanto para PI como PRA y PRI, pero además existe una alta probabilidad de que resulte la estrategia más eficiente. Con el envejecimiento de la población y la creciente presión asistencial, es necesario contar con innovaciones tecnológicas menos invasivas, que apuntan hacia la simplificación de los procesos, a la vez que se mantienen las garantías de éxito clínico y se optimizan recursos.
- –
La indicación de TAVI se ha ampliado a pacientes con EA sintomática con riesgo quirúrgico intermedio e incluso bajo debido a resultados clínicos publicados.
- –
En España, no hay ensayos sobre la eficiencia del uso de S3 en PRI que incorpore la última evidencia disponible.
- –
Respecto a las alternativas terapéuticas para cada indicación, el S3 se asocia con un menor consumo de recursos sanitarios en términos de estancia hospitalaria y tratamiento de las complicaciones durante el seguimiento.
- –
El implante de S3 resulta coste-efectivo en el tratamiento de la EA grave en PRI, PRA y PI.
- –
En centros con experiencia, este perfil favorable se observa tras el primer año desde la intervención.
Edwards Lifesciences SL, España, proporcionó fondos para el análisis de la evaluación económica, que fue planificado, interpretado y discutido con independencia por los autores.
CONTRIBUCIÓN DE LOS AUTORESE. Pinar participó en la obtención de datos clínicos, el análisis de los costes, el tratamiento estadístico, la preparación de los resultados, la redacción del manuscrito y su revisión. J. García de Lara participó en la obtención de datos clínicos y la redacción del manuscrito. J. Hurtado participó en la obtención de datos clínicos y la redacción del manuscrito. M. Robles colaboró en la obtención de datos económicos y la redacción del manuscrito. G. Leithold participó en la obtención de datos clínicos y la redacción del manuscrito. B. Martí-Sánchez participó en el análisis de los costes, la preparación de los resultados, la redacción del manuscrito y su revisión. J. Cuervo participó en el análisis de los datos clínicos y de los costes, el tratamiento estadístico, la preparación de los resultados, la redacción del manuscrito y su revisión. D.A. Pascual participó en la obtención de datos clínicos y la redacción del manuscrito. A. Estévez-Carrillo participó en el análisis de los datos clínicos y de los costes, el tratamiento estadístico, la preparación de los resultados y la redacción del manuscrito. C. Crespo participó en el análisis de los datos clínicos y de los costes, el tratamiento estadístico, la preparación de los resultados y la redacción del manuscrito. Todos los autores revisaron y están de acuerdo con la versión final del manuscrito.
CONFLICTO DE INTERESESB. Martí-Sánchez es empleada de Edwards Lifesciences. J. Cuervo, A. Estévez-Carrillo y C. Crespo son miembros de Axentiva Solutions, que recibió honorarios de consultoría de Edwards Lifesciences.